原子结构与元素的性质 知识点题库
X和Y是短周期元素,二者能形成化合物X2Y3 , 若Y的原子序数为n,则X的原子序数不可能是( )
A . n﹣8
B . n﹣3
C . n﹣1
D . n+5
短周期的A,B,C,D,E物种元素,原子序数依次增大.已知元素A的气态氢化物和A的最高价氧化物对应的水化物反应生成盐;B,E为同主族元素,B元素原子最外层电子数是次外层的3倍;D是地壳中含量最多的金属元素;C是短周期中与水反应最激烈的金属元素.下列叙述不正确的是( )
A . 原子半径:C>D>B
B . 元素B的气体氢化物的沸点比元素E气体氢化物的沸点高
C . 元素A的氧化物的大量排放能引起温室效应
D . 元素C,D,E的最高价氧化物对应的水化物两两之间能发生反应
下列各组指定原子序数的元素,能形成A2B3型化合物的是( )
A . 6和8
B . 11和9
C . 12和17
D . 13和8
X,Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的代数和为6,X和Y两元素形成的化合物为R,则下列关于R的叙述正确的是( )
A . R一定是共价化合物
B . R一定是离子化合物
C . R可能是共价化合物,也可能是离子化合物
D . R可能是液态物质,也可能是固态物质
某短周期元素R原子的最外层P轨道上的未成对电子只有2个.下列关于R的描述中正确的是( )
A . R的氧化物都能溶于水
B . R的最高价氧化物对应的水化物都是H2RO3
C . R是非金属元素
D . R的氧化物都能与NaOH溶液反应
某元素X的气态氢化物的化学式为H2X,则X的最高价氧化物的水化物的化学式为( )
A . H2XO3
B . HXO3
C . H3XO4
D . H2XO4
某元素原子的最外层电子数与次外层电子数相同,且最外层电子数与次外层电子数之和小于8,它是( )
A . 锂
B . 铍
C . 氦
D . 钙
下列说法不正确的是( )
①质子数相同的粒子一定属于同一种元素
②同一元素的核素种数由中子数决定
③同位素的化学性质几乎相同
④质子数相同、电子数也相同的两种粒子,不可能是一种分子和一种离子
⑤16O2与18O3两种物质互为同素异形体.
A . ③
B . ④
C . ②⑤
D . ①
下列各组原子中,彼此化学性质一定相似的是( )
A . 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B . 原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C . 2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y原子
D . 最外层都只有一个电子的X,Y原子
W,X,Y,Z是原子序数依次增大的短周期元素,X,Y是金属元素,X的焰色呈黄色.W,Z最外层电子数相同,Z的核电荷数是W的2倍.工业上一般通过电解氧化物的方法获得Y的单质,则下列说法不正确的是( )
A . W,X,Y形成的简单离子核外电子数相同
B . Z和W可形成原子个数比为1:2和1:3的共价化合物
C . Y和Z形成的化合物可以通过复分解反应制得
D . X,Y和Z三种元素形成的最高价氧化物对应的水化物能两两反应
核电荷数小于18的某元素X,某原子核外电子层数为a,最外层电子数为(2a+1),下列有关元素X的说法中,不正确的是( )
A . 元素X的原子核内质子数为(2a2﹣1)
B . 元素X的原子半径一定小于钠的原子半径
C . 由元素X形成的某些化合物,可能具有杀菌消毒的作用
D . 元素X形成的简单离子,各电子层的电子数均达到2n2个(n表示电子层数)
短周期主族元素W、R、X、Y、Z的原子序数依次增大,W的原子半径是周期表中所有元素中最小的,R是地壳中含量最多的元素,X与W同主族,Y是最外层电子数是最内层电子数的3倍.下列说法正确的是( )
A . 原子半径:R<Y<Z
B . 简单氢化物的热稳定性:R>Y
C . R与Y只能形成一种化合物
D . 最高价氧化物的水化物酸性:Y>Z
某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的核电荷数为( )
A . 11
B . 15
C . 17
D . 34
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有5个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
-
(1) A的最高价氧化物的水化物是(填化学式);
-
(2) 物质E中所包含的化学键有,写出C、D两元素形成的化合物C2D的电子式;
-
(3) 把盛有48mLAB、AB2混合气体的容器倒置于水中(同温、同压下),待液面稳定后,容器内气体体积变为24mL,则原混合气体中AB的体积分数为。
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中正确的是( )
A . X、M两种元素只能形成X2M型化合物
B . Y 的气态简单氢化物的热稳定性比W 的强
C . X2M、YM2中含有相同类型的化学键
D . 元素W和M的某些单质可作为水处理中的消毒剂
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据表所列数据判断错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
A . 元素X的常见化合价是+1
B . 元素Y是ⅢA族元素
C . 元素X与氯形成化合物时,化学式可能是XCl
D . 若元素Y处于第三周期,它可与冷水剧烈反应
2013年2月朝鲜进行了第三次核试验,引起国际社会的极大关注。 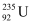 是一种重要的核燃料,下列有关
是一种重要的核燃料,下列有关 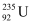 的说法正确的是( )
的说法正确的是( )
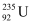 是一种重要的核燃料,下列有关
是一种重要的核燃料,下列有关 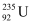 的说法正确的是( )
的说法正确的是( )
A . 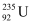 原子核中含有92个中子
B .
原子核中含有92个中子
B . 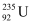 原子核外有143个电子
C .
原子核外有143个电子
C . 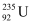 与
与  互为同位素
D .
互为同位素
D . 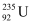 与
与  是两种不同的元素
是两种不同的元素
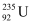 原子核中含有92个中子
B .
原子核中含有92个中子
B . 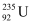 原子核外有143个电子
C .
原子核外有143个电子
C . 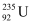 与
与  互为同位素
D .
互为同位素
D . 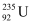 与
与  是两种不同的元素
是两种不同的元素
X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为+4价,Y元素与Z元素相邻,且化合物Z2X4的电子总数为18个;X与M元素同主族;Q元素的原子最外层电子数比次外层少一个电子。下列说法错误的是( )
A . 最高价氧化物对应水化物的酸性:Q>Z>Y
B . 原子半径:Z<Y<M
C . X、Z和Q三种元素形成的化合物一定是共价化合物
D . X2Z-ZX2易溶于水,其水溶液呈碱性
某元素的原子结构示意图为 。下列关于该元素的说法中,错误的是( )
。下列关于该元素的说法中,错误的是( )
 。下列关于该元素的说法中,错误的是( )
。下列关于该元素的说法中,错误的是( )
A . 元素符号是Ca
B . 属于金属元素
C . 在化学反应中易得电子
D . 最高正化合价是+2价
硅及其化合物在生产生活中有广泛应用。根据所学知识,回答下列问题:
-
(1) 三甲基卤硅烷【(CH3)3SiX,X为Cl、Br、I】是重要的化工原料。
①氯元素基态原子的价电子排布式为;按照核外电子排布对元素周期表分区,溴元素位于区;基态硅原子中有种运动状态不同的电子。
②Br、I的第一电离能的大小关系:I1(Br)I1(I)(填“大于”“小于”或“等于”)。
③常温下,(CH3)3SiI中Si—I键比(CH3)3SiCl中Si—Cl键易断裂的原因是。
-
(2) (CH3)3SiCl可作为下列有机合成反应的催化剂。
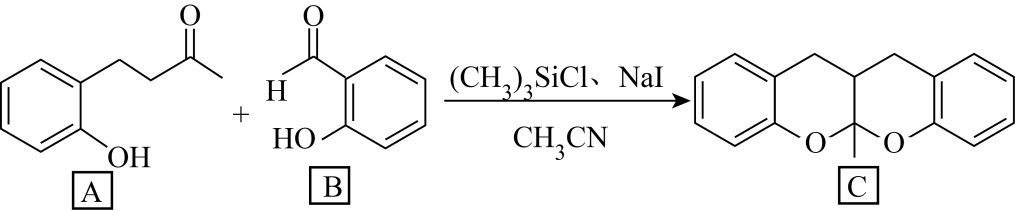
①1个有机物A分子中采取sp2杂化的碳原子有个。
②有机物B的沸点低于对羟基苯甲醛(
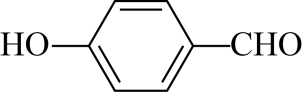 )的沸点,其原因是。
)的沸点,其原因是。③CH3CN中σ键与π键的个数比为。
-
(3) 一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(a、b方向的夹角为120°,c方向垂直于a、b方向,棱长a+b≠c),如图甲所示;晶胞中碳原子的投影位置如图乙所示。
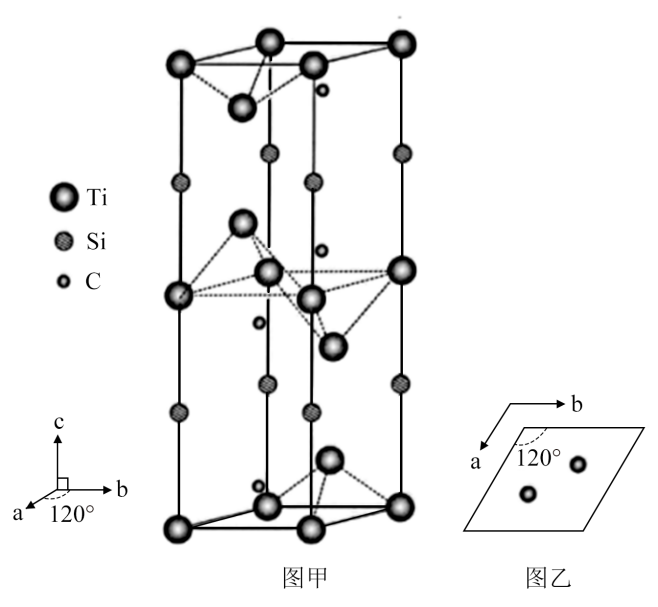
①该钛硅碳新型材料的化学式为。
②已知该新型材料的密度为4.51g•cm-3 , 且a、b的长度均为307pm,阿伏加德罗常数的值用NA表示,则c的长度为pm (列出计算式)。
最近更新
- 已知i,j,k是两两垂直的单位向量,a=2i-j+k,b=i+j-3k,则a·b等于( )A.-2
- 将“平行于同一条直线的两条直线平行”改写成“如果……那么……”的形式为 .
- Isn’t it time you got down to the papers? A.mark
- 上题材料还体现,我国在社会主义民主政治建设中坚持和完善 A.人民代表大会制度 B.民族区域自治制度 C.基
- 以下收录某部著作中的一段师生对话录 生:“必有是理,然后有是气,如何?” 师:“此本兄先后之可言,然比欲推其所从来,则需
- 文学常识: 居里夫人,原名玛丽·斯克罗多斯卡, 著名的 家和 家,曾两度荣获
- 下列有关人类染色体与遗传病的叙述,正确的是 ( ) A、 男性精子的染色体组成
- 下列实验操作中,主要不是从安全因素考虑的是() A.点燃氢气前一定要检验氢气的纯度 B.未使用完的白磷要随时收集起来,并
- 下列说法中,正确的是 A.只要导体在磁场中运动,就会产生感应电流 B.电动机是利用电磁感应现象制成的 C.发电机是把电
- 下列物质:①氮气、②液态氧气、③氧化镁、④自来水、⑤高锰酸钾、⑥矿泉水⑦铁粉、⑧冰水混合物,选择正确的答案用序号填入空格
- 化学知识与人类生活息息相关,下列有关说法错误的是( ) A.回收利用废旧金属是保护金属资源的有效途径之一 B.天
- 阅读古诗《使至塞上》,完成下面题目。(4分)使至塞上王维单车欲问边,属国过居延。征蓬出汉塞,归雁入胡天。大漠孤烟直,长河
- △ABC中,,,则△ABC是( )三角形 A.锐角 B.钝角 C.直角 D.等腰
- 某温度下,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是A.a点表示Ag2SO4的不饱和溶液,加入Na2
- 把 (-8)-(+4)+(-5)-(-2)写成省略加号的和的形式是 ( ) A.-8+4-5+2 B
- 变量满足线性约束条件,则使目标函数取得最大值的最优解有无数个,则的值为 .
- 党的十七届四中全会通过的《中共中央加强和改进新形势下党的建设若干重大问题的决定》指出,党内民主是党的生命,要切实推进党内
- I don't like ______ as you read.A. the novels B. the s
- 废除丞相后,全国重大政务都由明太祖决断,他曾在八天之内,平均每天批阅奏章两百多件,处理国事四百多件。明太祖深感力不从心,
- 阅读下面材料,然后按照要求作文。 生活充满了矛盾。我们一方面对自己说对人要有爱心,爱人如爱己;一方面在外头又怕跟陌生人说



