研究物质结构的基本方法和实验手段 知识点题库
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是( )
A . 蒸馏常用于分离提纯液态有机混合物
B . 核磁共振氢谱通常用于分析有机物中氢的个数
C . 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团
D . 燃烧法是研究确定有机物元素组成的有效方法
下列装置及相应操作能达到实验目的的是( )
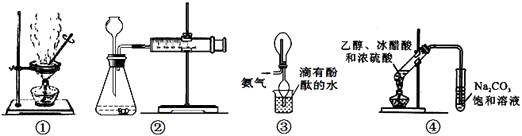
A . 装置①可用于“海带提碘”实验中将海带灼烧成灰
B . 装置②可用于H2O2分解速率的测定
C . 装置③可用于氨气的收集
D . 装置④可用于实验室制取乙酸乙酯
利用组成物质的原子、离子或分子的一些特征性质,检验组成化学物质的元素,是研究物质组成的常用方法.下列叙述不正确的是( )
A . 根据纤维在火焰上燃烧产生的气味,不能确定该纤维是否为蛋白质纤维
B . 用红外光谱仪确定物质中是否存在某些有机原子团
C . 用元素分析仪确定物质中是否含有C、H、O、N、S、Cl、Br等元素
D . 用原子吸收光谱确定物质中含有哪些金属元素
当有机物分子中的一个碳原子所连四个原子或原子团均不相同时,此碳原子就是“手性碳原子”,具有手性碳原子的物质往往具有旋光性,存在对映异构体,下列化合物中存在对映异构体的是( )
A . C2H5CH=CHCH(CH3)-CH=CHC2H5
B . 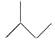 C . HCOOH
D . C6H5CH(CH3)CHO
C . HCOOH
D . C6H5CH(CH3)CHO
下列四种化学操作名称从左到右分别是()
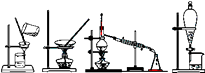
A . 过滤、蒸发、蒸馏、萃取分液
B . 过滤、蒸馏、蒸发、萃取分液
C . 蒸发、蒸馏、过滤、萃取分液
D . 萃取、蒸馏、蒸发、过滤分液
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等。过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量。
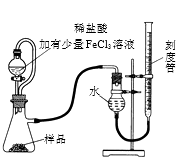
某研究小组拟用右图装置测定一定质量的样品中过氧化镁的含量。请回答:
-
(1) 稀盐酸中加入少量FeCl3溶液的作用是。
-
(2) 使用恒压分液漏斗的优点有:使分液漏斗中的溶液顺利滴下;。
-
(3) 实验结束时,待恢复至室温,先,
再平视刻度线读数。
氯化亚铜(CuCl)广泛应用于有机合成、染料、颜料、催化剂等工业。它是一种白色粉末,微溶于水,不溶于乙醇、稀硝酸及稀硫酸,可溶于氨水、浓盐酸,并生成配合物NH4[CuCl2];能在空气中迅速被氧化成绿色;见光则分解,变成褐色。下图是实验室制备氯化亚铜的流程图及实验装置图。
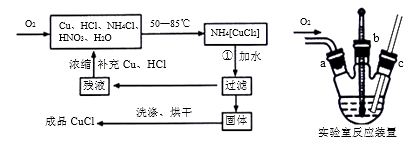
实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36%盐酸15mL、水。
-
(1) 请写出①的化学方程式。
-
(2) 本实验中通入O2的速率不宜过大,宜选择下图中的(填字母序号)方案,并说明选择该装置的理由。
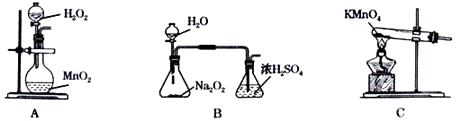
-
(3) 电炉加热升温至50℃时停止加热,反应快速进行,当烧瓶中液面上方的现象为时,停止通入氧气,打开瓶塞,沿C口倾出反应液于1000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出。
-
(4) 关于该实验过程中,下列说法正确的是 。A . 实验开始时,温度计显示反应液温度可能低于室温。 B . 流程中过滤操作,可以采用真空抽滤的方式,洗涤固体可以用95%的酒精。 C . 该实验流程中,残液中补充HCl的主要作用是抑制产物的水解。 D . 反应装置中使用长导管的目的是防止三颈烧瓶内气压过大。
-
(5) 氯化亚铜的定量分析:
①称取成品0.25g置于预先放入玻璃珠30粒和10mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.10 mol·L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表。(已知:CuCl + FeCl3 = CuCl2 + FeCl2 ,Fe2+ + Ce4+ = Fe3+ + Ce3+)
实验序号
1
2
3
滴定起始读数(mL)
0.75
0.50
0.80
滴定终点读数(mL)
24.70
24.95
24.85
④数据处理:计算得CuCl的纯度为。
测定胆矾晶体结晶水含量时,不会引起实验误差的操作是()
A . 称取一定量胆矾晶体,研磨后转入铁坩埚中进行加热
B . 大火加热,使胆矾晶体迅速升温失去结晶水并变黑
C . 停止加热后,硫酸铜固体放在空气中冷却再称量
D . 恒重操作时,连续两次称量结果相差 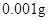 即停止加热
即停止加热
下列各组表述中,正确的是( )
A . 区分晶体和非晶体最可靠的科学方法是对固体进行 X-射线衍射
B . 离子键、金属键无方向性和饱和性,而所有共价键都有方向性和饱和性
C . 处于能量最低状态时,外围电子排布为4d15s2的某元素原子,M能层共有8个电子,该元素位于 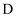 区第ⅢB族
D . 对充有氖气的霓虹灯管通电,灯管发出红色光.产生这一现象的主要原因是电子由基态向激发态跃迁时以光的形式释放能量
区第ⅢB族
D . 对充有氖气的霓虹灯管通电,灯管发出红色光.产生这一现象的主要原因是电子由基态向激发态跃迁时以光的形式释放能量
 区第ⅢB族
D . 对充有氖气的霓虹灯管通电,灯管发出红色光.产生这一现象的主要原因是电子由基态向激发态跃迁时以光的形式释放能量
区第ⅢB族
D . 对充有氖气的霓虹灯管通电,灯管发出红色光.产生这一现象的主要原因是电子由基态向激发态跃迁时以光的形式释放能量
化学是一门以实验为基础的学科,掌握基本实验方法和操作技能是做好化学实验的基础。下列说法错误的是( )
A . 元素分析仪可以确定物质中是否含有C、H、O、N、Cl 、Br等元素
B . 用红外光谱仪可以确定物质中是否存在某些有机原子团
C . 用原子吸收光谱可以确定物质中含有哪些金属元素
D . 瑞典化学家舍勒揭开了人工合成有机物的序幕
1999年度诺贝尔化学奖获得者艾哈迈德∙泽维尔(Ahmed H∙Zewail),快创了“飞秒(10-15)化学”的新领域,使运动激光光谱技术观测化学反应时分子中原子的运动成为可能。你认为该技术不能观察到的是( )
A . 化学变化中反应物分子的分解
B . 化学反应中原子的运动
C . 化学变化中生成物分子的形成
D . 原子核的内部结构
下列说法错误的是( )
A . 原子光谱可以用于定性鉴定元素
B . 霓虹灯能发出五颜六色的光,发光机理与氢原子光谱形成机理基本相同
C . 原子线状光谱的产生是原子核外电子在不同的能级之间跃迁所导致
D . 利用光谱仪只能测得原子的发射光谱
认识物质的空间结构可以借助某些实验手段来测定,下列有关说法错误的是( )
A . 在现代化学中,常利用原子光谱上的特征谱线来鉴定元素
B . 红外光谱仪可以用来测定分子结构
C . 通过测定物质的熔点和沸点可以确定物质是否含有配位键
D . 区别晶体和非晶体最可靠的科学方法是对固体进行X射线衍射实验
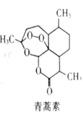
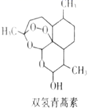
青蒿素转化为双氢青蒿素,其抗疟药效可提高10倍。转化过程如图所示:
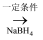
回答下列问题:
-
(1) 目前测定分子空间结构最普遍的方法是。
-
(2) 青蒿素三种元素的电负性由大到小的顺序是,双氢青蒿素比青蒿素水溶性好,原因是。
-
(3) 硼氢化钠(NaBH4)的制备方法为
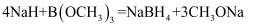 。
。 ①图甲是NaH的晶胞,若Na原子间最小核间距为b nm,则晶胞棱长为nm。
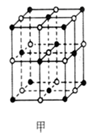
②图乙是NaBH4的晶胞,甲、乙两个晶胞中阳离子数目之比是,NaBH4晶体的密度为g/cm3(用含a的代数式表示)。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,图乙中原子1的坐标为(0,0,0),则原子2的坐标为。
下列实验操作正确的是( )
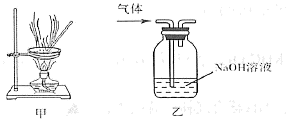
A . 实验室保存饱和FeCl2溶液时,应加入少量铁粉
B . 将4.0gNaOH固体置于100mL容量瓶中,加水至刻度,配制1.000 mol·L-1 NaOH标准溶液,滴定未知浓度的盐酸
C . 用装置甲蒸干AlCl3溶液制无水AlCl3固体
D . 用装置乙除去实验室所制乙烯中的少量SO2
下列说法正确的是( )
A . 含氧酸HClO、HBrO、HIO的电离平衡常数依次为
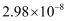 、
、
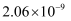 、
、
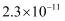 , 由此可知,氯、溴、碘的非金属性逐渐减弱
B . NaClO与少量
, 由此可知,氯、溴、碘的非金属性逐渐减弱
B . NaClO与少量
 反应生成HClO和
反应生成HClO和
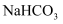 , 则
, 则
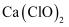 与少量
与少量
 反应生成HClO和
反应生成HClO和
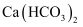 C . 向硅酸钠溶液中滴加盐酸,有白色胶状沉淀生成.可证明非金属性:Cl>Si
D . 化学腐蚀、电化学腐蚀本质上均为因金属失去电子发生氧化反应而被腐蚀
C . 向硅酸钠溶液中滴加盐酸,有白色胶状沉淀生成.可证明非金属性:Cl>Si
D . 化学腐蚀、电化学腐蚀本质上均为因金属失去电子发生氧化反应而被腐蚀
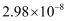 、
、
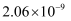 、
、
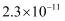 , 由此可知,氯、溴、碘的非金属性逐渐减弱
B . NaClO与少量
, 由此可知,氯、溴、碘的非金属性逐渐减弱
B . NaClO与少量
 反应生成HClO和
反应生成HClO和
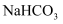 , 则
, 则
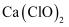 与少量
与少量
 反应生成HClO和
反应生成HClO和
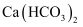 C . 向硅酸钠溶液中滴加盐酸,有白色胶状沉淀生成.可证明非金属性:Cl>Si
D . 化学腐蚀、电化学腐蚀本质上均为因金属失去电子发生氧化反应而被腐蚀
C . 向硅酸钠溶液中滴加盐酸,有白色胶状沉淀生成.可证明非金属性:Cl>Si
D . 化学腐蚀、电化学腐蚀本质上均为因金属失去电子发生氧化反应而被腐蚀
红磷是巨型共价分子,无定型结构,下列方法能证明红磷是非晶体的是( )
A . 质谱法
B . 原子发射光谱法
C . 核磁共振谱
D . X射线衍射法
随着科学技术的发展,人们可以利用很多先进的方法和手段来测定有机物的组成和结构。下列说法正确的是( )
A . 通过李比希元素分析仪可以确定有机物的分子式
B . 对乙醇和二甲醚进行质谱分析,质谱图完全相同
C . 利用红外光谱仪无法区分丁烯和环丁烷两种烃
D . X射线衍射图经过计算可获得键长和键角等数据
最近更新
- (原创)西洋某史家曾把中国两汉时代的历史,和罗马相比较,他说:凡罗马衰亡的原因,中国都有的。却有一件事,为中国所有,罗马
- 如图所示,将小砝码置于桌面上的薄纸板上,用水平向右的拉力将纸板迅速抽出,砝码的移动很小,几乎观察不到,这就是大家熟悉的惯
- 新中国成立后,我国对农村生产关系进行了几次重大调整,其中发生在建设中国特色社会主义新时期的措施是 A、土地改革
- 2011年10月9日,同志在纪念辛亥革命100周年大会上的讲话中说:“在实现中华民族伟大复兴的征程上,我们一定要大力弘扬
- .若是关于的一元二次方程,则的值应为( ) A. B. C.
- 2008年4月25日中国成功发射了首颗数据中继卫星“天链一号”,卫星准确定点于地球同步轨道。中继卫星享有“卫星的卫星”之
- 冬枣的种植已成为我县“特色农业”中的一部分,冬枣之所以受到人们的喜爱,是因为它不仅营养丰富,且又脆又甜,口感极佳。你知道
- 下面一段话中运用的修辞方法有( )。 风失去了雨前的野性,轻轻地抚摸着草根;水珠在草尖上闪光,像粒粒珍
- 地球同步卫星是指相对于地面不动的人造地球卫星,关于地球同步卫星,以下说法正确的是( )A.它可以在地面上任一
- 诱变育种有很多突出优点,也存在一些缺点,下列分析正确的是 ①结实率低,发育迟缓 ②提高变异频率,使后代变异性状较快稳定,
- 如下图,已知函数y=2cosx(0<x<2π)的图象和直线y=2围成一个封闭的平面图形,求这个封闭图形的面积.
- 对于函数,若存在区间,使得,则称函数为“可等域函数”,区间为函数的一个“可等域区间”.给出下列4个函数:①;②;③;④.
- 下列函数中,既是偶函数又在单调递增的函数是( ) A . B. C.
- 已知函数的图像过点P(一1,2),且在P点处的切线恰好与直线垂直. (1)求的函数关系式; (2)若在区间[]上单调递增
- 下图是一个生态系统部分结构示意图,据图分析回答:(1)图中的太阳光、水、空气、无机盐都属于生态系统中的 成分
- Pirates from Somalia who hijacked _____European carrier in _
- It’s kind YaoBeina to donate her corneas (眼角膜)
- 下列病症可以用孟德尔遗传规律预测后代患病概率的是() A.艾滋病 B.苯丙酮尿症 C.猫叫综合征
- ________ is no reason for dismissing her. A. Because she was
- 为测定碳酸钙纯度(设所含杂质为SiO2),同学们设计了如下两个实验方案: 【方案I】 (1)组装



