原子结构的构造原理 知识点题库
基态原子的核外电子在原子轨道上的能量大小关系不正确的是( )
A . 3s>2s
B . 3p>3s
C . 4s>3d
D . 3d>3s
下列有关多电子原子的叙述中,正确的是( )
A . 在一个多电子原子中,不可能有两个能量相同的电子
B . 在一个多电子原子中,不可能有两个运动状态完全相同的电子
C . 在一个多电子原子中,N层上的电子能量肯定比M层上的电子能量高
D . 某个多电子原子的3p能级上仅有两个电子,它们必然自旋状态不同
在d轨道中电子排布成 , 而不排成
, 而不排成 ,最直接的根据是( )
,最直接的根据是( )
 , 而不排成
, 而不排成 ,最直接的根据是( )
,最直接的根据是( )
A . 能量最低原理
B . 泡利原理
C . 构造原理示意图
D . 洪特规则
若将基态P原子的电子排布式写成1s22s22p63s23px23py1 , 它违背了( )
A . 泡利原理
B . 能量守恒原理
C . 构造原理
D . 洪特规则
有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同族,它们原子的最外层电子排布式为ns1。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。请回答下列问题:
-
(1) A是,B是,E是。
-
(2) 写出C元素基态原子的电子排布式:。
-
(3) 用电子排布图表示D元素原子的价电子构型:。
-
(4) 元素B与D的电负性的大小关系是B(填“>”“<”或“=”,下同)D,C与E的第一电离能大小关系是CE。
关于原子轨道的说法正确的是( )
A . 凡是中心原子采取sp3杂化轨道成键的分子其几何构型都是正四面体
B . 1个原子轨道里最多只能容纳2个电子,但自旋方向相同
C . sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组新轨道
D . 凡AB3型的共价化合物,其中的中心原子A均采用sp3杂化轨道成键
【化学一选修3: 物质结构与性质】
-
(1) CH3COONH2 分子中各元素第一电离能大小顺序 ,该物质中碳原子杂化方式为
-
(2) 工业制备铁氧体也可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4) 等弱碱。
N2H4
NH3
熔点/℃
2
-77.8
沸点/℃
113.5
-33.5
比较上表中氨(NH3)、联氨(N2H4) 的熔、沸点,解释其高低的主要原因 ,
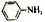 的离域π键表示为 ,与NH3 互为等电子体的阳离子有 。
的离域π键表示为 ,与NH3 互为等电子体的阳离子有 。 -
(3) 浅红色Cr [(H2O)3(NH3)3]Cl3中铬离子价电子排布式为 。
-
(4) SiC具有高硬度,高耐磨性,高耐腐蚀性和较高的高温强度特点,已成为一种重要的工程材料,其晶体具有六方ZnS 型结构。晶胞参数a=308pm,c=505pm,已知C原子的分数坐标(0,0,0)和( 2 3 , 1 3 , 1 2 );Si原子的分数坐标(0,0, 5 8 )和( 2 3 , 1 3 , 1 8 )
①按比例在下框中商出SiC 六方晶胞

②列式计算Si-C的键长 (保留整数部分)
将14Si的电子排布式写成1s22s22p63s23p  ,它违背了( )
,它违背了( )
 ,它违背了( )
,它违背了( )
A . 构造原理
B . 泡利原理
C . 洪特规则
D . 能量守恒原理
M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
-
(1) 单质M的晶体类型为,其中M原子的配位数为。
-
(2) 元素Y基态原子的核外电子排布式为,其同周期元素中,第一电离能最大的是(写元素符号)。
-
(3) M与Y形成的一种化合物的立方晶胞如图所示。
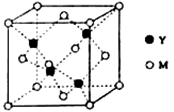
①该化合物的化学式为,已知晶胞参数a=0.542 nm,此晶体的密度为g·cm-3。(写出计算式,不要求计算结果。阿伏加德罗常数为NA)
②此化合物的氨水溶液遇到空气被氧化为深蓝色,其中阳离子的化学式为。
东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
-
(1) 镍元素基态原子的电子排布式为,3d能级上的未成对电子数为。
-
(2) 硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为,提供孤电子对的成键原子是。
-
(3) 单质铜及镍都是由键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1 958 kJ·mol–1、INi=1 753 kJ·mol–1 , ICu> INi的原因是。
砷化镓是继硅之后研究最深入、应用最广泛的半导体材料。回答下列问题:
-
(1) Ga基态原子核外电子排布式为,As基态原子核外有个成对电子。
-
(2) Ga、As、Se的第一电离能由打到小的顺序是Ga、As、Se的电负性由打到小的顺序是。
-
(3) 比较下列镓的卤化物的熔点和沸点,分析其变化规律及其原因:
镓的卤化物
GaCl3
GaBr3
GaI3
熔点/℃
77.75
122.3
211.5
沸点/℃
201.2
279
346
-
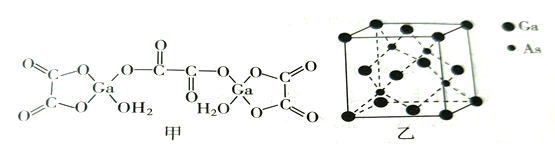
(4) 二水合草酸镓的结构式如图所示,其中镓原子的配位数是,草酸根离子中的原子杂化轨道类型是。
-
(5) 砷化镓的立方晶胞如图所示,晶胞参数为a=0.565nm,砷化镓晶体的密度为
g/cm3(设NA为阿伏加德罗常数的值,列出计算式即可)。
Cu(In1-xGaxSe2)(简称CIGS)可作多晶膜太阳能电池材料,具有非常好的发展前景。
回答下列问题:
-
(1) 已知铟的原子序数为49,基态铟原子的电子排布式为[Kr];Ga、In、Se,第一电离能从大到小顺序为。
-
(2) 硅与碳位于同主族,碳的化合物中往往有碳碳双键、碳碳三键,但是硅的化合物中只存在硅硅单键,其主要原因是。常温常压下,SiF4呈气态,而SiCl4呈液态,其主要原因是。
-
(3) 31Ga可以形成GaCl3·xNH3(x=3、4、5、6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2。则该溶液中溶质的化学式为。
-
(4) SeO32-的立体构型为;SeO2中硒原子采取杂化类型是。
-
(5) 常见的铜的硫化物有CuS和Cu2S两种。已知:晶胞中S2-的位置如图1所示,铜离子位于硫离子所构成的四面体中心,它们晶胞具有相同的侧视图如图2所示。已知CuS和Cu2S的晶胞参数分别为apm和bpm,阿伏加德罗常数的值为NA。
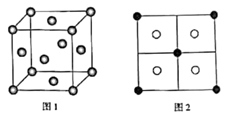
①CuS晶体中,相邻的两个铜离子间的距离为pm。
②Cu2S晶体中,S2-的配位数为。
③Cu2S晶体的密度为ρ=g·cm-3(列出计算式即可)。
下列叙述正确的是( )
A . 钠的焰色反应呈现黄色,是电子由激发态转化成基态时吸收能量产生的
B . 原子轨道和电子云都是用来形象地描述电子运动状态的
C . 各能层的s电子云轮廓图都是圆形,但圆的半径大小不同
D . 同一原子中,2p、3p、4p能级的轨道数依次增多
X 元素的原子最外层电子排布为(n+1)sn(n+1)pn+1 , 下列关于该元素及其化合物的叙述错误的是( )
A . X 的气态氢化物受热易分解
B . X 的最高价氧化物对应的水化物是一种强酸
C . X 的第一电离能比其左右相邻的两种元素的第一电离能都要大
D . X 是植物生长所需要的一种营养元素
具有下列电子排布式的基态原子中,半径最大的是( )
A . 1s22s22p63s23p3
B . 1s22s22p3
C . 1s22s22p4
D . 1s22s22p63s23p4
下列说法不正确的是( )
A . 原子核外电子排布,先排满K层再排L层、先排满M层再排N层
B . 同一原子中,1s、2s、3s电子的能量逐渐增大
C . 2p、3p、4p的轨道形状均为哑铃形
D . 各能层含有的原子轨道数为n2(n为能层序数)
下列分子中的中心原子发生 sp2 杂化的是( )
A . CH4
B . NH3
C . BF3
D . H2O
下列粒子的VSEPR模型为四面体且其空间结构为Ⅴ形的是。( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
许多元素及它们的化合物在科学研究和工业生产中具有多种用途。请回答下列有关问题:
-
(1) 现代化学中,常利用上的特征谱线来鉴定元素。
-
(2) 某同学画出的基态碳原子的核外电子排布图为
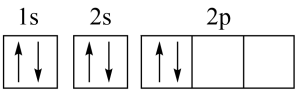 , 该电子排布图背了。CH
, 该电子排布图背了。CH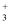 、-CH3、CH
、-CH3、CH 都是重要的有机反应中间体。CH
都是重要的有机反应中间体。CH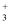 、CH
、CH 的空间构型分别为、。
的空间构型分别为、。
-
(3) 咪唑的结构为
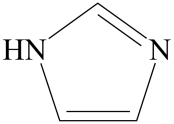 。分子中的大π键可用符号π
。分子中的大π键可用符号π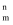 表示。其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示。其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π )。咪唑分子中的大π键可表示为,咪唑比环戊烯C5H8熔点高的主要原因是。
)。咪唑分子中的大π键可表示为,咪唑比环戊烯C5H8熔点高的主要原因是。
-
(4)
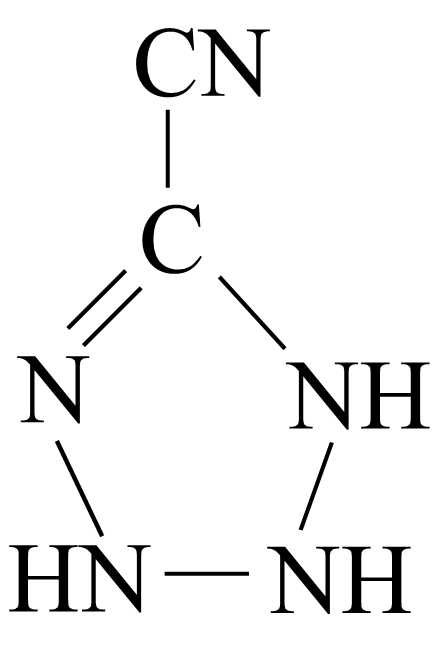 中孤电子对与π键比值为,碳原子的杂化方式为。
中孤电子对与π键比值为,碳原子的杂化方式为。
-
(5) 铁氮化合物是磁性材料研究中的热点课题之一,因其具有高饱和磁化强度、低矫顽力。有望获得较高的微波磁导率,具有极大的市场潜力。其四子格结构如图所示,已知晶体密度为ρg·cm-3 , 阿伏加德罗常数为NA。
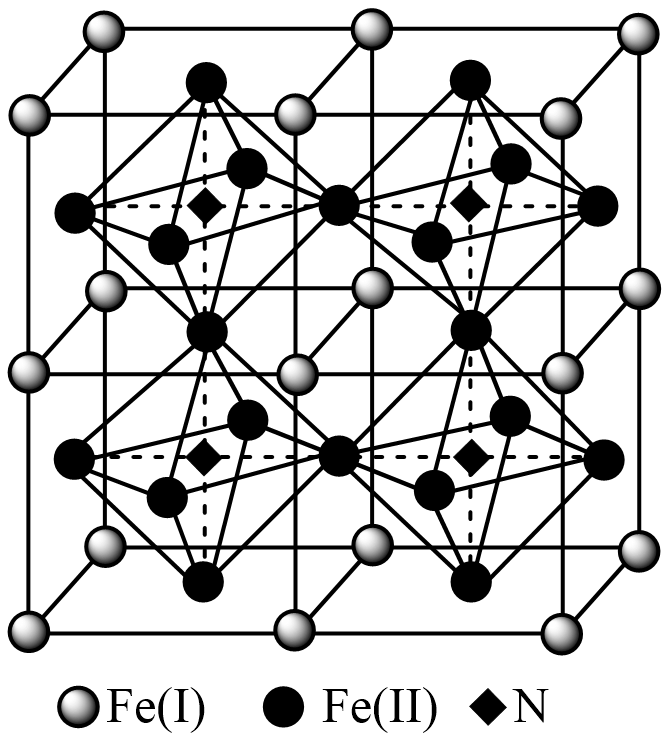
①写出氮化铁中铁的堆积方式为。
②该化合物的化学式为。
③计算出Fe(II)围成的八面体的体积为cm3。
氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi),在性质上表现出从典型的非金属元素到典型的金属元素的一个完整的过渡。
-
(1) 下列氮原子的能量最低的是____。A .
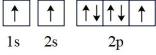 B .
B . 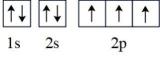 C .
C . 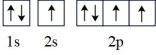 D .
D . 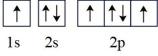
-
(2) ①氮族元素简单氢化物的键角NH3>PH3>AsH3 , 其原因是。
②南开大学某课题组成功合成了无机二茂铁类似物[Fe(η4- P4)2]2-。环状
 是芳香性π配体,P的杂化方式是 ,
是芳香性π配体,P的杂化方式是 , 中的大π键应表示为(分子中的大π键可用符号
中的大π键应表示为(分子中的大π键可用符号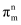 表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)
表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)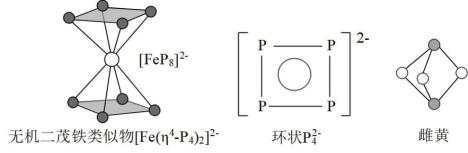
-
(3) 雌黄的分子式为As2S3 , 1个As2S3分子中孤电子对数目为。
-
(4) 天津理工大学科研团队制备出一种智能离子交换剂,由平行堆积的一维链阴离子(部分结构如下图)和K+阳离子组成,含有n个最简单元的阴离子可表示为。
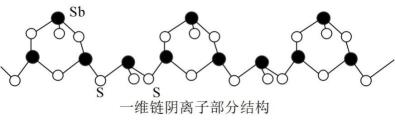
-
(5) ①基态铋原子的价电子排布式为。
②铋的一种氧化物的立方晶胞结构如图所示,已知最近的两个铋离子之间的距离为a pm,阿伏加德罗常数为NA , 则该晶体的密度为g·cm-3(列出计算式即可)。
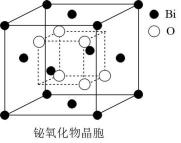
最近更新
- 某种植物的两个开白花的品系AAbb和aaBB杂交,F1自交得F2中有紫花和白花,且比例为9∶7。则F1的表现型为(
- 南、北半球的分界线是( ) A.回归线 B.赤道 C.极圈 D
- 下列物质中不含共价键的是 A. 冰 B.碳化硅 C.干冰
- (本小题满分14分) 平面内与两定点,连续的斜率之积等于非零常数的点的轨迹,加上、两点所成的曲线可以是圆、椭圆成双曲线.
- — Hi! Grace, why notgo fishing next vacation? —____________
- 读下面四个省区的轮廓图,完成25~28题。25、图中所示我国纬度最高的省是( )A.① B.②
- 这是一场特殊的战争,它存在于两个不同社会制度之间,既威胁了世界和平又维持了相对的和平。这场战争是: ( )A.第
- 修建城市轻轨铁路,除了能改善城市交通,还可以 A.改善城市的景观 B.提高城市居民的经济收入 C.改善城市的环境质量
- 下图为体液免疫示意图,下列叙述正确的是()A.①过程体现了细胞膜的流动性 B.⑤过程主要发生在细胞质基质中 C.浆细胞能
- 下列关于生物大分子的叙述中,不正确的是A.蛋白质是以氨基酸为基本单位构成的生物大分子 B.核酸是储存遗传信息、控制蛋白质
- 用化学用语表示: (1)2个汞原子; (2)4个水分子; (3)氢氧根离子; (4)氧化镁中镁元素的化合价 .
- 下列记录了某系统受迫振动的振幅随驱动力变化的关系,若该振动系统的固有频率为f固,则( ) 驱动频率/Hz30405
- 1. 研究金属丝电阻大小与材料关系的实验中,正确的做法是 ( )A.选用长
- In the end I lost my ______ and shouted at her. A. char
- (湖北省黄冈市黄州区一中2012届高三月考)粒子回旋加速器的工作原理如图所示,置于真空中的D型金属盒的半径为R,两金属盒
- 太阳与地球的距离为1.5×1011m,太阳光以平行光束入射到地面.地球表面2/3的面积被水面所覆盖,太阳在一年中辐射到地
- 下列说法中错误的是( ) A.在元素周期表金属与非金属分界线附近能找到制半导
- The building project________next year is not easy________in
- 、在△ABC中,∠C=90°,a、b分别是∠A、∠B所对的两条直角边,c是斜边,则有A. sinA= B. c
- 下列离子方程式正确的是( ) A.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+ H2↑+ Cl2↑ B.N



