原子核外电子的运动状态 知识点题库
反应①:2NH3+3F2NF3+3NH4F
利用“化学蒸气转移法”制备TaS2晶体;
反应②:TaI4(g)+S2(g)⇌TaS2(s)+2I2(g)+Q kJ,Q>0
-
(1) 反应①中:非金属性最强的元素原子核外有 种不同运动状态的电子;该反应中的某元素的单质可作粮食保护气,则该元素最外层的电子有 种自旋方向.
-
(2) 反应①中:物质所属的晶体类型有 ;并写出所有原子符合8电子稳定结构的化合物的电子式
-
(3) 反应②中:平衡常数表达式K= ,若反应达到平衡后,保持其他条件不变,降低温度,重新达到平衡时 .
a.平衡常数K增大 b.S2的浓度减小 c.I2的质量减小 d.V(TaI4)逆增大
-
(4) 反应②在一定温度下进行,若反应容器的容积为2L,3min后达到平衡,测得蒸气的质量减少了2.45g,则I2的平均反应速率为
-
(5) 某同学对反应②又进行研究,他查阅资料,发现硫单质有多种同素异形体,可表示Sx , 且在一定条件下可以相互转化,他认为仅增大压强对平衡是有影响的,则TaI4的平衡转化率会 (填增大或减小),其原因是
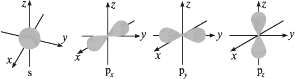
-
(1) s电子云轮廓图呈 形,每个s能级有个原子轨道;p电子云轮廓图呈状,每个p能级有个原子轨道,其能量关系为(填“相同”或“不相同”)。
-
(2) 元素X的原子最外层的电子排布式为nsnnpn+1,原子中能量最高的是电子;元素X的名称是,它的氢化物的电子式是。
-
(3) 若元素Y的原子最外层的电子排布式为nsn-1npn+1,那么Y的元素符号应为,原子的电子排布图为。
-
(1) 镓(Ga)的原子结构示意图为
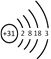 ,镓元素在周期表中的位置是。
,镓元素在周期表中的位置是。
-
(2) 镓能与沸水剧烈反应生成氢气和氢氧化镓,该反应的化学方程式是。
-
(3) 氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。
资料:镓的熔点较低(29.8℃),沸点很高(2403℃)。
①传统的氮化镓(GaN)制备方法是采用GaCl3与NH3在一定条件下反应,该反应的化学方程式是。
②当代工业上固态氮化镓(GaN)的制备方法是利用镓与NH3在1000℃高温下合成,同时生成氢气,每生成1mol H2时放出10.27 kJ热量。该可逆反应的热化学方程式是 。
③在密闭容器中,充入一定量的Ga与NH3发生上述反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。
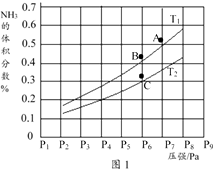
图中A点和C点化学平衡常数的关系是:KA KC (填“>”“=”或“<”),理由是。
-
(4) 电解法可以提纯粗镓,具体原理如图2所示:
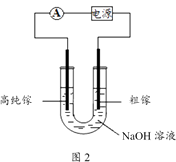
①粗镓与电源极相连。(填“正”或“负”)
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2- , GaO2-在阴极放电的电极反应式是
。
-
(1) 锰与铼处于同一族,锰原子价层电子的轨道表示式(价层电子排布图)为,它处于周期表的区。
-
(2) 与铼伴生的铜能形成多种配合物。如:醋酸二氨合铜(I)[Cu(NH3)2]Ac可用于吸收合成氨中对催化剂有害的CO气体:[Cu(NH3)2Ac+CO+NH3
 [Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
[Cu(NH3)3]Ac·CO。(Ac表示醋酸根)①与铜离子形成配合物的分子或离子应具备的结构特征是。
②配位体NH3中N原子的杂化类型为,1mol 配离子[Cu(NH3)2]+中含有σ键的数目为。
③写出与CO 互为等电子体的一种离子的化学式。
-
(3) 金属铼的熔点高于锰,试从原子结构的角度加以解释。
-
(4) 三氧化铼为立方晶胞,晶胞参数为3.74A(1A=10-10m),铼原子占据顶点,氧原子占据所有棱心。则铼原子的配位数为,三氧化铼的密度为g/cm3。(用NA表示阿伏加德罗常数的值,写计算式即可)
-
(1) 最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子的排布图为。
-
(2) 铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述符合题意的有_____(填字母)。A . 都属于p区主族元素 B . 电负性都比镁大 C . 第一电离能都比镁大 D . 氯化物的水溶液pH均小于7
-
(3) 铍、铝晶体都是由金属原子密置层在三维空间堆积而成(最密堆积)。铍的熔点(1551K)比铝的熔点(930K)高,原因是。
-
(4) 氯化铍在气态时存在BeCl2分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。
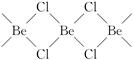
①a属于(填“极性”或“非极性”)分子。
②二聚分子(BeCl2)2中Be原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为(标出配位键)。
-
(5) Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所:
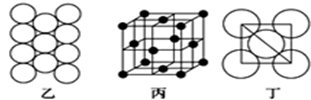
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为个;Al晶体的密度为(用字母表示)。
-
(1) 卤族元素位于元素周期表区,其中电负性最大的是(填元素符号)。
-
(2) 基态氟原子核外有种运动状态不同的电子,其中含有单电子的轨道形状为。
-
(3) 溴元素对应的含氧酸 HBrO4酸性比 HBrO3酸性(填“强”或“弱”),原因是。
-
(4) 化合物 I3 AsF6为离子化合物,其中阳离子(I
 )中心原子的杂化方式为。该晶体中不含有的化学键类型为(填选项字母)。
)中心原子的杂化方式为。该晶体中不含有的化学键类型为(填选项字母)。 a.配位键 b.金属键 c.极性键 d.非极性键
-
(5) 由钾、氧、碘三种元素构成的晶体晶胞结构如图1所示。则该晶体的化学式为,晶胞中位置与 K+紧邻的 O 的个数为。
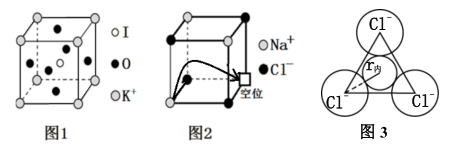
-
(6) 有“点缺陷”的 NaCl 晶体可导电,其结构如图 2 所示。有人认为:高温下有“点缺陷”的 NaCl 晶体能导电,是因为 Na+经过一个由 3 个 Cl-组成的最小三角形窗孔(如图 3 所示),迁移到另一空位而造成的。已知立方体边长 a=282pm,粒子半径 r(Na+)=115pm,r(Cl-)=167pm,计算内切圆半径 r内的值并判断该观点是否正确。(已知:
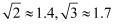 )
)
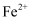 时首先失去3d轨道电子
B .
时首先失去3d轨道电子
B .  的空间构型为平面正三角形
C . 通过化学变化可以实现
的空间构型为平面正三角形
C . 通过化学变化可以实现 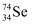 与
与 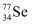 的相互转化
D . 基态F原子的核外电子有9种空间运动状态
的相互转化
D . 基态F原子的核外电子有9种空间运动状态
-
(1) 氮原子最外层电子排布式为;氮离子(N3- )核外有种运动状态不同的电子;N4分子的空间结构为
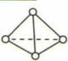 , 它是一种(填“极性"或“非极性")分子。
, 它是一种(填“极性"或“非极性")分子。
-
(2) PH3分子与NH3分子的空间结构关系: (填“相同”或“不相同”),P-H键 (填“有”或“无")极性,PH,分子(填“有"或“无" )极性。
 (简称LFP)电池的使用大幅降低了高端全电动汽车的成本。下列说法不正确的是( )
(简称LFP)电池的使用大幅降低了高端全电动汽车的成本。下列说法不正确的是( )
 的价层电子排布式为
的价层电子排布式为 D . 基态O原子核外电子空间运动状态有5种
D . 基态O原子核外电子空间运动状态有5种
 Si3N4(s) +12HCl(g)。请回答:
Si3N4(s) +12HCl(g)。请回答:
-
(1) 基态N原子的价电子轨道式为。
-
(2) Si原子与H原子结合时,Si呈正化合价,则电负性:SiH(选填“<”或“>”)。
-
(3) 元素第一电离能:SiN(选填“<”或“>”)。
-
(4) 基态Cl原子的核外电子运动状态有种。
-
(5) Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是。
-
(6) 锗(Ge与Si是同一主族的元素。Ge的最高价氯化物分子式是。Ge元素可能的性质或应用有(填序号)。
A.是一种活泼的金属元素 B.其电负性大于硫
C.其单质可作为半导体材料 D.其气态氢化物的稳定性低于硅的气态氢化物
-
(1) 三甲基卤硅烷【(CH3)3SiX,X为Cl、Br、I】是重要的化工原料。
①氯元素基态原子的价电子排布式为;按照核外电子排布对元素周期表分区,溴元素位于区;基态硅原子中有种运动状态不同的电子。
②Br、I的第一电离能的大小关系:I1(Br)I1(I)(填“大于”“小于”或“等于”)。
③常温下,(CH3)3SiI中Si—I键比(CH3)3SiCl中Si—Cl键易断裂的原因是。
-
(2) (CH3)3SiCl可作为下列有机合成反应的催化剂。
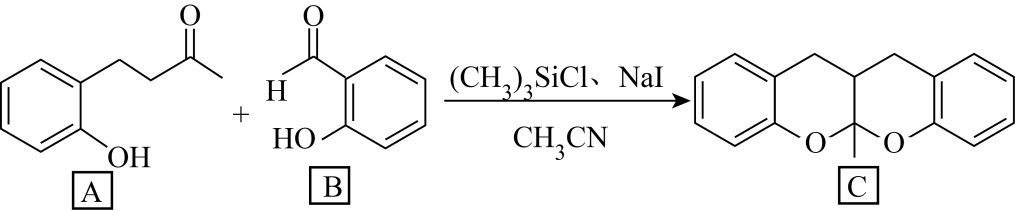
①1个有机物A分子中采取sp2杂化的碳原子有个。
②有机物B的沸点低于对羟基苯甲醛(
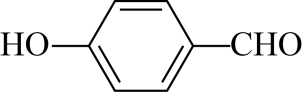 )的沸点,其原因是。
)的沸点,其原因是。③CH3CN中σ键与π键的个数比为。
-
(3) 一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(a、b方向的夹角为120°,c方向垂直于a、b方向,棱长a+b≠c),如图甲所示;晶胞中碳原子的投影位置如图乙所示。
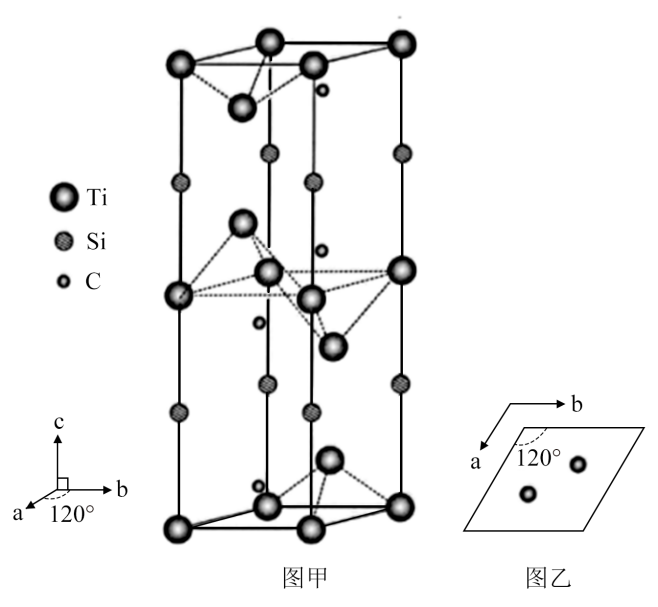
①该钛硅碳新型材料的化学式为。
②已知该新型材料的密度为4.51g•cm-3 , 且a、b的长度均为307pm,阿伏加德罗常数的值用NA表示,则c的长度为pm (列出计算式)。
回答下列问题:
-
(1) 基态Co原子核外电子排布式为[Ar],有 个 运动状态不同的电子。
-
(2) 原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 号表示,与之相反的用-
号表示,与之相反的用-  表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为。
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为。
-
(3) 科学家证实,BeCl2是共价化合物,请设计一个简 单实验证明该结论:;Be的杂化轨道类型为。
-
(4) 在N
 、 NH3、N2H4、NH
、 NH3、N2H4、NH  、N2H
、N2H  五种微粒中,同种微粒间能形成氢键的有;不能作为配位体的有;空间构型为直线形的是。
五种微粒中,同种微粒间能形成氢键的有;不能作为配位体的有;空间构型为直线形的是。
-
(5) 氮原子的第一电离能(填“大于”“小于”或“等 于”)磷原子的第一电离能。
-
(6) 分别用
 、
、  表示H2PO
表示H2PO  和K+ , KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+ , KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO  、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA , 晶体的密度为 g·cm-3(写出表达式即可)。
、K+在晶胞xz面、yz面上的位置。若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为NA , 晶体的密度为 g·cm-3(写出表达式即可)。 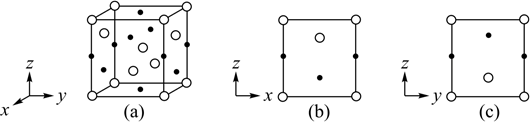
- ......
- 1898年前后,一个英国外交官来到中国上海,此时他不可能了解到的情况是 A.英国商人在上海缴纳的税款,中国须同英国协商B
- 通常把萝卜腌成咸菜需要几天,而把萝卜炒成熟菜使之具有相同的咸味只需几分钟,造成这种差别的主要原因是( ) A.盐的
- 不能用2H + + CO32- == CO2 ↑+H2O表示的反应是 A.醋酸溶液与碳酸钠溶液反应 B.稀
- 原始大气的成分中不包括下列哪种物质( ) A.氧气 B.二氧化碳 C.氢
- 如图是A、B两种固体物质的溶解度曲线,请回答下列问题: (1)t1℃时,A物质的溶解度(填“>”、“=”或“<”)B物质
- 材料是人类文明进步的标志.图12-21中不同时代物品的材料在加工、制取过程中只发生物理变化的是 ( )A.石器
- 某商场按月订购一种家用电暖气,每销售一台获利润200元,未销售的产品返回厂家,每台亏损50元,根据往年的经验,每天的需求
- 人胰岛细胞能产生胰岛素,但不能产生血红蛋白,据此推测胰岛素细胞中( ) A.只有胰岛素基因
- 已知集合等于 A.{x|1<x<2 B.{x|1<x<2,或x>3 C.{x|0
- 利用农田蜘蛛可防治农田中的害虫,下列说法错误的是( ) A.可消灭所有害虫 B.减少施用农
- 物体静止在光滑的水平桌面上.从某一时刻起用水平恒力F推物体,则在该力刚开始作用的瞬间 (
- 下列句子中加点词语使用有误的一项是( ) A.今年中秋月饼“遇冷”的背后是党激浊扬清的决心。 B.“艾青”回到自己
- X和Y两种元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径,Z和X两种元素的原子核外电子层数相
- 有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述正确
- 某同学尝试在适宜的条件下制作果酒和果醋,在消毒后的锥形瓶中装入新鲜的葡萄汁后封闭通气口,进行自然发酵,发酵初期将温度控制
- 一次函数y1=x+1与y2=-2x+4图像交点的横坐标是( ) A.4
- 如图,在△ABC中,∠ACB=90º,∠A=15º,AB=8,则AC·BC的值为【 】
- He hurried to the stadium without supper, ________the footba
- -It's time for class. Please be_______. -Sorry, I won't t



