浓硫酸的性质 知识点题库
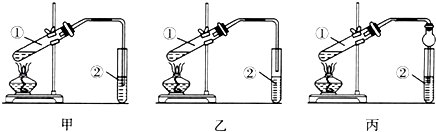
下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯.他们分别设计了如图所示的三套实验装置:
-
(1) 请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,较合理的是(填“甲”或“乙”).丙同学将甲装置进行了改进,将其中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是.
-
(2) 【实验步骤】
①按丙同学选择的装置组装仪器,在试管中先加入3 mL乙醇,并在摇动下缓缓加入2 mL浓硫酸充分摇匀,冷却后再加入2 mL冰醋酸;
②将试管固定在铁架台上;
③在试管②中加入适量的饱和Na2CO3溶液;
④用酒精灯对试管①加热;
⑤当观察到试管②中有明显现象时停止实验.
【问题讨论】
a.步骤①安装好实验装置,加入样品前还应检查;
b.写出试管①发生反应的化学方程式(注明反应条件);
c.试管②中饱和Na2CO3溶液的作用是;(填“能”或“不能”)换成NaOH溶液,原因为;
d.从试管②中分离出乙酸乙酯的实验操作是;
e.若60g乙酸与足量的乙醇反应能生成53 g乙酸乙酯,计算该反应中乙酸的转化率(要求写出计算过程).
-
(1) Al(OH)3 与氢氧化钠溶液反应:
-
(2) 氢氧化亚铁被氧化成氢氧化铁:
-
(3) 二氧化硅与氢氟酸反应:
-
(4) 氨气的实验室制取法:
-
(5) 浓硫酸与木炭反应:
-
(6) 稀硝酸与铜反应:.
-
(1) 铁与水蒸气在高温下:
-
(2) 苛性钠腐蚀玻璃:
-
(3) 制取漂白粉:
-
(4) 稀硝酸与铜片:
-
(5) 氨的催化氧化:
-
(6) 铜片在浓硫酸中加热:.
|
实验操作 |
答案 |
实验现象 |
|
⑴将浓硫酸滴在小木条上 |
|
A.产生白烟 |
|
⑵将分别蘸有浓氨水和浓盐酸的玻璃棒靠近 |
|
B.产生蓝色物质 |
|
⑶在盛有KI淀粉溶液的试管中滴加氯水 |
|
C.溶液呈血红色 |
|
⑷在盛有FeCl3溶液的试管中滴入2滴KSCN溶液 |
|
D.变黑色 |
| 选项 | 操作和现象 | 结论 |
| A | 向某溶液中加入稀盐酸,有刺激性气味的气体产生,将气体通入澄清石灰水,石灰水变浑浊 | 该溶液中一定含有SO |
| B | 二氧化硫通入酸性高锰酸钾溶液,紫红色褪去 | SO2有漂白性 |
| C | 将铝片分别放入足量浓硝酸,稀硝酸溶液中,浓硝酸无明显变化,稀硝酸有大量气泡产生 | 氧化性:稀硝酸>浓硝酸 |
| D | 蔗糖固体加入浓硫酸,出现“黑面包现象” | 浓硫酸具有脱水性和强氧化性 |
| 选项 | 物质的性质 | 物质的用途 |
| A | 液氨汽化吸收大量热 | 液氨作制冷剂 |
| B | 铁不与浓硫酸反应 | 用铁罐储运浓硫酸 |
| C | 二氧化硫有还原性 | 葡萄酒中添加二氧化硫抗氧化 |
| D | 二氧化硅有光学特性 | 二氧化硅制光导纤维 |
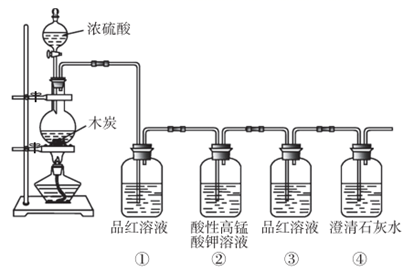
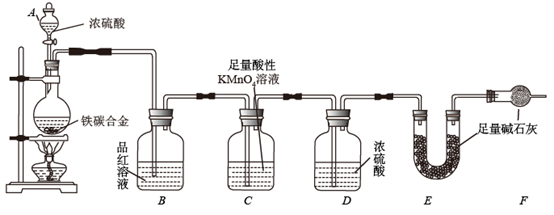
-
(1) 仪器A的名称是 。
-
(2) 装置B中品红溶液的作用是;装置C中酸性高锰酸钾溶液的作用是。
-
(3) 取生铁样品15g,与足量浓硫酸完全反应后无固体剩余。假设产生的
 全部进入装置E中,称得装置E增重2.2g,则该生铁样品中的碳元素含量为 ;甲同学认为装置F多余,若撤去装置F,则测得样品中的碳元素含量 (填“偏高”、“偏低”或“无影响”)。
全部进入装置E中,称得装置E增重2.2g,则该生铁样品中的碳元素含量为 ;甲同学认为装置F多余,若撤去装置F,则测得样品中的碳元素含量 (填“偏高”、“偏低”或“无影响”)。
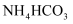 受热易分解,可用作化肥
B . 稀硫酸具有酸性,可用于除去铁锈
C .
受热易分解,可用作化肥
B . 稀硫酸具有酸性,可用于除去铁锈
C .  具有漂白性,可用于纸浆漂白
D . 明矾溶于水形成胶体,可用于自来水厂净水
具有漂白性,可用于纸浆漂白
D . 明矾溶于水形成胶体,可用于自来水厂净水
已知:①SO2难溶于饱和亚硫酸氢钠溶液。②SO2能与酸性高锰酸钾溶液发生氧化还原反应。请回答下列问题:
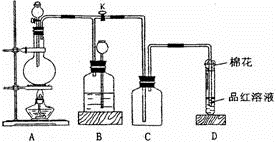
-
(1) 装置A中发生的化学反应方程式为;此反应表明浓硫酸具有(填字母)。
a. 酸性 b. 脱水性 c. 强氧化性 d. 吸水性
-
(2) 装置D中试管口放置的棉花中浸入溶液,其作用是。
-
(3) 装置B的作用是贮存多余的气体,B中应放置的液体是(填字母)。
a. 水 b. 饱和NaHSO3溶液 c. 酸性KMnO4溶液 d. NaOH溶液
-
(4) 实验中,取一定质量的铜片和一定体积18.4 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是(填字母)。
a. 银粉 b. 铁粉 c. BaCl2溶液 d. NaHCO3溶液
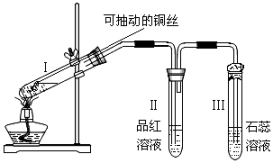
-
(1) 试管Ⅰ中发生反应的化学方程式为。实验中采用可抽动的铜丝,与直接放铜片相比,优点是。
-
(2) 若将试管Ⅱ换成KMnO4溶液,则反应的离子方程式为。
-
(3) 试管Ⅲ的管口用浸有碱(NaOH溶液)的棉团塞住,其作用是; 发生反应的化学方程式为。
-
(4) ①实验开始时时,取ag铜丝和VmL 18mol/L浓硫酸放在试管中共热。反应进行一段时间后,铜丝还有剩余,且能深入溶液内,但发现继续加热,铜丝不再溶解。该小组同学根据所学知识认为还有一定的硫酸剩余,下列药品中能用来证明反应结束后的试管中确有硫酸剩余的是(填序号字母)。
a.铜粉 b.BaCl2溶液 c.硝酸钾溶液 d.Na2CO3溶液
②该小组同学通过实验测得剩余铜丝质量为bg(假设反应前后溶液的体积不变),则剩余硫酸的物质的量浓度为mol/L。
- 假说——演绎法是现代科学研究中常用的方法,包括“提出问题、作出假设、演绎推理、检验推理、得出结论”五个基本环节。利用该方
- 2010年3月,江苏某市有300多名领导干部在网上“晒”出了自己的《述职述廉报告》全文,网民可以跟贴对每一位干部作出评议
- 已知函数f(x)=Asin2(ωx+φ)(A>0,ω>0,0<φ<),且y=f(x)的最大值为2,其图象相邻两对称轴间的
- 如图所示,是放置在竖直平面内的游戏滑轨的模拟装置,滑轨由四部分粗细均匀的金属杆组成。AB为水平直轨,CPA与BFD圆形轨
- 如图,圆O从直线上的点(圆心与点重合)出发,沿直线以厘米/秒的速度向右运动(圆心始终在直线上).已知线段厘米,圆O、圆B
- 一、 阅读下面的文章,完成1~4题。 拜谒三苏园 王剑冰 ①天要黑了,我才赶来,我顺着一条弯弯曲曲的小道,我不知道是不是
- 一个几何体的三视图形状都相同、大小均相等,那么这个几何体不可以是(). A.球 B.三棱锥 C.正方体 D.圆柱
- 读“德国鲁尔区和我国辽中南工业基地图”,比较两地的区位特点,完成1~4题。1.两地发展钢铁工业相同的区位优势是() ①接
- A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,其余均为常见化合物,J是一种黑色固体
- 下图为下丘脑某神经细胞的部分膜结构示意图,下列叙述正确的是A.若此图为突触后膜局部结构,则兴奋经过此处时的信号转换是:电
- —Whichflight ? —I want to catch the13:00. A.you are to ca
- 水稻的高秆(D)对矮秆(d)是显性,抗锈病(R)对不抗锈病(r)是显性,这两对基因自由组合。甲水稻(DdRr)与乙水稻杂
- .已知双曲线x2-=1的焦点为F1、F2,点M在双曲线上且=0,则点M到x轴的距离为 A. B.
- 光合作用和有氧呼吸过程中都有[H]的生成与利用,下列分析中合理的是( ) A
- 6.Manuel ____(fly)to London next Monday. 7. The funny storym
- From their ____ on thetop of the TV Tower, visitors can ha
- 电解100 mL含c(H+)=0.30mol/L的下列溶液。当电路中通过0.04mol电子时,理论上析出金属质量最大的是
- Listen! Can you see a boy _______ in the next room ?
- 已知函数,则的值为 .
- 已知函数f(x)=sin的图像上,相邻的一个最大值点与一个最小值点恰好都在圆x2+y2=R2上,则f(x)的最小正周期为




