化学平衡的调控 知识点题库
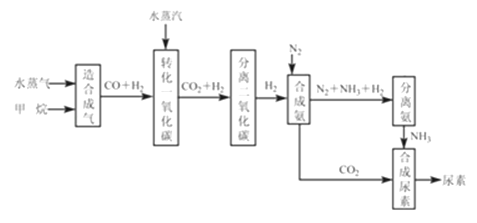
填写下列空白:
(1)已知0.5mol甲烷和0.5mol水蒸气在t℃,p k Pa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量.该反应的热化学方程式是:
(2)上述流程中,工业上分离H2、CO2合理的方法是
A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸
B.混合气加压冷却,使CO2液化
C.混合气用氨水洗涤
D.混合气先通入到石灰浆,然后高温煅烧固体,
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行 ,目的是 ;在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法:
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,阐述图中的两处可以合理利用资源情况
工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2(g)⇌2SO3(g)△H=﹣196.6kJ•mol﹣1
(1)生产中为提高反应速率和SO2的转化率,下列措施可行的是
A.向装置中充入N2 B.向装置中充入过量的SO2C.向装置中充入O2 D.升高温度
(2)若在一定温度下,向一个容积可变的恒压容器中,通入3mol SO2 和2mol O2及固体催化剂,发生上述反应,平衡时容器内气体体积为起始时的90%.保持同一反应温度,在相同容器中,将起始物质的量改为 5mol SO2(g)、3.5mol O2(g)、1mol SO3 (g),下列说法正确的是
A.第一次平衡时反应放出的热量为294.9kJ
B.两次平衡SO2的转化率相等
C.两次平衡时的O2体积分数相等
D.第二次平衡时SO3的体积分数等于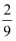
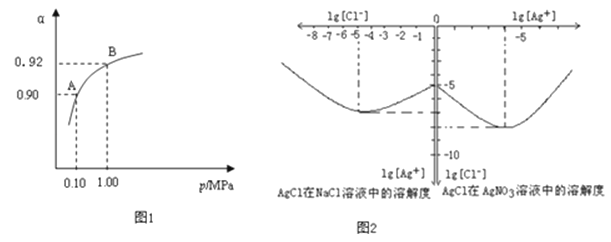
(3)生产中在550℃时,将2.0mol SO2和1.0mol O2置于5L密闭容器中,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图1所示.反应达平衡后,体系总压强为0.10M Pa.试计算反应2SO3⇌2SO2+O2 在550℃时的平衡常数K= .A、B表示不同压强下的平衡转化率,通常工业生产中采用常压的原因是: ,并比较不同压强下的平衡常数:K(0.10MPa) K(1.0MPa)(填“<”或“>”或“=”).
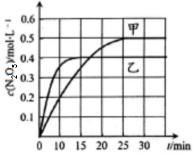
(4)沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变.已知AgCl+Cl﹣=[AgCl2]﹣ , 如图2是某温度下AgCl在NaCl溶液中的溶解情况.由以上信息可知:
①由图知该温度下AgCl的溶度积常数为
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:
 =,实际生产要将r值维持在1.7~2.2之间,原因是.
=,实际生产要将r值维持在1.7~2.2之间,原因是. 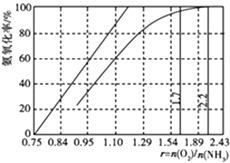
 H++ OH-ΔH > 0 ,下列叙述正确的是( )
H++ OH-ΔH > 0 ,下列叙述正确的是( )
 NO(g)+CO2(g),该反应过程及能量变化如图所示,下列说法正确的是( )
NO(g)+CO2(g),该反应过程及能量变化如图所示,下列说法正确的是( ) 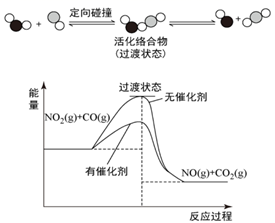
-
(1) I.在25 ℃、101 kPa下:①2Na(s)+
 O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1;②2Na(s)+O2(g)=Na2O2(s) ΔH2=-511 kJ·mol-1;25℃、101 kPa下,Na2O2(s)与Na(s)反应生成Na2O(s)的热化学方程式为。
O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1;②2Na(s)+O2(g)=Na2O2(s) ΔH2=-511 kJ·mol-1;25℃、101 kPa下,Na2O2(s)与Na(s)反应生成Na2O(s)的热化学方程式为。
-
(2) II.在2L密闭容器内,800℃时反应:2NO(g)+O2(g)⇌2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s)
0
1
2
3
4
5
n(NO)(mol)
0.020
0.011
0.008
0.007
0.007
0.007
写出该反应的平衡常数表达式:K=。
-
(3) 如图中表示NO2的变化的曲线是。用O2表示从0~2s内该反应的平均速率v=
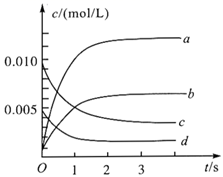
-
(4) 能说明该反应已达到平衡状态的是。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
-
(5) 某同学查阅资料得知,该反应K300℃>K350℃;25℃时,生成1molNO2 , 热量变化为56.4kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为。
-
(6) 为使该反应的反应速率增大,且平衡向正反应方向移动的是。
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
 CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表: | t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
-
(1) 该反应的化学平衡常数表达式K=。
-
(2) 该反应为反应(填“吸热”或“放热”)。
-
(3) 830℃,在1L的固定容器的密闭容器中放入1 mol CO和5 mol H2O,反应达平衡后,其化学平衡常数K1.0(填“大于”、“小于”或“等于”)
-
(4) 830℃,容器中的反应达到平衡。在其他条件不变的情况下,扩大容器的体积,平衡移动。(填“向正方向”、“向逆方向”或“不”)
-
(5) 若1200℃时,在某时刻该容器中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1 , 则此时上述反应的平衡移动方向为(选填“正反应方向”、“逆反应方向”、“不移动”)。
 增大
D . 加入0.1mol•L-1CH3COONa溶液使pH=7,则c(CH3COO-)=c(Na+)
增大
D . 加入0.1mol•L-1CH3COONa溶液使pH=7,则c(CH3COO-)=c(Na+)
Ⅰ.CO(g)+2H2(g)  CH3OH(g)△H1=-90.8kJ·mol-1
CH3OH(g)△H1=-90.8kJ·mol-1
Ⅱ.2CH3OH(g)  CH3OCH3(g)+H2O(g)△H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g)△H2=-23.5kJ·mol-1
-
(1) 2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g)△H3=kJ·mol-1。
CH3OCH3(g)+H2O(g)△H3=kJ·mol-1。
-
(2) 若在恒温恒容的密闭容器内只发生反应Ⅱ,可判断该反应已达到平衡状态的是 (填标号)。A . 气体的平均摩尔质量保持不变 B . CH3OCH3浓度与H2O浓度相等 C . CH3OCH3的体积分数保持不变 D . 2v(CH3OCH3)=v(CH3OH)
-
(3) T℃时,将2molCO和2molH2充入一恒容密闭容器内发生反应:2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g)。起始时,容器内压强为2×106Pa,平衡时总压减少了25%,H2的转化率为,该反应的平衡常数Kp=Pa-4(保留2位有效数字)。达到平衡后﹐欲增加CO的平衡转化率,可采取的措施有(填标号)。
CH3OCH3(g)+H2O(g)。起始时,容器内压强为2×106Pa,平衡时总压减少了25%,H2的转化率为,该反应的平衡常数Kp=Pa-4(保留2位有效数字)。达到平衡后﹐欲增加CO的平衡转化率,可采取的措施有(填标号)。 A.再通入一定量的CO B.降低温度
C.及时移走CH3OCH3(g) D.通入氮气
-
(4) 当压强为p时,在一密闭容器中充入一定量的CO和H2 , 测得不同温度下CO的平衡转化率及催化剂的催化效率如图所示。
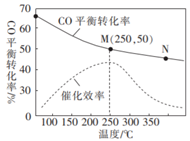
达到平衡后,增大压强,反应Ⅰ的平衡(填“向正反应方向”、“向逆反应方向”或“不”,下同)移动,反应Ⅱ的平衡移动,故工业上选择(填“高压”或“低压”)制备二甲醚。工业生产中不选择350℃的原因是。
 NO(g)+O2(g)。测得:v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。向容积均为2L的甲、乙两个密闭容器中充入一定量的NO和O3 , 测得NO的体积分数随时间的变化如图所示。下列说法正确的是( )
NO(g)+O2(g)。测得:v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。向容积均为2L的甲、乙两个密闭容器中充入一定量的NO和O3 , 测得NO的体积分数随时间的变化如图所示。下列说法正确的是( ) 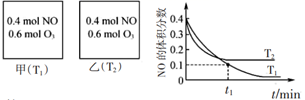
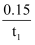 mol·L-1·min-1
C . T1时,NO(g)+O3(g)
mol·L-1·min-1
C . T1时,NO(g)+O3(g)  NO2(g)+O2(g)的k正<3k逆
D . T2时,向2 L密闭容器中充入0.6 mol NO、0.4 mol O3 , 到达平衡时c(NO2)小于乙容器中平衡时c(NO2)
NO2(g)+O2(g)的k正<3k逆
D . T2时,向2 L密闭容器中充入0.6 mol NO、0.4 mol O3 , 到达平衡时c(NO2)小于乙容器中平衡时c(NO2)
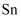 、
、 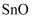 )联合生产氯化亚锡和硫酸亚锡晶体,其工艺流程如下:
)联合生产氯化亚锡和硫酸亚锡晶体,其工艺流程如下: 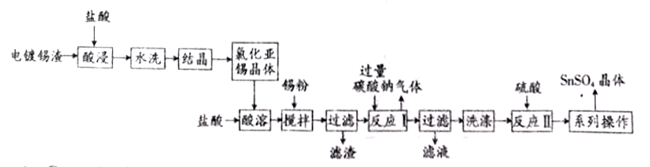
已知:① 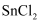 易水解生成碱式氯化亚锡
易水解生成碱式氯化亚锡 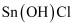 ;②在水溶液中,
;②在水溶液中,  易被氧化为
易被氧化为  。
。
请回答下列问题:
-
(1) 锡在周期表中的位置为。
-
(2) 已知反应I得到的沉淀是
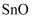 ,产生气体的结构式为,反应的化学方程式为。
,产生气体的结构式为,反应的化学方程式为。
-
(3) 图中滤液的主要成分为、(写化学式)。
-
(4) 酸溶时一般加入浓盐酸进行溶解,请用化学方程式及必要文字解释原因:。
-
(5) 电镀锡渣中的锡与烧碱、硝酸钠溶液反应可生产锡酸钠,并产生一种碱性气体,该反应的化学方程式为。
-
(1) 天然气中含有的微量 H2S 会腐蚀管道和设备,在 1200℃下进行脱硫处理,H2S 会被氧气氧化为SO2 , 并产生水蒸气。
化学键
H-S
O=O
H-O
SO2 中共价键
键能/(kJ▪mol-1)
339
498
464
1083
请写出该反应的热化学方程式:.
-
(2) 利用 NaClO2/H2O2 酸性复合吸收剂可同时有效脱硫、脱硝,将 NO、SO2 氧化为硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液pH 对脱硫脱硝的影响如下图所示:
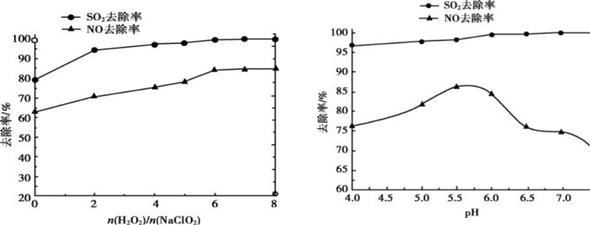
图 a 图 b
①从图a和图 b中可知脱硫脱硝最佳 n(H2O2)/n(NaClO2)是、最佳 pH 是。
②图b中 SO2 的去除率随pH 的增大而增大,而 NO 的去除率在pH>5.5 时反而减小,请解释 NO 去除率减小的可能原因。
-
(3) 臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g)
 N2O5(g)+O2(g),不同温度下,在体积为 1L 的甲、乙两个恒容密闭容器中均充入1mol O3 和 2 mol NO2 , 相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为 1L 的甲、乙两个恒容密闭容器中均充入1mol O3 和 2 mol NO2 , 相关信息如下图所示,请回答下列问题:
①0-15min 内乙容器中反应的平均速率:v(NO2)=。(保留2位有效数字)
②下列措施能提高容器乙中 NO2 转化率的是(填字母标号)
A.向容器中充入氦气,增大容器的压强
B.升高容器的温度
C.向容器中再充入一定量的 NO2
D.向容器中再充入1mol O3 和 2 mol NO2
 N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法错误的是( )
N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法错误的是( )
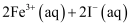
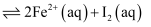 。下列说法正确的是( )
。下列说法正确的是( )
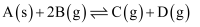 , 不能说明该反应已达到化学平衡的是( )
, 不能说明该反应已达到化学平衡的是( )
 的体积分数不随时间变化而变化
B . 压强不随时间变化而变化
C . 混合气体的密度不再发生改变
D . 单位时间内生成
的体积分数不随时间变化而变化
B . 压强不随时间变化而变化
C . 混合气体的密度不再发生改变
D . 单位时间内生成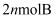 , 同时生成
, 同时生成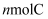
-
(1) CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a)
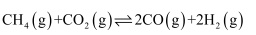
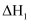
b)
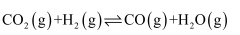

c)
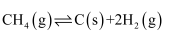
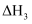
d)


e)
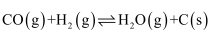

①根据盖斯定律,反应a的
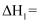 (写出一个代数式即可)。
(写出一个代数式即可)。②一定条件下,CH4分解形成碳的反应历程如图所示。该历程分步进行,其中,第步的反应最慢。
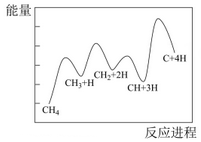
-
(2) 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。反应可表示为:
 。在起始物
。在起始物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 , 在
, 在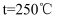 下的
下的 、在
、在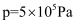 下的
下的 如图所示。
如图所示。
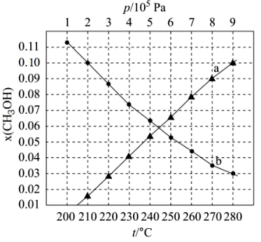
①用各物质的平衡分压[如
 的分压可表示为
的分压可表示为 ]表示该反应平衡常数,表达式
]表示该反应平衡常数,表达式 ;
;②图中对应等温过程的曲线是,判断的理由是;
③当
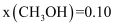 时,
时, 的平衡转化率
的平衡转化率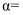 ,反应条件可能为或。
,反应条件可能为或。
- 下列各组词语中,没有错别字的一组是 A.稗官野史 纵横捭阖 爱乌及屋 吹毛求疵 B
- 紫茉莉的花色有红花、白花和粉红花三种类型,已知纯合红花与纯合白花杂交后代全部开粉红花。现对紫茉莉的花色和叶色进行遗传研究
- 2006年6月5日《人民日报》载文指出,农民是建设社会主义新农村的主要力量。农民的认识不统一、觉悟不提高、积极性得不到充
- 一个车间为了规定工时定额,需要确定加工零件所花费 的时间,为此进行了次试验,收集数据如下:实验顺序 第一次 第二次 第三
- 同学们用如图所示电路探究“电功与电流的关系”.以下观点不正确的是( ) A. 实验要选取规格不同的灯泡 B.
- 式子在实数范围内有意义,则 x 的取值范围是_______ .
- 已知点P(x,y)在不等式组表示的平面区域上运动,则z=x-y的取值范围是( )A.[-2,-1]
- 化简:= ▲
- 魔术师把手伸进一锅沸腾“油”,1分钟2分钟-------再把手拿出来——没事!对这一现象的分析正确的是 A.魔术师由特异
- 右图为我国著名画家张光宇在七七事变后所作的漫画《“七七”与“切切”》,图中的两人都是日本人。对下面这幅漫画的理解比较准确
- 在根式:①,②,③,④中,最简二次根式是( )A.①②B.③④C.①③D.①④
- 人站在小车上尽力水平推铅球,设人和小车的总质量为M,铅球的质量为m.若小车固定不动时,铅球被推出的速度为v0,那么,当地
- 下列句子中没有语病的一项(2分)( )A.学校开展的感恩活动,掀起了同学之间互帮、互助、互学、互进,增进了彼此的
- 一个带电粒子沿垂直于磁场方向射入一匀强磁场.粒子的一段径迹如图8-3-23所示.径迹上的每一小段都可以近似看成圆弧.由于
- 等体积等物质的量浓度的NaCl和NaClO溶液,两份溶液中离子总数相比A.前者多 B
- 东欧国家动荡不安的1989年,法国在进行它的200周年国庆纪念活动,7月14日,他们用飞机洒下了法国人引以为豪的“献给人
- 设函数. (Ⅰ)判断能否为函数的极值点,并说明理由; (Ⅱ)若存在,使得定义在上的函数在处取得最大值,求实数的最大值.
- “五一”期间,小刚从广州乘火车到北京旅游,沿途可能看到( ) A.湖南乡村片片茶园分布
- 下图为两种单基因遗传病的系谱图,已知个体6不带有甲病的致病基因。(甲病基因用B、b,乙病基因用A、a)(1)甲病是位于_
- The fire was finally ______ after the building had ______ fo



