甲烷的化学性质 知识点题库
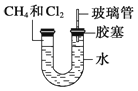
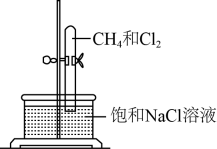
如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解度可以忽略.将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.
-
(1) 假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:
-
(2) 经过几个小时的反应后,U形管右端的玻璃管中水柱变化是 .
A.升高 B.降低 C.不变 D.无法确定
-
(3) 若水中含有Na2SiO3 , 则在U形管左端会观察到
-
(4) 右端玻璃管的作用是
请回答下列问题:
-
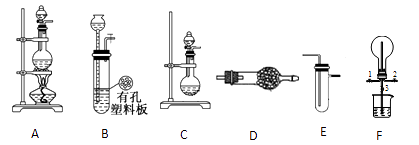
(1) 根据上述实验装置,用MnO2和浓盐酸制备纯净、干燥的Cl2 , 可选用的发生、净化装置连接顺序为→E→接E,第一个E装置的药品是。
-
(2) 根据上述实验装置,为制备干燥NH3 , 可选用的发生、净化装置为接。其中发生装置中可以选用的药品为(填选项字母)
a.碱石灰和浓氨水 b.浓H2SO4和浓氨水 c.碱石灰和氯化铵 d.生石灰和氯化铵
-
(3) 一定条件下,Cl2 与CH4在装置F中发生反应,其有机物有。(填化学式)
-
(4) 利用装置F可探究Cl2和NH3的反应。
已知Cl2与NH3可发生反应:3Cl+2NH3=N2+6HCl,实验时打开开关1、3,关闭2,先向烧瓶中通入Cl2 , 然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的NH3。
①不能先通入NH3的原因:。
②试验一段时间后烧瓶内出现的现象为: 。
③装置F中烧杯内发生反应的离子方程式为:。
④请设计一个实验方案(操作过程、实验现象)鉴定烧瓶内最终固体产物的阳离子,其方案为:。
-
(1) 甲烷具有型的空间结构,而乙炔则具有型结构。
-
(2) 苯酚遇FeCl3溶液会显色;蛋白质与浓硝酸共热会变色;淀粉遇碘则显色。这些特性常被用于物质的检验或鉴别。
-
(3) 构成蛋白质的氨基酸几乎都是
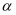 -氨基酸。若用R—表示烃基,
-氨基酸。若用R—表示烃基, 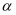 -氨基酸的结构通式可表示为。两个氨基乙酸分子在一定条件下能相互作用生成一种二肽,该反应的化学方程式为。
-氨基酸的结构通式可表示为。两个氨基乙酸分子在一定条件下能相互作用生成一种二肽,该反应的化学方程式为。
实验操作 | 现象 | 结论 | |
A | 食醋浸泡水垢 | 产生无色气体 | 乙酸的酸性比碳酸强 |
B | 乙醇与橙色酸性重铬酸钾溶液混合 | 橙色溶液变为绿色 | 乙醇具有氧化性 |
C | 向试管中加入苯,再加入酸性高锰酸钾溶液,振荡 | 分层,下层紫红色 | 苯与高锰酸钾溶液不反应 |
D | 甲烷通入氢氧化钠溶液中 | 无明显变化 | 甲烷的化学性质稳定 |
回答下列问题:
-
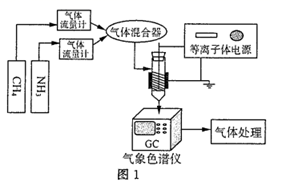
(1) 甲烷和氨气反应生成HCN和一种单质气体的化学方程式为。
-
(2) 实验室中制备CH4和NH3的反应原理分别为:
制备
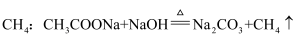
制备NH3(以浓氨水和生石灰为原料):。
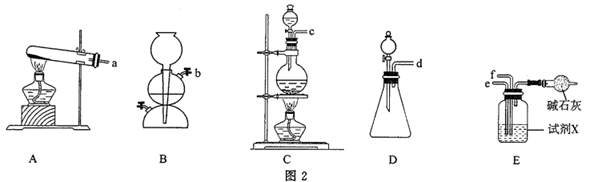
下图所示分别为制备CH4和NH3并得到合适体积比混合气体的装置,根据上述原理选择合适的仪器并连接成装置,则连接顺序为a→e,→f(填接口标号)。装置E中的试剂为(选填“饱和食盐水”、“浓硫酸”或“四氯化碳”)。装置E相当于上述图1装置中的。
-
(3) 实验过程中,选择不同的温度,对氰化氢和乙腈的选择性不同,下图所示为不同温度下甲烷的转化率和氰化氢、乙腈的选择性关系。高温时,甲烷的转化率升高,但乙腈的选择性却降低,原因是。
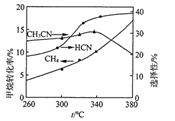
实验过程中,采用不同的催化剂,HCN的产率不同,下图所示分别为不同温度,不同催化剂条件下HCN、H2和N2的产率关系图。
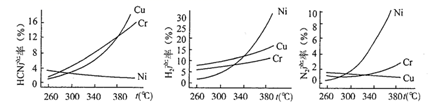
由图可知,低温条件下最适宜的催化剂为,高温条件下,选择该催化剂不如另外两种作催化剂时HCN产率高的原因是。
 既是一种重要的能源,也是一种重要的化工原料。
既是一种重要的能源,也是一种重要的化工原料。
-
(1) 甲烷分子的空间构型为。
-
(2) 如图是某同学利用注射器设计的简易实验装置。甲管中注入10mLCH4 , 同温、同压下乙管中注入50mL
 , 将乙管气体全部推入甲管中,用日光照射一段时间,气体在甲管中反应。
, 将乙管气体全部推入甲管中,用日光照射一段时间,气体在甲管中反应。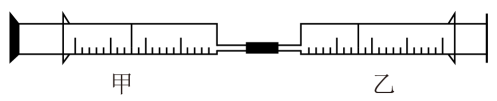
①某同学预测的实验现象:a.气体最终变为无色;b.反应过程中,甲管活塞向内移动;c.甲管内壁有油珠;d.产生火花。其中正确的是(填字母,下同)。
②实验结束后,甲管中剩余气体最宜选用下列试剂吸收。
A.水 B.氢氧化钠溶液 C.硝酸银溶液 D.饱和食盐水
③反应结束后,将甲管中的物质推入盛有适量
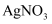 溶液的试管中,振荡后静置,可观察到,再向其中滴加几滴石蕊试液,又观察到。
溶液的试管中,振荡后静置,可观察到,再向其中滴加几滴石蕊试液,又观察到。 -
(3) 甲烷可直接应用于燃料电池,该电池采用可传导
 的固体氧化物为电解质,其工作原理如图所示。
的固体氧化物为电解质,其工作原理如图所示。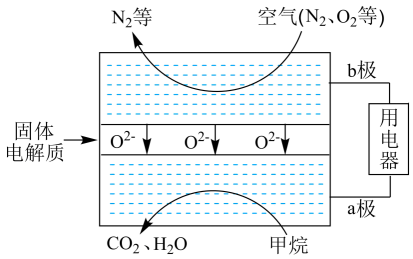
①外电路电子移动方向为(填“a→b”或“b→a”)。
②a极的电极反应式为。
③若该燃料电池消耗空气5.6L(标准状况下),则理论上消耗甲烷mol(假设空气中
 体积分数为20%)。
体积分数为20%)。
- 下图每一方框中的字母代表一种反应物或生成物:产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质。试
- 如图,将等腰直角△ABC沿BC方向平移得到△A1B1C1.若BC=3,△ABC与△A1B1C1重叠部分面积为2,则BB1
- 在下列命题中:①若、共线,则、所在的直线平行; ②若、所在的直线是异面直线,则、一定不共面; ③若、、三向量两两共面,则
- 下列物质与水反应生成强酸的是 A.Na2O2 B.SiO2 C.NO2
- 如图所示,实直线是某电场中的一条电场线,虚线是该电场中的两条等势线,由图可以得出的正确结论是:A.M点的电势一定高于N点
- 恩格斯说:“它无疑是全部社会主义文献中传布最广和最带国际性的著作,是从西伯利亚起到加利福尼亚的世界各国千百万工人共同的纲
- 新时期我国农村改革是不断总结经验的基础上逐步展开、递次推进的,它经历了从“大包干”到税费改革,再到包括乡镇机构和管理体制
- 下列各组元素中,元素符号的第一字母相同的一组是( ) A.氯、碳、钙、铜 B.氢、汞、铁、银
- 已知a>b>c,且a+b+c=0,则b2-4ac( )A.恒正 B.恒负
- 常温下,下列混合溶液中,各离子浓度的关系正确的是A.pH=12的氨水溶液与pH=2的盐酸溶液等体积混合c()>c(Cl-
- 哲学的两大基本派别是 A、唯物主义和唯心主义 B、主观唯心主义和客观唯心主义 C、可知论与不可知论 D、辩证法和形而上学
- 一艘轮船在静水中的最大航速为30千米/时,它沿江以最大航速顺流航行100千米所用时间,与以最大航速,逆流航行60千米所用
- ......
- 为了制定一个符合中国国情和时代特点的《国家中长期教育改革和发展规划纲要(2010——2020年)》(简称《纲要》),政府
- 《中国史纲》指出“他(秦始皇)让秦国原有的军队依旧集中在秦国本部,少数地方兵只是警察的性质。……为的是任何地方若有叛乱,
- 如图,Rt△ABO的两直角边OA、OB分别在x轴的负半轴和y轴的正半轴上,O为坐标原点,A、B两点的坐标分别为(-3,0
- 一容器中X元素构成的气态单质X2分子有3种,相对分子质量分别为32、34、36。又知容器中3种分子数之比为15∶4∶1。
- 在△ABC中,a、b、c分别为∠A、∠B、∠C的对边,三边a、b、c成等差数列,且B=,则|cosA一cosC|的值为
- 实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是 A.950m
- 在十二届二次全国人大会议上,李克强总理所作的《政府工作报告》中指出:“各级政府要自觉接受同级人大及其常委会的监督,接受人



