化学反应中能量的转化 知识点题库
已知反应X+Y═M+N为放热反应,对该反应的说法正确是( )
A . X的能量一定高于M
B . Y的能量一定高于N
C . X和Y的总能量一定高于M和N的总能量
D . 因为该反应为放热反应,故不必加热就可发生
化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( ) 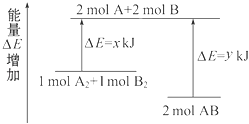
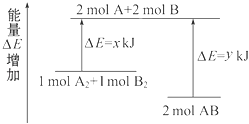
A . 该反应是吸热反应
B . 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
C . 断裂1 mol A﹣A键和1 mol B﹣B键能放出x kJ能量
D . 断裂2 mol A﹣B键需要吸收y kJ的能量
下图是2SO3(g) ⇌ 2SO2(g) + O2(g) 的能量变化图,据图得出的相关叙述正确的是( )

A . 2SO3(g) ⇌ 2SO2(g) + O2(g) + (a-b) kJ
B . 1mol SO2的能量比1mol SO3的能量高
C . 若有2mol SO3充分反应,吸收(a-b) kJ热量
D . 该化学反应过程中的能量变化既有吸热又有放热
下图表示某可逆反应在其他条件相同时使用和未使用催化剂,反应过程和能量的对应关系。下列说法一定正确的是( )
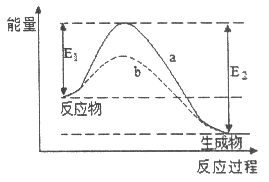
A . 该反应为吸热反应
B . a与b相比,a的反应速率更快
C . a与b相比,反应的平衡常数一定不同
D . 反应物的总能量大于生成物的总能量
氢卤酸的能量关系如图所示,下列说法正确的是( )
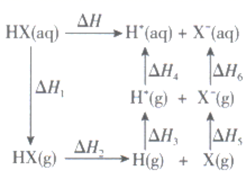
A . 已知 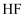 气体溶于水放热,则
气体溶于水放热,则 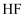 的△H1<0
B . 相同条件下,
的△H1<0
B . 相同条件下,  的△H2比
的△H2比 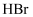 的小
C . 相同条件下,
的小
C . 相同条件下,  的(△H3+△H4)比
的(△H3+△H4)比 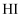 的大
D . 一定条件下,气态原子生成
的大
D . 一定条件下,气态原子生成 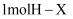 键放出
键放出 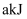 能量,则该条件下△H2=+akJ/mol
能量,则该条件下△H2=+akJ/mol
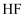 气体溶于水放热,则
气体溶于水放热,则 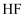 的△H1<0
B . 相同条件下,
的△H1<0
B . 相同条件下,  的△H2比
的△H2比 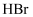 的小
C . 相同条件下,
的小
C . 相同条件下,  的(△H3+△H4)比
的(△H3+△H4)比 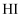 的大
D . 一定条件下,气态原子生成
的大
D . 一定条件下,气态原子生成 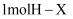 键放出
键放出 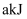 能量,则该条件下△H2=+akJ/mol
能量,则该条件下△H2=+akJ/mol
反应 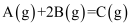 的能量变化与反应进行的关系如图所示,下列说法中错误的是( )
的能量变化与反应进行的关系如图所示,下列说法中错误的是( )
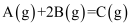 的能量变化与反应进行的关系如图所示,下列说法中错误的是( )
的能量变化与反应进行的关系如图所示,下列说法中错误的是( )
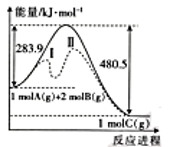
A . 图中虚线表示加入了催化剂
B . 加入催化剂,反应速率加快但反应焓变不变
C . 图中虚线表示的反应I、反应II均为放热反应
D . 该反应的焓变 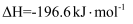
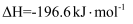
以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如下图所示。
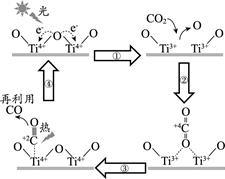
下列说法正确的是( )
A . 过程①中钛氧键断裂会释放能量
B . 该反应中,光能和热能转化为化学能
C . 使用TiO2作催化剂可以降低反应的焓变,从而提高化学反应速率
D . CO2分解反应的热化学方程式为2CO2(g) =2CO(g) + O2(g) ΔH= + 30 kJ/mol
我国科研人员提出了由小分子X、Y转化为高附加值产品M的催化反应历程。该历程可用示意图表示如图,下列说法错误的是( )
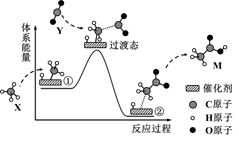
A . ①→②过程有热量放出
B . X、Y、M分别为甲烷、二氧化碳和乙酸
C . 反应过程中有C-H键、C-C键、O-H键生成
D . 由X、Y生成M的总反应原子利用率为100%
根据能量变化示意图,下列说法不正确的是( )
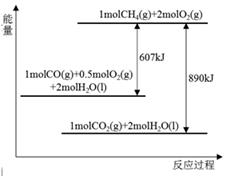
A . 2 mol CO(g)与1 mol O2(g)完全反应生成2 mol CO2(g)时要释放 566 kJ 的能量
B . 1 mol CH4(g)与2 mol O2(g)具有的总能量高于1 mol CO2(g)与2 mol H2O(l)
C . 1 mol CH4(g)完全燃烧生成气态水时释放的能量小于890 kJ
D . 16 kg 液化天然气完全燃烧释放的能量为890000 kJ
以CO2、H2为原料合成CH3OH涉及的主要反应如下:
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49.5 kJ/mol
②CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4 kJ/mol
③CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
不同压强下,按照n(CO2):n(H2)=1:3投料,CO2平衡转化率随温度变化关系如图。下列说法正确的是( )
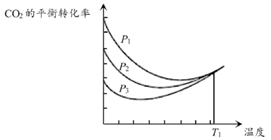
A . ∆H3=-40.9 kJ/mol
B . p1 < p2 < p3
C . 为同时提高CO2的平衡转化率和CH3OH的平衡产率,反应条件应选择高温、高压
D . T1温度时,三条曲线几乎交于一点的原因是:该温度下,主要发生反应③
如图所示,下列叙述正确的是( )
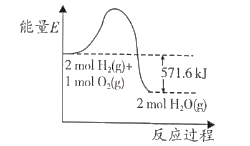
A . 生成物能量总和大于反应物能量总和
B . 生成 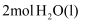 要吸收571.6kJ热量
C .
要吸收571.6kJ热量
C . 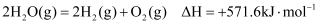 D .
D . 
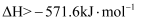
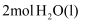 要吸收571.6kJ热量
C .
要吸收571.6kJ热量
C . 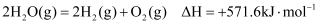 D .
D . 
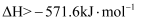
二氧化碳加氢制甲醇(CH3OH)的反应机理一般表示为如下步骤:
① 
② 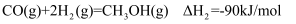
若反应②为快反应,下列示意图中能体现上述反应能量变化的是( )
A . 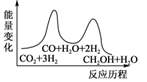 B .
B . 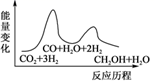 C .
C . 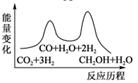 D .
D . 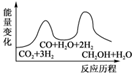
 B .
B .  C .
C .  D .
D . 
10月16日,搭载神舟十三号载人飞船的长征二号F遥十三运载火箭,在酒泉卫星发射中心点火升空。长征系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法错误的是( )
A . 煤油和液氢都是可再生能源
B . 火箭燃料燃烧时,化学能转化为热能
C . 运载火箭主体结构件框所用高精尖铝合金材料具有质量轻、强度高等优点
D . 液氢属于纯净物,煤油属于混合物
下列有关说法正确的是( )
A . 所有非金属元素都分布在元素周期表的p区
B . 构成原电池的两个电极不可采用相同的电极材料
C . 第一电离能的大小可作为判断元素金属性强弱的依据
D . 铜锌原电池放电一段时间后溶液温度升高,此时化学能同时转化为电能和热能
HCHO(g)与O2在羟基磷灰石(HAP)表面发生催化氧化生成CO2、H2O(g)的历程可能如图所示(E1、E2和E3分别表示各阶段物质的能量):
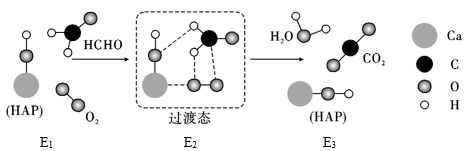
已知:HCHO(g)+O2(g)=CO2(g)+H2O(g)ΔH=-526.7kJ·mol-1
下列说法正确的是( )
A . E1>E2>E3
B . HAP能减小上述反应的焓变
C . HAP可使上述反应在较低的温度下迅速进行
D . 若改通18O2 , 则反应可表示为HCHO+18O2=C18O2+H2O
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
-
(1) 已知断开1molH−H键、1molN−H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、945kJ,则H2与足量N2反应生成2molNH3需(填“吸收”或“放出”)能量kJ。
-
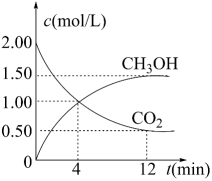
(2) 科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以一定比例混合通入反应器,适当条件下可获得甲醇(CH3OH)。某温度下在1L的恒容密闭容器中,充入2molCO2和6molH2 , 发生如下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。①能判断该反应已达到化学反应限度标志的是(填字母)。
A.容器内压强保持不变
B.容器中H2浓度与CO2浓度之比为3:1
C.容器中混合气体的质量保持不变
D.CO2的生成速率与CH3OH的生成速率相等
②现测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始经过12min达到平衡,则这段时间氢气的平均反应速率υ(H2)= mol∙L−1∙min−1。
下列表示化学反应2H2(g)+ O2(g)= 2H2O(g)过程能量变化的示意图中,合理的是( )
A . 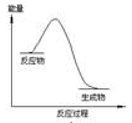 B .
B . 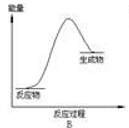 C .
C . 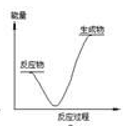 D .
D . 
 B .
B .  C .
C .  D .
D . 
下列关于化学反应与能量变化的说法中,错误的是( )
A . 放热反应都是不需要加热条件的
B . 能量变化是化学反应的基本特征之一
C . 化学键的断裂与形成是化学反应中能量变化的主要原因
D . 反应物的总能量高于生成物的总能量,发生反应时能够向环境放出能量
近日IPCC发布了由来自40个国家的91位科学家编写的《全球升温1.5℃特别报告》,报告表明:温室效应引发的环境问题日益严重,CO2的减排和综合利用是解决温室效应及能源问题的有效途径,将CO2转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入3molCO2和9molH2 , 一定条件下发生反应CO2(g)+3H2(g)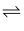 CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的物质的量随时间变化情况如表所示,并根据数据绘制图像如图(已知相同条件下气体的压强之比等于物质的量之比):
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的物质的量随时间变化情况如表所示,并根据数据绘制图像如图(已知相同条件下气体的压强之比等于物质的量之比):
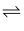 CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的物质的量随时间变化情况如表所示,并根据数据绘制图像如图(已知相同条件下气体的压强之比等于物质的量之比):
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的物质的量随时间变化情况如表所示,并根据数据绘制图像如图(已知相同条件下气体的压强之比等于物质的量之比):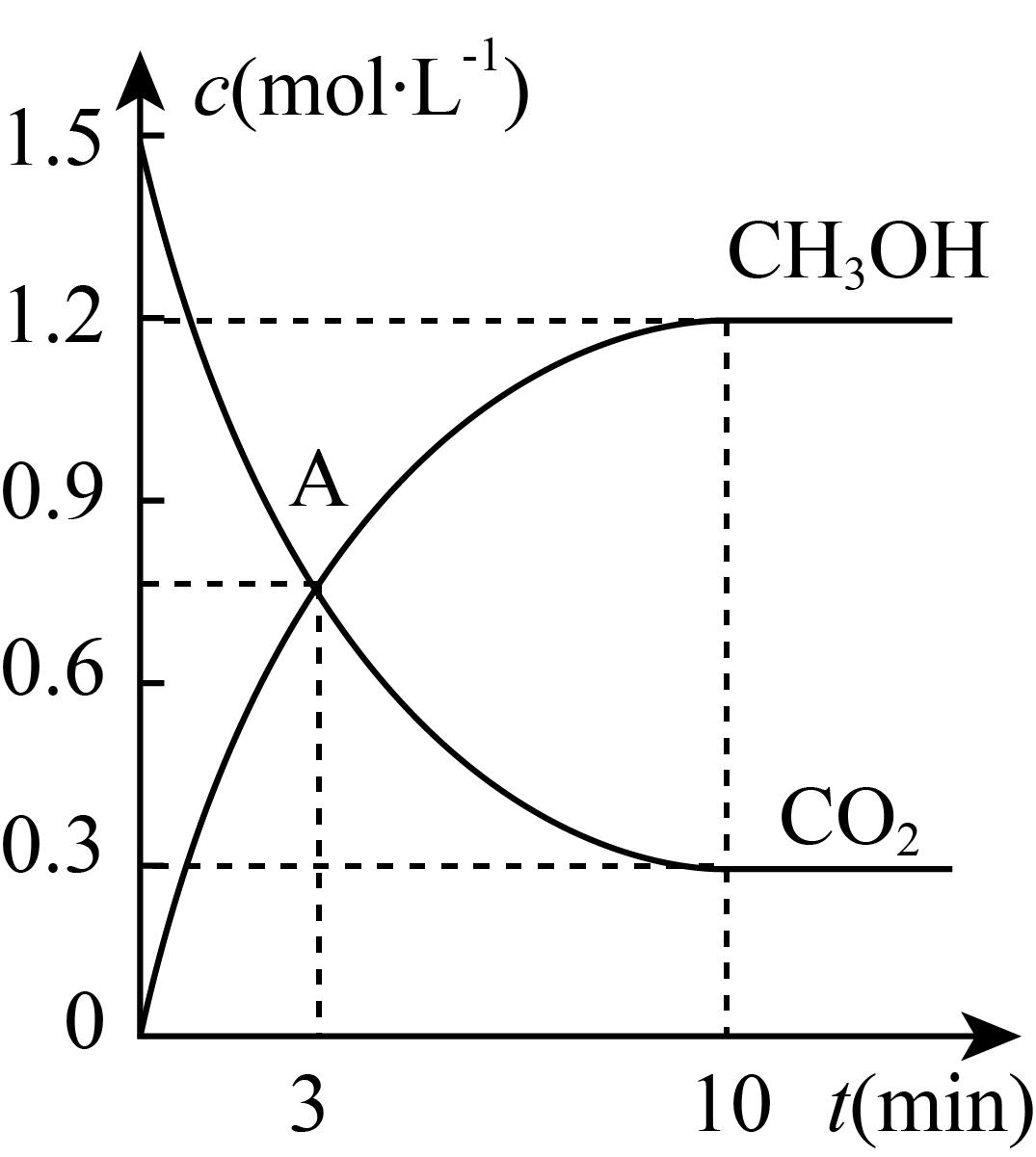
时间 | 0min | 3min | 6min | 10min | 12min |
n(CH3OH)/mol | 0 | 1.5 | 2.1 | 2.4 | 2.4 |
n(CO2)/mol | 3 | 1.5 | 0.9 | a | 0.6 |
回答下列问题:
-
(1) a=;A点(填“是”或“不是”)化学平衡状态。
-
(2) 5min时,正反应速率(填“>”、“<”或“=”)逆反应速率。
-
(3) 相同条件下,10min时体系的压强与开始反应时的压强之比为。
-
(4) 为提高此反应的速率,下列措施可行的是____(填字母代号)。A . 恒容时充入氦气 B . 降低温度 C . 使用合适的催化剂 D . 移出CO2
-
(5) 该反应的能量变化关系如图所示:
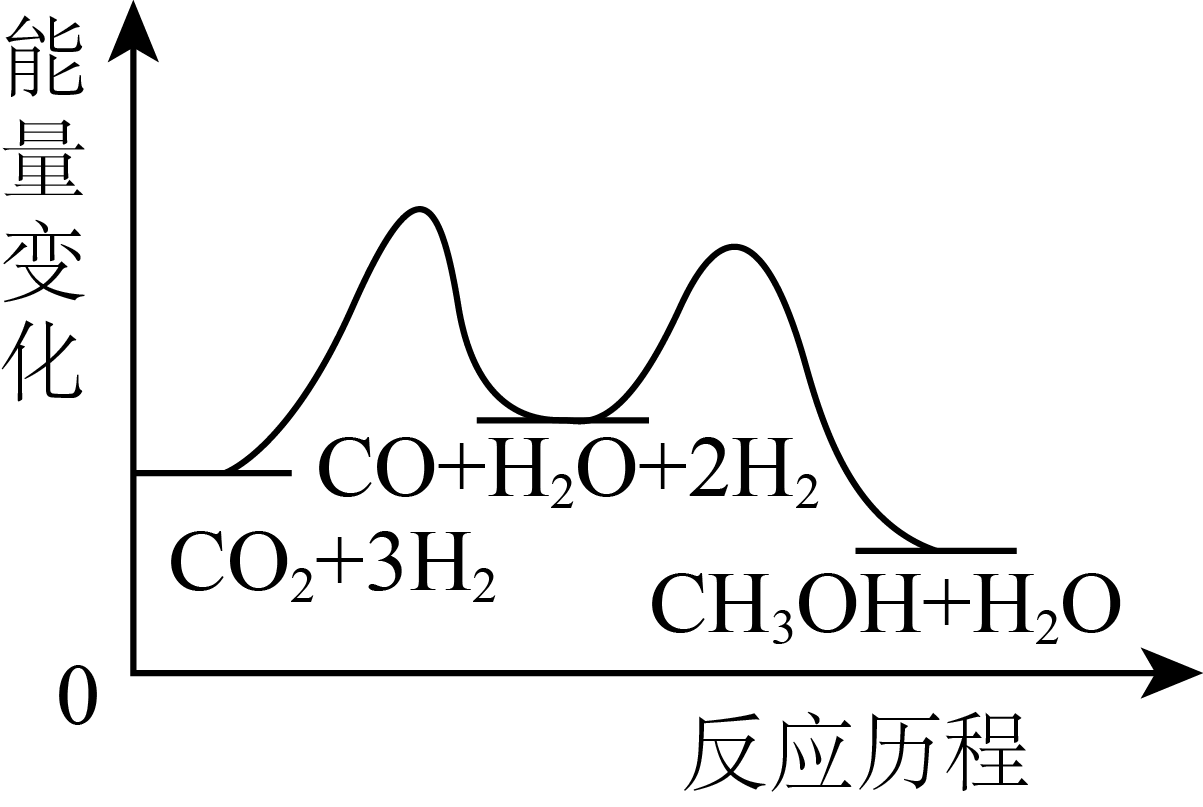
该反应属于(填“放热”或“吸热”)反应。
-
(6) 所得的CH3OH可以作燃料电池的燃料。CH3OH燃料电池是目前开发最成功的燃料电池之一,从节约能源和保护生态环境的角度来看是很有发展前途的发电技术。CH3OH燃料电池由CH3OH、空气(氧气)、KOH(电解质溶液)构成。下列说法正确的是____(填字母代号)。
已知:该燃料电池的总反应为2CH3OH+3O2+4OH-=2CO
 +6H2OA . 电池放电时,通入空气的电极为负极 B . 电池放电时,电解质溶液的碱性逐渐减弱 C . 电池放电时,理论上每消耗6.4gCH3OH转移1.2mol电子 D . 负极的电极反应式为CH3OH-6e-+H2O=CO2+6H+
+6H2OA . 电池放电时,通入空气的电极为负极 B . 电池放电时,电解质溶液的碱性逐渐减弱 C . 电池放电时,理论上每消耗6.4gCH3OH转移1.2mol电子 D . 负极的电极反应式为CH3OH-6e-+H2O=CO2+6H+
一种碘硫热化学分解、水循环制氢的化学工艺流程如图所示,下列说法错误的是( )
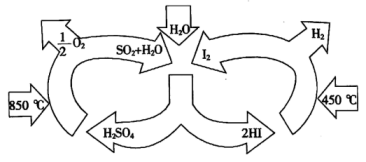
A . 该工艺流程图中只有化学能与热能之间的相互转化
B . 该工艺流程图中生成氢气与氧气的反应均为吸热反应
C . 该工艺流程中 和
和 为催化剂
D . 该工艺需要消耗大量的热能
为催化剂
D . 该工艺需要消耗大量的热能
 和
和 为催化剂
D . 该工艺需要消耗大量的热能
为催化剂
D . 该工艺需要消耗大量的热能
最近更新
- 乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示。将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应
- 在高等植物细胞有丝分裂过程中,下列直接参与活动的细胞器有() A. 高尔基体和核糖体B. 高尔基体和中心体 C. 叶绿体
- 设点B是点A(2,-3,5)关于xOy面的对称点,则|AB|=( ) A.10 B. C.
- 如图,在平面直角坐标系中,等腰梯形ABCD的顶点A.B.D的坐标分别是(0,0)、(5,0)、(1,3),则顶点C的坐标
- 【浙江省衢州市】 纪鸮①鸣 【唐】林简言 ⑴东渭桥有贾食于道者,其舍之庭有槐焉,耸干舒柯,布叶凝翠,不与他槐等。其舍既陋
- 如图1,是的直径,弦于点,连结,若,,则OE=( ▲ ) A. 1 B.2 C.3
- 溶液在生产、生活中起着十分重要的作用。请回答下列问题: (1)可以作为溶质的是_________。 A.只有固体 B.
- 下列句子中画线的词语使用不当的一项是( ) A.我的眼前仿佛看见冬花开在雪野中,有许多蜜蜂忙碌地飞着,也听得他们
- 图一是将含有生长素的琼脂块放在切去尖端的胚芽鞘的一侧,胚芽鞘弯曲的情况(弯曲角度用A表示);图二是生长素对胚芽鞘生长的促
- 如图1所示,A、B两物体叠放在水平面上,质量分别为mA=1kg,mB=4kg,B与水平面间的动摩擦因数为μ=0.2.当
- 化学反应前后肯定发生变化的是A.原子数目 B.原子质量 C.物质种类 D.元素种类
- 常温下体积相同的下列四种溶液:①pH=3的盐酸 ②pH=3的醋酸溶液 ③pH=11的氨水 ④pH=11的NaOH溶
- 胚胎的发育场所是 ( )A.脐带B.羊水C.胎盘D.子宫
- 2008年10月28日,孔子家族最后一代“衍圣公”──孔子第77代长孙孔德成在台北慈济医院病逝。“衍圣公”是孔子嫡派后裔
- .晓明看电视剧《封神演义》时看到这样一个镜头:周武王联合800多个部落击败商朝军队,纣王自焚,商朝灭亡。与这一镜头相关的
- 有氧呼吸与无氧呼吸的相同点是( ) ①都在线粒体中进行 ②都需要酶 ③都需要氧 ④都产生ATP
- 把文言文中画横线的句子翻译成现代汉语。 (1)古人有羹污衣、烛然须不动声色者,主能言不能行乎? 译文:
- (本小题满分10分)已知三条直线l1:,l2:,:,它们围成. (I)求证:不论取何值时,中总有一个顶点为定点; (II
- 以下推理合理的是 A. 含碳元素的物质充分燃烧会有CO2生成,则燃烧能生成CO2的物质一定含碳元素 B. 化合物是由不同
- ____ felt funny watching myself on TV.A. One B. T



