化学反应中能量的转化 知识点题库
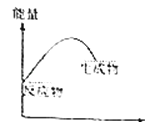 B .
B . 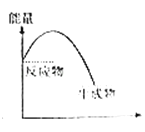 C .
C . 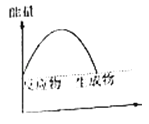 D .
D . 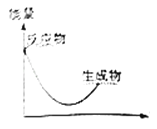
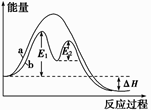
(1)生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和.
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量 (填“>”、“<”或“=”)572kJ.
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能(kJ/mol) | 436 | 243 | 431 |
对于反应H2(g)+Cl2(g)=2HCl(g)的能量变化描述正确的是( )
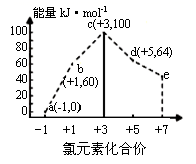
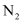 、CO、
、CO、  、
、  和少量
和少量  ,经“脱硫”、转换反应可制得合成氨原料气。
,经“脱硫”、转换反应可制得合成氨原料气。
-
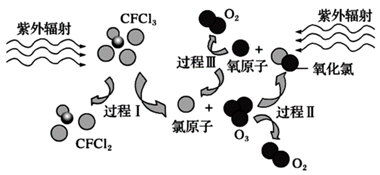
(1) 这种半水煤气跟空气按一定比例混合后通入
 、
、 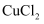 的混合溶液中完成“脱硫”,其转化过程如图所示,该过程中发生多个反应,总反应为
的混合溶液中完成“脱硫”,其转化过程如图所示,该过程中发生多个反应,总反应为  ,该转化过程中起催化作用的离子为,写出该过程中属于非氧化还原反应的离子方程式。
,该转化过程中起催化作用的离子为,写出该过程中属于非氧化还原反应的离子方程式。 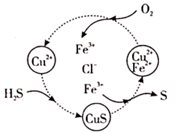
-
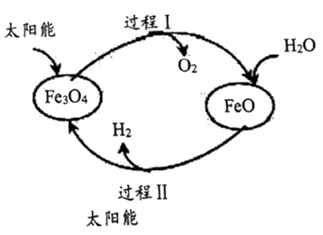
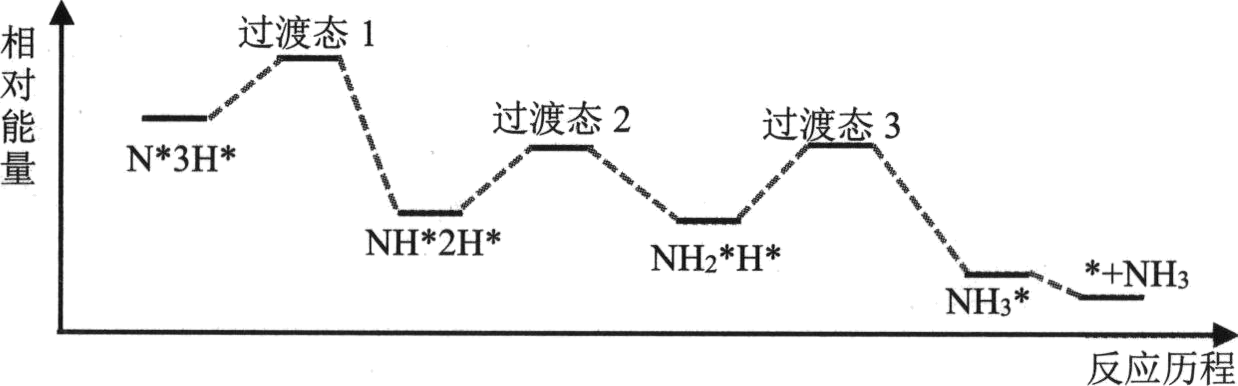
(2) 脱硫后的半水煤气与水蒸气以1:15比例混合后通入转换塔中,变换反应为:
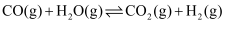 。该反应用氧化铁作催化剂,其活性组分是四氧化三铁。研究发现,变换反应经下列两步完成:
。该反应用氧化铁作催化剂,其活性组分是四氧化三铁。研究发现,变换反应经下列两步完成: 第一步:
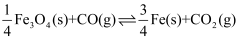
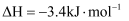 (慢反应)
(慢反应)第二步:
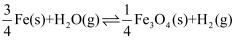
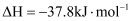 (快反应)
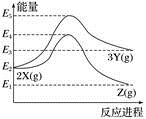
(快反应)①在下图中绘制变换反应(经上述催化反应过程)的“能量~反应过程”示意图。

②由于
 和CO还原性较强,能够将氧化铁直接还原成铁而使催化剂失活,但实际生产中一般不会发生这种情况,请从反应速率,化学平衡角度解释可能的反应过程原因是。
和CO还原性较强,能够将氧化铁直接还原成铁而使催化剂失活,但实际生产中一般不会发生这种情况,请从反应速率,化学平衡角度解释可能的反应过程原因是。 -
(3) 半水煤气处理后得到的混合气中,可通过在熔融碳酸盐中经电化学还原消除其中的二氧化碳,并得到高纯度的碳,写出生成碳的电极反应式为。
-
(1) 铝的冶炼、提纯的方法很多。
①高温碳热歧化氯化法冶铝包含的反应之一为:Al2O3(s)+AlCl3(g)+3C(s)
 3CO(g)+3AlCl(g),其平衡常数表达式为K=。
3CO(g)+3AlCl(g),其平衡常数表达式为K=。②碳热还原Al2O3冶铝的部分反应如下:
Ⅰ.2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) △H1=akJ/mol
Ⅱ. 4Al2O3(s)+Al4C3(s)=3Al4O4C(s) △H2=bkJ/mol
Ⅲ. Al4O4C(s)+Al4C3(s)=8Al(g)+4CO(g) △H3=ckJ/mol
反应Al2O3(s)+3C(s)=2Al(g)+3CO(g)的△H=kJ/mol
③用离子液体AICb-BMIC(阳离子为EMIM+、阴离子为AlCl4-、Al2Cl7-)作电解质,可实现电解精炼铝。粗铝与外电源的极(填“正”或“负")相连;工作时,阴极的电极反应式为。
-
(2) 真空条件及1173K时,可用铝热还原Li5AlO4制备金属锂(气态),写出该反应的化学方程式:。
-
(3) 用Al、Fe或Al-Fe合金还原脱除水体中的硝态氮(NO3--N),在45℃,起始c(KNO3-N)为50mg·L-1、维持溶液呈中性并通入Ar等条件下进行脱除实验。结果如图所示(c0为起始浓度、c为剩余浓度):
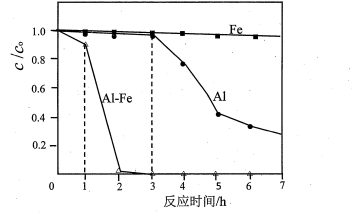
①纯Al在0~3h时,NO3-几乎没有被脱除,其原因是;写出3h后NO3-被还原为N2的离子方程式:。
②Al-Fe合金1~2h比纯Al 3~4h的脱除速率快得多的可能原因是。
-
(1) 已知:
 、
、  分子中化学键的键能分别是
分子中化学键的键能分别是 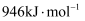 、
、 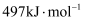

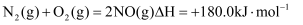
则相同条件下破坏1molNO中化学键需要吸收的能量为kJ。
-
(2) 如图所示,U形管内盛有100mL的溶液,
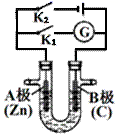
①断开
 ,闭合
,闭合 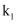 ,若所盛溶液为
,若所盛溶液为 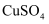 溶液:则A为极。若所盛溶液为KCl溶液:
溶液:则A为极。若所盛溶液为KCl溶液: 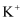 移向极
移向极  填“A”、“B”
填“A”、“B” 
②断开
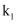 ,闭合
,闭合  ,若所盛溶液为滴有酚酞的NaCl溶液,则:A电极附近可观察到的现象是。反应一段时间后打开
,若所盛溶液为滴有酚酞的NaCl溶液,则:A电极附近可观察到的现象是。反应一段时间后打开  ,若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的。
,若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的。③若是电解精炼粗铜,断开
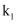 ,闭合
,闭合  ,电解液选用
,电解液选用 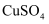 溶液,则A电极的材料应换成,反应一段时间后电解质溶液中
溶液,则A电极的材料应换成,反应一段时间后电解质溶液中  浓度
浓度  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 
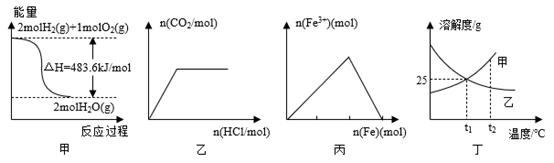
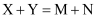 为放热反应,对该反应的下列说法中正确的( )
为放热反应,对该反应的下列说法中正确的( )
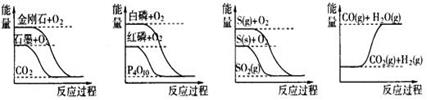
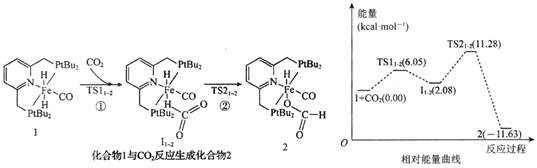
据此判断下列说法中正确的是( )
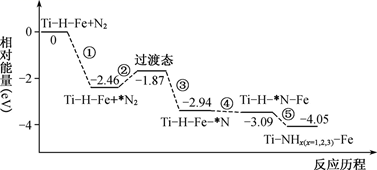
- --How many hours does the boss make the workers __ a day?--A
- (09年东城区二模文)已知点在直线上,点在直线上,中点为,且,则的取值范围是_________.
- 2010年10月20日,政协十一届全国委员会常务委员会第十一次会议在北京开幕。这次会议的主要议题是学习贯彻中共十七届五中
- III 词汇基础 (共三节, 满分35分) 第一节 语法填空(共10小题;每小题1.5分,满分15分) 阅读下面短文,
- 解方程:
- 由甲城市到乙城市t分钟的电话费由函数g(t)=1.06×(0.75[t]+1)给出,其中t>0,[t]表示大于或等
- 读下图,利用所学过的地理知识,回答问题。(7分) (l)图中爱尔兰的都柏林和纽芬兰的圣约翰斯所处的纬度差不多,但1月份都
- 为了防止送往香港的蔬菜和水果变质,可以利用干冰在 时会从蔬菜和水果中 (填“吸”或“放”)热,来降低它们的
- 某校正在进行“网络语言能否进作文”的辩论赛,请你针对正方的发言,作为反方代表写一段辩词,要求语言得体,反驳有力,运用比喻
- 如图,表示下列某个不等式的解集,其中正确的是()A.x>2 B.x<2 C.x≥2 D.x≤﹣2
- “闯关东”是我国近代史上一个独特的现象。电视剧《闯关东》从艺术形式再现了这段历史,成为一部叫好又叫座的主旋律电视剧。回
- 下列各项,划线成语使用恰当的一项是( ) A乔光仆放着轻车熟路不走,明知现在基层的经最难念,却偏下基层去。 B
- 分别刺激图中的Ⅰ、Ⅱ、Ⅲ、Ⅳ四处,不能引起肌肉收缩的是()A.Ⅰ B.Ⅱ C.Ⅲ D.Ⅳ
- 人类遗传病有多种诊断方法,通过患者对颜色的判断来进行诊断的遗传病是( ) A.21三体综合症
- 在溶液中加入大量Na2O2后仍能大量共存的离子组是( ) A.NH4+、Ba2+、Cl-、NO3-
- “a和b都不是偶数”的否定形式是() A.a和b至少有一个是偶数 B.a和b至多有一个是偶数 C.a是偶数,b不
- 抛物线y=-x2上的点到直线4x+3y-8=0的距离的最小值是.
- 某班13位同学参加每周一次的卫生大扫除,按学校要求需要完成总面积为80m2的三项任务,它们的面积比例及每人每分钟完成各项
- 用显微镜观察洋葱根尖的装片时,为使视野内看到的细胞数目最多,应选用()A.目镜5× 物镜10×
- 如图,某居民小区内A、B两楼之间的距离MN=30米,两楼的高都是20米,A楼在B楼正南,B楼窗户朝南.B楼内一楼住户的窗



