元素周期表的结构及其应用 知识点题库
X,Y,Z三种短周期元素,原子半径的大小关系为:r (Y)>r(X)>r(Z),原子序数之和为16。X,Y,Z三种元素的常见单质在适当条件下可发生右图所示变化,其中B和C均为10电子分子。下列说法不正确的是( )
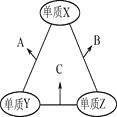
A . X元素位于ⅥA族
B . A不能溶于B中
C . A和C不可能发生氧化还原反应
D . B的沸点高于C的沸点
关于原子序数为53的元素,以下说法正确的是( )
A . 位于第六周期
B . 是金属元素
C . 最外电子层含有6个电子
D . 属于卤族元素
“蛟龙”号外壳用特殊的钛合金材料制成,它可以在深海中承受700个大气压的压力.已知金属钛的原子序数为22,化学性质与铝类似.下列说法正确的是( )
A . 钛属于主族元素
B . 钛合金强度很大
C . 蒸干TiCl4溶液可得无水钛盐
D . 在空气中将金属钛、铝混合后熔化可制得合金
某元素原子序数为85,下面关于该元素说法不正确的是( )
A . 它的银盐不溶于水
B . 它的氢化物很不稳定
C . 它的单质是白色固体
D . 该元素位于元素周期表第六周期、第十七列
如果n为第ⅡA族中某元素的原子序数,则原子序数为(n+1)的元素可能位于( )
A . ⅢA或ⅢB
B . ⅣA
C . ⅠB
D . ⅠA
短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数。X与Y位于不同周期,X与W的最高化合价之和为8,元素Z的单质是目前使用量最大的主族金属元素单质。下列说法中正确的是( )
A . 化合物YX4W溶于水后,得到的溶液呈碱性
B . 化合物YW3为共价化合物,电子式为 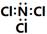 C . Y、Z形成的一种化合物强度高,热膨胀系数小,是良好的耐热冲击材料
D . 原子半径大小:W>Z>Y>X
C . Y、Z形成的一种化合物强度高,热膨胀系数小,是良好的耐热冲击材料
D . 原子半径大小:W>Z>Y>X
元素周期表共有18个纵列,下列有关元素周期表的说法不正确的是( )
A . 第3列含有的元素种类最多
B . 第14列元素所形成的化合物种类最多
C . 第2列到第12列都是金属元素
D . 最高价为+7的元素均在第17列
有关元素周期表的说法中错误的是( )
A . 元素周期表中第16个纵行为ⅥA族
B . ⅦA族元素也称为卤族元素
C . 0族元素的原子最外层电子数均为8,元素化合价为0
D . 元素周期表中,Ⅷ族包括第8,9,10三个纵行
四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是( )
A . 简单离子半径: 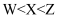 B . W与X形成的化合物溶于水后溶液呈碱性
C . 气态氢化物的热稳定性:
B . W与X形成的化合物溶于水后溶液呈碱性
C . 气态氢化物的热稳定性: 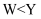 D . 最高价氧化物的水化物的酸性:
D . 最高价氧化物的水化物的酸性: 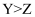
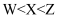 B . W与X形成的化合物溶于水后溶液呈碱性
C . 气态氢化物的热稳定性:
B . W与X形成的化合物溶于水后溶液呈碱性
C . 气态氢化物的热稳定性: 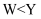 D . 最高价氧化物的水化物的酸性:
D . 最高价氧化物的水化物的酸性: 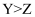
X、Y、Z、Q、E、M六种元素中,X的原子的基态价电子排布式为2s2 , Y的基态原子核外有5种运动状态不同的电子,Z元素的两种同位素原子通常作为示踪原子研究生物化学反应和测定文物的年代,Q是元素周期表中电负性最大的元素,E的阳离子通常存在于硝石、明矾和草木灰中,M的原子序数比E大1。下列说法正确的是( )
A . EYQ4 中阴离子中心原子的杂化方式为sp3杂化
B . X、Y元素的第一电离能大小关系:X<Y
C . ZO32-的空间构型为V形
D . MZ2仅含离子键,可用于制备乙炔
周期表前四周期的元素  、
、  、
、 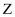 、
、 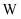 ,原子序数依次增大,X原子核外有 6 种不同运动状态的电子;
,原子序数依次增大,X原子核外有 6 种不同运动状态的电子;  原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;
原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料; 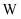 位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
 、
、  、
、 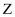 、
、  ,原子序数依次增大,X原子核外有 6 种不同运动状态的电子;
,原子序数依次增大,X原子核外有 6 种不同运动状态的电子;  原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;
原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;  位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
-
(1) X位于周期表的第周期,第族。
-
(2) 元素的第一电离能:XY(填“>”或“<”,下同);原子半径:XY。
-
(3)
 的最高价氧化物对应水化物中酸根离子的空间构型(用文字描述)。
的最高价氧化物对应水化物中酸根离子的空间构型(用文字描述)。
-
(4)
 基态核外电子排布式为,用硫氰化钾溶液检验
基态核外电子排布式为,用硫氰化钾溶液检验  的离子方程式为。
的离子方程式为。
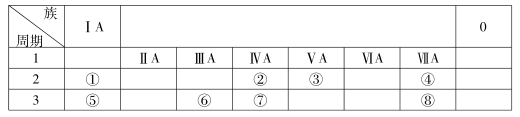
下表为元素周期表的一部分。请参照元素①~⑧在表中的位置,用化学用语回答问题:
-
(1) 画出元素③的原子结构示意图:,它的气态氢化物的化学式为。
-
(2) ①~⑧中,最活泼的金属元素是(写元素符号,下同);最活泼的非金属元素是。
-
(3) ⑦⑧的最高价氧化物对应水化物的酸性由强到弱的顺序是。
-
(4) ④、⑤、⑥三种元素的简单离子半径由大到小的顺序是。
-
(5) ⑥的最高价氧化物与⑤的最高价氧化物对应水化物反应的离子方程式是。
铍(4Be)的右下角元素是铝,根据“对角线规则”,下列描述错误的( )
A . BeO是两性氧化物
B . 已知AlCl3是共价化合物,则BeCl2也可能是共价化合物
C . Be(OH)2既能与H2SO4溶液反应也能与NaOH溶液反应
D . Be(OH)2与NaOH溶液反应后生成NaBeO2和H2O
已知X、Y、Z、W是四种原子序数依次增大的短周期元素,其中只有W是金属。X、Z是人体中含量最高的物质的两种组成元素,Y与Z处于相邻位置。则下列说法中正确的是( )
A . 由W、Y、Z三种元素组成的盐的水溶液一定是中性的
B . X和Y的单质之间的化合反应不需要任何条件即可发生
C . X、Z、W组成的化合物可能不溶于水
D . W的氢氧化物一定是强碱
下列关于元素周期表的说法正确的是( )
A . 能生成碱的金属元素都在ⅠA族
B . 第二周期ⅣA族元素的原子核电荷数和中子数一定为6
C . 稀有气体元素原子的最外层电子数均为8
D . 原子序数为14的元素位于元素周期表的第3周期ⅣA族
元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如表所示。
|
氧族元素 |
8O(氧) |
16S(硫) |
34Se(硒) |
52Te(碲) |
|
单质熔点/℃ |
-218.4 |
113 |
450 |
|
|
单质沸点/℃ |
-183 |
444.6 |
685 |
1390 |
|
元素主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
回答下列问题:
-
(1) 硫元素在元素周期表中位置是,H2S的电子式为,硒原子最外层电子数为。
-
(2) 依据元素周期律和表中知识,预测单质硒的熔点范围可能大于℃,小于℃,元素碲的主要化合价可能有。
-
(3) 从物质类别和硫元素的价态分析,在一定条件下,SO2能与下列物质发生反应,在横线上写出反应产物中含硫物质的化学式:
①NaOH溶液,②H2S,③Na2O2。
-
(4) 已知硒最高价氧化物对应的硒酸是强酸,写出能证明硒酸比碳酸强的离子方程式:。
-
(5) 氢硒酸(H2Se)有较强的还原性,因此露置在空气中长期保存易变质出现浑浊,可能发生反应的化学方程式为。
短周期中8种元素a~h,其原子半径、最高价或最低价随原子序数递增的变化如图所示。下列判断正确的是( )
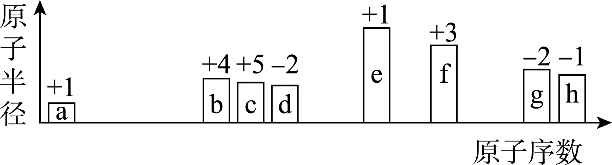
A . a、d、f组成的化合物能溶于氨水
B . e的阳离子与c的阴离子具有相同的电子层结构
C . 简单离子半径: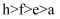 D . 由d和g组成的化合物,其水化物一定是强酸
D . 由d和g组成的化合物,其水化物一定是强酸
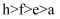 D . 由d和g组成的化合物,其水化物一定是强酸
D . 由d和g组成的化合物,其水化物一定是强酸
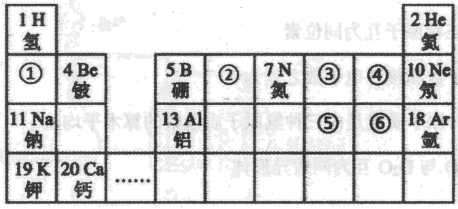
历史上,为了寻求各种元素及其化合物间的内在联系和规律,门捷列夫编制了第一张元素周期表,并在后来的化学发现中使元素周期表变得更完整,有多位化学家也因此获得诺贝尔奖。下列是元素周期表的部分信息:
-
(1) 写出④对应元素的原子结构示意图:。
-
(2) ③④⑤对应原子半径的最大的是,推测⑤⑥对应元素非金属性较强的是(填元素符号)。
-
(3) Ca在元素周期表中的位置为。
-
(4) 第三周期中最高价氧化物对应的水化物碱性最强的是,最简单氢化物稳定性最强的:(填化学式)。
-
(5) “铷(Rb)原子钟”被誉为卫星的“心脏”,已知铷的原子序数为37,最外层电子数为1,写出铷与水反应的化学方程式:。
短周期非金属元素X、Y、Z、W的原子序数依次增大,基态X原子的未成对电子数是其所在周期中最多的,基态W原子的电子总数是其最高能级电子数的4倍。四种元素与Xe元素组成的某化合物的结构如图所示。下列说法错误的是( )
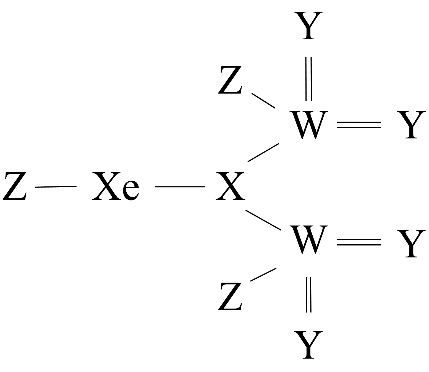
A . W的常见氧化物是酸性氧化物
B . 最简单氢化物的沸点:Z>Y>X
C . 气态氢化物的还原性W> Z
D . X和W的最高价氧化物对应水化物的浓溶液都具有强氧化性
四种短周期元素X、Y、Z和W在元素周期表中的位置如图,X、Y、Z和W原子的最外层电子数之和为24。下列说法错误的是( )
X | Y | |
Z | W |
A . Z位于第三周期第VIA族
B . Y的非金属性比Z的强
C . X的原子半径比Y的大
D . W的含氧酸的酸性比Z的含氧酸的酸性强
最近更新
- It is _____ work of literature that many people are desperat
- 地球公转产生了( ) A、四季变化 B、昼夜现象 C、昼夜的交替 D、太阳的东
- Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32—和Cl2反应的产物之一为SO42—
- 《周礼》载“金有六齐(配方),六分其金而锡居一,谓之钟鼎之齐”。这反映了( ) A.甲骨文的雕刻技巧
- 16. When he realized the police had seen him, the man_____th
- 斜面高0.6 m,倾角为37°,质量是1.0 kg的物体由顶端从静止滑至底端,已知动摩擦因数为μ=0.25,g取10 m
- He was___today, but was asked to stay for___week.A.to have r
- 2010年实现人均国内生产总值比2000年翻一番是我国重要的奋斗目标。国内生产总值与国民生产总值的相同点在于( )
- 图为我国南方某地规划示意图,读图完成下列各题(1)计划修建从a村到b镇的公路,在图中①②两个线路方案中,你认为较为合 理
- 题词“为消灭文盲而斗争”,反映了中国哪一时期的一种“文化”现象。 () A.土地革命时期 B.
- 3.填入下面文段空白处的词语,最恰当的一组是( ) 大量的新诗正散布在我们周围,飘散在日子的深处。 ① 他们与我们的
- 2006年1月30日至2月10日,我国应非洲八国总统的邀请,对喀麦隆、利比里亚、苏丹、赞比亚、纳米比亚、南非、莫桑比克、
- 结合语境,在下面语段中的横线处填写句子最恰当的一项是 起风了,风从沙漠那边来,那苍劲的沙枣,挺起古铜色的躯干,舞动起粗
- 向等物质的量浓度的NaOH和Na2CO3的混合液中加入稀盐酸。下列离子方程式与事实不相符的是( ) A.OH-+CO
- 依次填入下列各句横线上的词语,最恰当的一组是( ) ①以色列空军对巴勒斯坦武装组织连日制造的爆炸事件,采取了____
- 下图为夏季晴朗白天某植物叶片光合作用强度的变化曲线图, 请观察后回答: (1)曲线AB表明光合作用强度随光照增强__
- 阅读下面的内容,完成下面4题 秦且灭六国,兵已临易水。恐其祸至,燕太子丹患之。 樊将军亡秦之燕,太子容之。太傅鞠
- 阅读下面的文言文,完成文后各题。 李通,字次元,南阳宛人也。父守,身长九尺,为人严毅。初事刘歆,为王莽宗卿师。通亦为五威
- 铍元素性质与铝元素性质相似,下列方法能证明氯化铍由共价键构成的是() A.溶于水加硝酸银溶液,观察是否有白色沉淀生成 B
- 保持氧气化学性质的最小粒子是 A.氧分子 B.氧原子 C.氧离子 D.氧气



