碱金属的性质 知识点题库
对于锂、钠、钾、铷、铯五种元素的单质或化合物的说法不正确的是( )
A . 随着电子层数的增加单质的密度逐渐升高
B . 随着核电荷数的增加单质的熔点逐渐降低
C . 在自然界中都只能以化合态形式存在
D . 单质都能与水反应,且反应后的溶液都呈碱性
下列叙述正确的是( )
A . Li在氧气中燃烧能生成Li2O2
B . 将SO2通入过量FeCl3和BaCl2的混合溶液中可生成BaSO4沉淀
C . 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后最终溶液呈红色
D . 将稀硫酸滴加到Fe(NO3)2溶液中无明显现象
下列说法错误的是( )
A . 食物放在冰箱中会减慢食物变质的速率
B . 钾的金属性强,所以钾与水的反应比钠的反应剧烈
C . 2mol SO2与1mol O2混合反应后一定能生成2 mol SO3
D . 面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸
下列叙述正确的是( )
A . Li在氧气中燃烧主要生成Li2O2
B . 将CO2通入次氯酸钙溶液可生成次氯酸
C . 将SO2通入BaCl2溶液可生成BaSO3沉淀
D . 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu
下列对于铯(Cs)的性质的预测中,正确的是( )
A . 它只有一种氧化物Cs2O
B . 它与水剧烈反应
C . Cs+具有很强的氧化性
D . CsHCO3受热不易分解
关于碱金属单质的性质叙述正确的是( )
A . 在空气中燃烧都能生成过氧化物
B . 与盐酸溶液反应时都能生成碱和氢气
C . 熔沸点随原子序数增加而升高
D . 还原性随原子电子层数的增加而增加
某课外活动小组研究金属钾的性质.首先他们通过Na、K原子结构示意图及查找有关资料,知道Na、K属于同一类物质,且知K燃烧生成KO2 . 请完成下列内容:
-
(1) 观察钾的切面.硬度:,颜色:,状态.
-
(2) 预测钾的性质,写出下列反应的化学方程式:
①在空气中缓慢氧化:;
②点燃剧烈燃烧:;
③与水剧烈反应:.
下列关于碱金属、卤素的描述正确的是( )
A . 碱金属在空气中加热均可生成多种氧化物
B . 碱金属与水反应,均浮在水面上.
C . 卤素各单质都能和水剧烈反应.
D . 卤素单质越活泼,其熔沸点就越低
下列有关碱金属的说法不正确的是( )
A . 均为ⅠA族元素,最外层均有1个电子
B . 单质的还原性:Li>Na>K>Rb>Cs
C . 碱性:LiOH<NaOH<KOH<RbOH<CsOH
D . 由Li到Cs,核电荷数依次增加,电子层数、原子半径依次增大
下列关于碱金属、卤族元素的说法正确的是( )
A . 碱金属单质的失电子能力随着原子序数的增加而减小
B . 从上到下,卤素原子的电子层数依次增多,半径依次减小
C . 从F到I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱
D . 碱金属单质都是强氧化剂
碱金属元素和卤族元素广泛存在,用化学用语回答下列问题。
-
(1) 氢氟酸可以用来雕刻玻璃。用电子式表示氟化氢的形成过程。
-
(2) 过氧化钠可以用于潜水艇中氧气的来源,其与二氧化碳反应的化学方程式是。
-
(3) 次氯酸钠溶液(pH>7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是。
-
(4) Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。组装该电池必须在无水、无氧的条件下进行,原因是(用化学方程式表示)。
-
(5) 关于碱金属和卤族元素,下列说法一定正确的是____________。A . 从上到下,单质密度依次增大 B . 从上到下,单质熔沸点依次升高 C . 从上到下,原子半径依次增大 D . 单质都可以与水反应
下列关于铷的叙述正确的是( )
A . 它位于周期表中第4周期
B . 氢氧化铷是弱碱
C . 在钠、钾、铷三种单质中,铷的熔点最高
D . 硝酸铷是离子化合物
下列有关说法不正确的是( )
A . 随着原子序数的递增,碱金属元素单质的密度依次增大、熔点降低
B . 光照下甲烷和氯气混合能发生取代反应,生成的有机物属于烃的衍生物
C . 含 2n 个氢原子的烷烃分子中,所含有的化学键都是单键,且为(3n-2)个
D . 水结成冰,体积膨胀,密度变小的原因与氢键有关
CaCO3→CaO→Ca(OH)2→NaOH的各步反应中,所属反应类型不包括( )
A . 化合反应
B . 分解反应
C . 置换反应
D . 复分解反应
以下关于锂、钠、钾、铷、铯的叙述错误的是( )
①氢氧化物中碱性最强的是CsOH;
②单质熔点最高的是铯;
③与O2反应均可得到多种氧化物;
④它们的密度依次增大;
⑤其单质的还原性依次增强;
⑥它们对应离子的氧化性依次增强;
A . ①⑤
B . ②⑥
C . ②③④⑥
D . ②③④
下列实验中 , 不能观察到明显变化的是( )
A . 把Cl2通入FeCl2溶液中
B . 把绿豆大的钾投入少量水中
C . 把溴水滴加到淀粉KI溶液中
D . 把一段打磨过的铝条放入少量冷水中
借助碱金属和卤族元素性质的递变性分析下面的推断,其中正确的是( )
A . 已知Ca是第四周期第ⅡA族元素,故Ca(OH)2的碱性比Mg(OH)2的碱性弱
B . 已知As是第四周期第ⅤA族元素,故AsH3的稳定性比NH3的稳定性强
C . 已知Cs的原子半径比Na的原子半径大,故Cs与水反应不如Na与水反应剧烈
D . 已知Cl的核电荷数比F的核电荷数多,故Cl的原子半径比F的原子半径大
下列元素不属于碱金属元素的是( )
A . Li
B . Na
C . K
D . Al
类推的思维方式在化学学习与研究中经常采用。以下类推的结论正确的是( )
A . 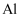 与氢氧化钠溶液反应,故
与氢氧化钠溶液反应,故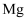 也可以
B . 金刚石的硬度大,则
也可以
B . 金刚石的硬度大,则 的硬度也大
C .
的硬度也大
C . 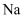 常温下与水剧烈反应,故K常温下也能与水剧烈反应
D .
常温下与水剧烈反应,故K常温下也能与水剧烈反应
D .  与
与 化学式相似,则
化学式相似,则 与
与 的物理性质也相似
的物理性质也相似
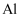 与氢氧化钠溶液反应,故
与氢氧化钠溶液反应,故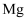 也可以
B . 金刚石的硬度大,则
也可以
B . 金刚石的硬度大,则 的硬度也大
C .
的硬度也大
C . 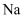 常温下与水剧烈反应,故K常温下也能与水剧烈反应
D .
常温下与水剧烈反应,故K常温下也能与水剧烈反应
D .  与
与 化学式相似,则
化学式相似,则 与
与 的物理性质也相似
的物理性质也相似
下列关于碱金属的性质递变,叙述不正确的是( )
A . 随着核电荷数的递增,单质的还原性越来越强
B . 随着核电荷数的递增,碱金属的单质与水反应的剧烈程度越来越大
C . 随着核电荷数的减小,碱金属的原子半径依次减小
D . 随着核电荷数的递增,碱金属的单质熔点依次升高
最近更新
- 正弦交变电源与电阻、交流电压表、交流电流表按照图1所示的方式连接, =200Ω.图2是交变电源输出电压随时间变化的图象.
- 马明和王群在解这样一道题:“如图,在△ABC中,∠ACB=90°,点D、E在边AB上,AD=AC,BE=BC.求∠DCE
- 下列句子组成语段顺序排列正确的一项是( )(2分) ①这样长而富有变化的墨线是中国画的特点。 ②宋代梁楷《李白行吟图
- 下列图示实验操作中,正确的是() A.粉末
- 下列关于科学研究、实验方法和实验原理的叙述,不正确的是 A.研究红绿色盲的遗传方式应该在患者家系中调查 B.摩尔根等人通
- 如图所示,在水平面上运动的小车内,有一质量为M的物块与两根劲度系数分别为k1、k2的弹簧连接,小车向右以加速度a的大小做
- 金属氧化物的化学式为M2O3,电子总数为50,每个M离子具有10个电子,若其中每个氧原子核内都有8个中子,M2O3的式量
- I wonder why he hasn't __ any of my letters for such a long
- 函数中,自变量x的取值范围是________.
- 已知α为锐角,且tan(α+)=-3,则tanα等于A.2 B.C.
- 以煤为原料可合成重要化工中间体G,其中B与乙酸互为同分异构体,也能与钠反应放出氢气(注:下列图示流程中某些反应条件不一定
- 常温下不能与铝反应的物质是 ( )A.硫酸铜溶液 B.烧碱溶液 C.四氧化三铁 D.
- _____ in the dark, his head hit against a tree. A. Walking
- -----I saw Mr Smith in the office atten yesterday morning.
- ______ at my classmates’ face, I read the sameexcitement in
- (14分)如图所示,质量mA=1kg的小物块以向右VA=4.0m/s的初速度滑上质量mB=1.0kg以向左初速度VB=5
- 人口、资源、环境问题是强国富民安天下的大事,读“我国人口年龄构成比重图”,据此回答各题。据我国第五次人口普查,全国共有1
- 变法维新的呼声早在19世纪60年代初期就已经酝酿,但只有到甲午中日战争以后,它才发展成一场救亡图存的政治运动,其社会条件
- 下列过程中,只发生物理变化的是() A. 湿法炼铜 B. 雕琢玉石 C. 制造轮胎 D. 葡萄酿酒
- 第二节 阅读下面短文,回答文章后面的5个问题。 (E) Most people agree that the direc



