探究碳酸钠与碳酸氢钠的性质 知识点题库
把7.4gNa2CO3·10H2O和NaHCO3组成的混合物溶于水,配成100mL 溶液,其中c(Na+)=0.6mol/L.若把等质量的混合物加热到恒重时,残留物的质量是( )
A . 3.18g
B . 2.21g
C . 5.28g
D . 4.22g
欲进行下列实验,其方案设计合理的是( )
A | B | C | D |
检验装置气密性 | 氨气尾气处理 | NO2被水完全吸收 | 比较NaHCO3和Na2CO3溶解度 |
|
|
|
|
A . A
B . B
C . C
D . D
将一定量的NaOH和NaHCO3的混合物X放在密闭容器中加热,充分反应后生成V1L气体Z(V1=0).反应后的固体残渣Y与过量的稀盐酸反应,又生成V2L气体Z( V1、V2均为标准状况下气体的体积).下列判断错误的是( )
A . V1>V2
B . Z的成分为CO2
C . Y的成分为Na2CO3
D . X中n(Na+)=V2/11.2mol
现有Na2CO3、NaHCO3和NaCl组成的混合物共33.25g,加热到质量不再改变时,称得剩余固体质量为27.05在剩余固体中加入过量盐酸,产生CO2的体积在标准状况下是4.48L,求:
-
(1) 原混合物中三种物质的质量
-
(2) 溶液中Na+的物质的量.
下列有关碳酸钠和碳酸氢钠的说法中,不正确的是( )
A . Na2CO3稳定性大于NaHCO3
B . 相同条件下Na2CO3的溶解度大于NaHCO3
C . 可以用滴加BaCl2溶液的方法,鉴别Na2CO3和NaHCO3溶液
D . 将澄清石灰水分别加入Na2CO3和NaHCO3溶液中,前者产生沉淀,后者无现象
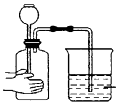
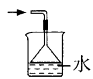
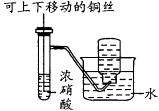
下列图示装置的实验,能达到实验目的的是( )
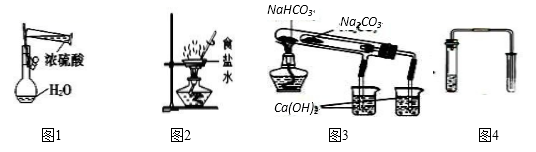
A . 图 1 配制稀硫酸
B . 图 2 食盐水制得食盐晶体
C . 图 3 比较苏打和小苏打的热稳定性
D . 图 4 铜与浓硫酸反应产生 SO2
A,B,C是中学化学常见的三种物质,它们之间的相互转化关系如图所示(部分反应条件及产物略去)。
![]()
-
(1) 若A是一种淡黄色单质固体,则B→C的化学方程式为。
-
(2) 若A是一种黑色单质固体,将一定量C缓慢通入NaOH溶液中,充分反应,测得最后溶液的显碱性,此时溶液的溶质如果是单一成分,可能是、;如果是多种成分,可能是、。
-
(3) 若A是一种活泼金属,C是淡黄色固体,试用化学方程式表示该物质C的一个重要应用。 将C长期露置于空气中,最后将变成物质D,D的化学式为。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为。
向某碳酸钠溶液中逐滴滴加1 mol·L─1的盐酸,测得溶液中Cl─、HCO3─的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2,则下列说法中正确的是()
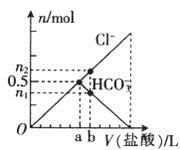
A . Oa段反应的离子方程式与ab段反应的离子方程式相同
B . 该碳酸钠溶液中含有1molNa2CO3
C . b点的数值为0.6
D . b点时生成CO2的物质的量为0.3mol
食品疏松剂在受热时会产生气体,使食品内部形成均匀致密的海绵状多孔组织,让食品酥脆、疏松。下列物质可作为食品疏松剂的是( )
A . 碳酸氢钠
B . 碳酸钠
C . 氢氧化铝
D . 亚硫酸钠
下列关于Na2CO3和NaHCO3性质的说法错误的是( )
A . 热稳定性Na2CO3>NaHCO3
B . 相同温度时,在水中的溶解性:Na2CO3>NaHCO3
C . 与盐酸反应生成CO2速率:Na2CO3>NaHCO3
D . 等物质的量浓度溶液的碱性:Na2CO3>NaHCO3
下列说法错误的是( )
A . 硝化甘油在体内能够分解出大量硝酸,会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛
B . 侯氏制碱法的工艺流程应用了物质溶解度的差异
C . 刚玉、红宝石、蓝宝石的主要成分是氧化铝,而青花瓷、分子筛的主要成分是硅酸盐
D . 生物炼铜法就是利用某种能耐受铜盐毒性的细菌,利用空气中的氧气把不溶性的硫化铜转化为可溶性的铜盐,从而使铜的冶炼变得成本低,污染小,反应条件十分简单
下列有关Na2CO3和NaHCO3性质的说法中,错误的是( )
A . 热稳定性:Na2CO3>NaHCO3
B . 相同温度下,在水中Na2CO3的溶解度大于NaHCO3
C . Na2CO3和NaHCO3均可与澄清石灰水反应
D . 相同质量的Na2CO3和NaHCO3分别与过量盐酸反应,Na2CO3放出CO2多
下列说法正确的是:( )
A . Na2CO3的热稳定性比NaHCO3强
B . Al2O3既是金属氧化物,也是碱性氧化物
C . 氧气和臭氧的相互转化是物理变化
D . 利用过滤法可把Fe(OH)3胶体从FeCl3溶液中分离出来
下列对于实验装置的有关说法错误的是( )
A . 装置Ⅰ:可以用来验证碳的非金属性比硅强 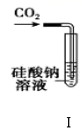 B . 装置Ⅱ:可以用来比较Na2CO3和NaHCO3的热稳定性
B . 装置Ⅱ:可以用来比较Na2CO3和NaHCO3的热稳定性 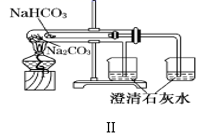 C . 装置Ⅲ:先从①口进气收集满二氧化碳,再从②口进气,则可收集NO气体
C . 装置Ⅲ:先从①口进气收集满二氧化碳,再从②口进气,则可收集NO气体 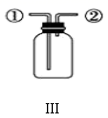 D . 装置Ⅳ:可以用于制备Fe(OH)2并能保证相对较长时间观察到白色沉淀Fe(OH)2
D . 装置Ⅳ:可以用于制备Fe(OH)2并能保证相对较长时间观察到白色沉淀Fe(OH)2 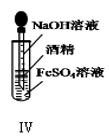
 B . 装置Ⅱ:可以用来比较Na2CO3和NaHCO3的热稳定性
B . 装置Ⅱ:可以用来比较Na2CO3和NaHCO3的热稳定性  C . 装置Ⅲ:先从①口进气收集满二氧化碳,再从②口进气,则可收集NO气体
C . 装置Ⅲ:先从①口进气收集满二氧化碳,再从②口进气,则可收集NO气体  D . 装置Ⅳ:可以用于制备Fe(OH)2并能保证相对较长时间观察到白色沉淀Fe(OH)2
D . 装置Ⅳ:可以用于制备Fe(OH)2并能保证相对较长时间观察到白色沉淀Fe(OH)2 
某化学兴趣小组设计如下装置(棉花球沾有无水硫酸铜粉末),并完成实验。下列说法错误的是( )
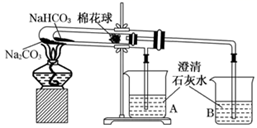
A .  处的温度高于
处的温度高于
 处的温度
B . 加热一段时间后,棉花球处变蓝色
C . 实验结束时,应先熄灭酒精灯,再移开烧杯B
D . 烧杯A中没有出现浑浊,烧杯B中出现浑浊,说明
处的温度
B . 加热一段时间后,棉花球处变蓝色
C . 实验结束时,应先熄灭酒精灯,再移开烧杯B
D . 烧杯A中没有出现浑浊,烧杯B中出现浑浊,说明
 热稳定性比
热稳定性比
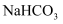 强
强
 处的温度高于
处的温度高于
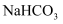 处的温度
B . 加热一段时间后,棉花球处变蓝色
C . 实验结束时,应先熄灭酒精灯,再移开烧杯B
D . 烧杯A中没有出现浑浊,烧杯B中出现浑浊,说明
处的温度
B . 加热一段时间后,棉花球处变蓝色
C . 实验结束时,应先熄灭酒精灯,再移开烧杯B
D . 烧杯A中没有出现浑浊,烧杯B中出现浑浊,说明
 热稳定性比
热稳定性比
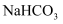 强
强
类比是研究物质性质的常用方法之一。下列类比正确的是( )
A . Cu与Cl2能化合生成CuCl2 , 则Fe与Cl2能化合生成FeCl3
B . Mg在空气中燃烧生成MgO,则Na在空气中燃烧生成Na2O
C . NaHCO3可以治疗胃酸过多,则Na2CO3也可以治疗胃酸过多
D . Na与水反应生成碱和氢气,则红热的铁与水蒸气反应也可以生成碱和氢气
-
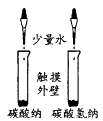
(1) Ⅰ。某校化学课外小组为了鉴别Na2CO3和NaHCO3两种白色固体,用不同的方法做了以下实验,如图所示:
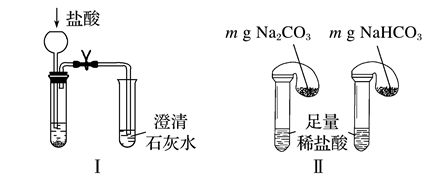
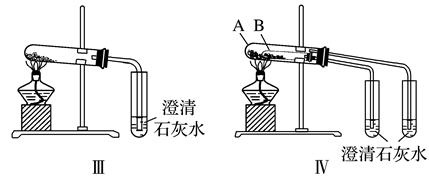
方法Ⅰ中逐滴加入稀盐酸(填“能”或“不能”)鉴别Na2CO3和NaHCO3。
-
(2) 方法Ⅱ能鉴别Na2CO3和NaHCO3的现象是
-
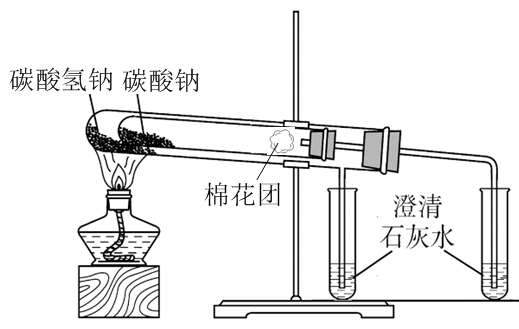
(3) 方法Ⅲ、Ⅳ均能鉴别这两种物质,其中加热试管中发生反应的化学方程式为,与方法Ⅲ相比,方法Ⅳ的优点是(填字母)。
A.Ⅳ比Ⅲ复杂 B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便 D.Ⅳ可以做到用一套装置同时进行两个实验,而Ⅲ不行
-
(4) 若用方法Ⅳ验证Na2CO3和NaHCO3的稳定性,则试管B中装入的固体是(填化学式)。
-
(5) Ⅱ。为进一步探究Na2CO3和NaHCO3的性质,实验小组利用传感器继续做如下实验:
编号
实验操作
实验数据
实验Ⅴ
测量下面实验过程中温度的变化
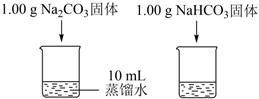
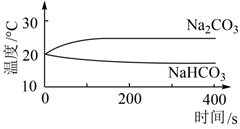
实验Ⅵ
测量下面实验过程中溶液pH的变化
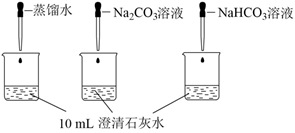
注:Na2CO3溶液和NaHCO3溶液的浓度相等
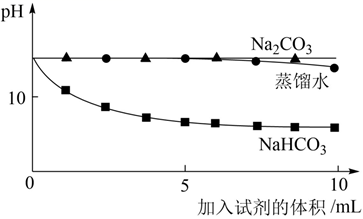
(查阅资料)溶液pH越小,OH-的浓度越小,溶液碱性越弱。
实验Ⅴ中,溶解时吸收热量的物质是(填化学式)。
-
(6) 实验Ⅵ中,Na2CO3溶液和澄清石灰水反应的离子方程式为
OH-未参与该反应的实验证据是
-
(7) 实验Ⅵ中,滴加NaHCO3溶液的烧杯中溶液pH的变化与滴加Na2CO3溶液的pH有明显差异,原因是滴加NaHCO3溶液的烧杯中(填离子符号)参与了反应。
下列实验方案中不能确定试样xNa2CO3yNaHCO3的组成的是( )
A . 取 ag 混合物充分加热,质量减少 bg
B . 取 ag 混合物与足量氢氧化钡溶液充分反应,将所得沉淀洗涤、干燥、称量得到 bg固体
C . 取 ag 混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到 bg 固体
D . 取 ag 混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加 bg
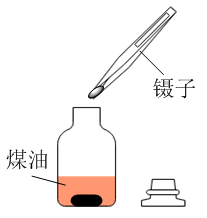
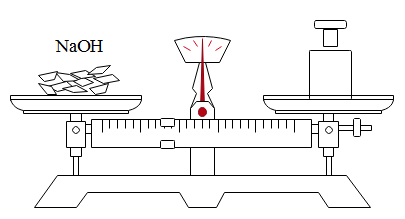
下列实验装置正确的是( )
A | B | C | D |
|
|
|
|
比较 | 将剩余钠块放回原试剂瓶 | 称量NaOH固体 | 向容量转移溶液 |
A . A
B . B
C . C
D . D
下列物质的性质与用途(或储存方法)都正确且有逻辑关系的是( )
A .  溶液与
溶液与 不反应而与HCl能反应生成
不反应而与HCl能反应生成 , 可用饱和
, 可用饱和 溶液除去
溶液除去 中少量HCl气体
B . 碳酸钠和碳酸氢钠均溶于水,可用作食用碱或工业用碱
C . 过氧化钠为碱性氧化物,可用于呼吸面具中吸收二氧化碳
D . 次氯酸见光易分解,所以氯水应保存在钢瓶中
中少量HCl气体
B . 碳酸钠和碳酸氢钠均溶于水,可用作食用碱或工业用碱
C . 过氧化钠为碱性氧化物,可用于呼吸面具中吸收二氧化碳
D . 次氯酸见光易分解,所以氯水应保存在钢瓶中
 溶液与
溶液与 不反应而与HCl能反应生成
不反应而与HCl能反应生成 , 可用饱和
, 可用饱和 溶液除去
溶液除去 中少量HCl气体
B . 碳酸钠和碳酸氢钠均溶于水,可用作食用碱或工业用碱
C . 过氧化钠为碱性氧化物,可用于呼吸面具中吸收二氧化碳
D . 次氯酸见光易分解,所以氯水应保存在钢瓶中
中少量HCl气体
B . 碳酸钠和碳酸氢钠均溶于水,可用作食用碱或工业用碱
C . 过氧化钠为碱性氧化物,可用于呼吸面具中吸收二氧化碳
D . 次氯酸见光易分解,所以氯水应保存在钢瓶中
最近更新
- 罗马以军事扩张立国,它与伽太基进行的长达110多年的争霸战争被称为 A.布匿战争
- 下列加点词语的用法和意义都不同的一项是( ) A.然豫州新败之后,安能抗此难乎? 吾师道也,夫庸知其年之先后生于吾乎
- 碘缺乏症遍及全球,多发生于山区。南美的安第斯山区、欧洲的阿尔卑斯山区和亚洲的喜马拉雅山区是高发病地区。我国云南、河南等1
- 下列生物化学反应能在真核细胞的细胞溶胶中进行的是: A.丙酮酸的无氧分解 B.色盲基因的转录
- 从社会进步和制度创新的角度看,20世纪初期国际社会最重大的事件是 A.第二次工业革命的兴起 B.俄国十月革命的
- 阅读下面一首诗,然后回答下列问题。 与夏十二登岳阳楼 李 白 楼观岳阳尽,川迥洞庭开。 雁引愁心去,山衔好月来。 云间连
- Which sign shows “For the disabled (残疾人) to go through” ?
- Have you ever noticed the colour of the water in a river or
- 在图中画出力F对支点O的力臂,并用字母L表示。
- “十月怀胎,一朝分娩”,在从受精卵到胎儿呱呱坠地前的整个过程中,人的生长发育所需各种营养物质从下列哪项中获取?(
- 在平直的轨道上,甲、乙两车相距为s,同向同时开始运动.甲在后以初速度v1,加速度a1做匀加速运动,乙在前做初速度为零,加
- Ihear someone _______at the door. Please go and see who ____
- 下列关于实验现象的描述中,错误的是A.将红热的细铁丝放在氧气中,剧烈燃烧,火星四射,生成黑色固体B.在空气中点燃镁条.发
- 我国政府要求努力消除制约消费的制度和政策障碍,改善居民消费预期,引导和促进居民扩大消费需求。我国政府这样做的目的在于
- (2012·宁德一模)在构成美利坚民族的最初“原料”中,有一群人被称为“不情愿的移民”。“这群人”主要属于() A.白
- 下列词语中加点的词语读音、字形全都正确的一组是( ) A沉缅(miǎn) 浸渍(zì) 所向披糜 锱(zī)铢必较 B三
- 19世纪末,“六大公司统治着德国化学工业市场,它们组成两大集团……此后不久,又吞并了两大独立的公司。”上述现象的产生,主
- 下图表示北半球中纬度某地连续三天的天气状况,读图回答29~30题 29.11月4日白天云层的主要作用是 A.保温作用
- 有些奇怪的动物会生蛋,但又给它的幼崽喂奶。(lay eggs)
- (05年全国卷Ⅱ)已知点,,.设的平分线与相交于,那么有,其中等于(A) 2(B)(C)-3(D)-
 和
和


