探究铝与酸、碱溶液的反应 知识点题库
下列说法正确的是( )
A . 一定温度和压强下,各种气态物质的体积大小,主要由构成气体的分子大小决定
B . 常温下,铝遇浓硫酸、浓硝酸时会在表面生成致密的氧化膜而发生钝化
C . 氧化铝的熔点很高,可以制耐火坩锅,熔融烧碱样品可以选用此坩锅
D . 氢氧化钠、蔗糖、碳酸、次氯酸、醋酸均为弱电解质
1 L某混合溶液中,溶质X、Y浓度都为0.1mol·L-1 , 向混合溶液中滴加0.1 mol·L-1某溶液Z,所得沉淀的物质的量如图所示,则X、Y、Z分别是( )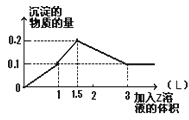
A . 氯化铝、氯化镁、氢氧化钠
B . 偏铝酸钠、氢氧化钡、硫酸
C . 氯化铝、氯化铁、氢氧化钠
D . 偏铝酸钠、氯化钡、硫酸
称取两份铝粉,第一份加足量的NaOH溶液,第二份加足量的盐酸,若放出等量的气体,则两份铝粉的质量比为:( )
A . 1:1
B . 2:3
C . 1:2
D . 1:3
用离子方程式表示下列变化过程
-
(1) 除去铁粉中混有铝粉。
-
(2) 除去二氧化碳中的氯化氢气体。
-
(3) 二氧化硅固体中含有碳酸钙。
-
(4) 盛放氢氧化钠溶液的试剂瓶不用玻璃塞原因。
-
(5) 用稀盐酸清洗铜器皿表面上的铜绿。
在两个烧杯中分别盛有100mL 3.0mol·L-1的盐酸和氢氧化钠溶液,向两个烧杯中分别加入等质量的铝粉,在相同状况下生成的气体的体积比为2∶5,则加入的铝粉的质量为( )
A . 8.10g
B . 5.40g
C . 6.75g
D . 2.70g
下列物质中既能跟稀盐酸反应,又能跟氢氧化钠溶液反应的是( )
① 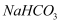 ②
②  ③
③ 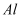 ④
④ 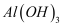 ⑤MgO ⑤Fe(OH) 3 ⑥CuSO4
⑤MgO ⑤Fe(OH) 3 ⑥CuSO4
A . 全部
B . ②③④⑤
C . ①②③④
D . ①②③④⑥
下列元素在自然界中都以化合态存在的是( )
①钠 ②铝 ③铁 ④硅 ⑤氯
A . ①②③
B . ①④⑤
C . ①②③④⑤
D . ①②③④
化学在生活中有着广泛的应用,下列对应关系错误的是( )
| 选项 | 化学性质 | 实际应用 |
| A | NH3具有还原性 | 用作食品工业的制冷剂 |
| B | K2FeO4易与H2O反应生成Fe(OH)3 | 用作水的消毒剂和絮凝剂 |
| C | Ag2O具有氧化性 | 用作银锌纽扣电池正极的活性物质 |
| D | 硫酸铝能与小苏打溶液反应 | 用作泡沫灭火剂原料 |
A . A
B . B
C . C
D . D
下列通过实验观察得到的结论正确的是( )
选项 | 实验操作 | 结论 |
A | AlCl3溶液中逐滴滴加NaOH溶液至过量 | Al(OH)3能溶于强碱溶液 |
B | 铝、镁分别投入相同浓度的NaOH溶液 | 铝比镁更活泼 |
C | 铝箔用酒精灯加热至熔化,轻轻晃动 | 铝单质熔点高 |
D | 铁粉与水蒸气反应后固体加稀HCl溶解,再加KSCN溶液,溶液不变红 | 反应后固体中不含+3价的铁 |
A . A
B . B
C . C
D . D
将某铁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中铁、铝的物质的量之比为( )
A . 3∶2
B . 2∶1
C . 3∶4
D . 4∶3
常温下,取铝热反应后所得固体(含有Al2O3、Fe、Fe2O3等物质)用过量稀硫酸浸出后的溶液,分别向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
A . 加入过量 NaOH 溶液:Na+、AlO2-、OH-、SO42-
B . 加入过量氨水:NH4+、Al3+、OH-、SO42-
C . 加入过量铁粉:Fe3+、H+、Al3+、SO42-
D . 加入过量 NaNO3 溶液:Fe2+、H+、NO3-、SO42-
根据下图的转化关系判断,下列说法正确的是(反应条件已略去)( )
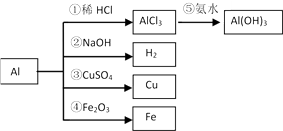
A . 生成等质量H2时,①和②反应消耗n (HCl)=n (NaOH)
B . 反应③中氧化剂与还原剂的物质的量之比为2︰3
C . 反应③和④消耗等量的Al时,生成的n (Cu)︰n (Fe)=3︰2
D . 反应⑤的离子方程式为Al3+ + 3OH-=Al(OH)3↓
有关Al与NaOH溶液反应的说法中,正确的是( )
A . Al是还原剂,NaOH及H2O均是氧化剂
B . 还原产物是H2 , 且由H2O还原所得的H2与由NaOH还原所得的H2物质的量之比为2∶1
C . 此反应说明铝具有两性,铝的活泼性比只具有金属性的金属弱
D . 此反应中,只有H2O是氧化剂,NaOH既不是氧化剂也不是还原剂
金属铝不能用来()
A . 存储酸性溶液
B . 冶炼难熔金属
C . 制电线电缆
D . 制航天材料
在实验室里,要想使AlCl3中的Al3+全部沉淀出来,应选用下列试剂中的( )
A . AgNO3溶液
B . NaOH溶液
C . 石灰水
D . 氨水
铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
-
(1) 铝粉和铁的氧化物(FeO·Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是。
-
(2) NaOH溶液可以除去铝表面的氧化膜,在处理过程中常会产生H2 , 产生H2的离子方程式是。
-
(3) 工业上以铝土矿(Al2O3·H2O)为原料生产铝,主要包括下列过程:
i.将粉粹、筛选后的铝土矿溶解在NaOH溶液中;
ii.加入过量的试剂A使所得溶液中析出Al(OH)3固体;
iii.使Al(OH)3脱水生成Al2O3;
iv.电解熔融Al2O3生成Al。
铝土矿粉粹的目的是,电解熔融Al2O3时,加入冰晶石,其作用是。写出电解熔融Al2O3的化学方程式。
-
(4) 明矾化学式为KAl(SO4)2·12H2O,向明矾溶液中加入Ba(OH)2溶液,当溶液中的SO42-恰好沉淀时,铝元素的存在形式是。
某同学欲检验抗酸药中是否含有Al(OH)3 , 操作如下:取药剂3~4片研碎,向样品中加入过量的盐酸,过滤,得澄清溶液,向澄清溶液中滴加NaOH溶液,观察到有白色沉淀,继续加过量NaOH溶液,白色沉淀又溶解。你能得出该抗酸药中是否含有Al(OH)3?(填含或不含),请写出有关反应的化学方程式:
①
②
③
如图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列选项编号对应的曲线编号错误的是( )
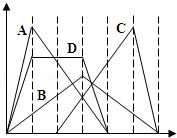
A . 向NaAlO2溶液中逐渐滴入HCl至过量
B . 向澄清石灰水中通入SO2至过量
C . 向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量
D . 向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至过量
下列过程中的化学反应,相应的离子方程式正确的是( )
A . 用碳酸钠溶液处理水垢中的硫酸钙: CO32- +CaSO4 =CaCO3 + SO42-
B . 过量铁粉加入稀硝酸中:Fe + 4H+ + NO3- = Fe3+ +NO↑ +2H2O
C . 硫酸铝溶液中滴如少量氢氧化钾溶液: Al3+ +4 OH- =AlO2- + 2H2O
D . 氯化铜溶液中通入硫化氢: Cu2+ + S2- =CuS ↓
2020年比亚迪汉EV和特斯拉Model3均搭载了磷酸亚铁锂(LiFePO4)电池组。某企业设计了磷酸亚铁锂电池正极生产和回收的工艺流程如图:
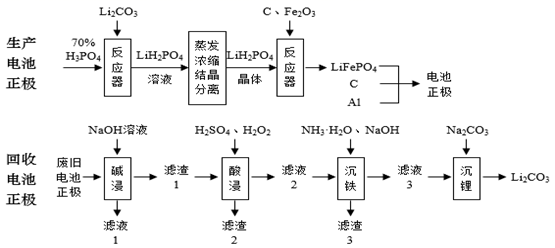
已知:①Ksp[Fe(OH)3]=10-39;②Li2CO3的溶解度:0℃为1.54g,100为0.72g。
-
(1) H3PO4和Li2CO3反应的化学方程式为。
-
(2) 获得LiH2PO4晶体的分离操作是。
-
(3) 写出一条可以提高“碱浸”效率的措施。
-
(4) 向滤液1中加入过量CO2可得到白色胶状物质,该反应的离子方式为。
-
(5) “酸浸”时若用HNO3代替H2O2 , 缺点是,若“沉铁”后溶液中c(Fe3+)=10-6mol·L-1 , 则该过程应调节pH=,“沉锂”时,所得Li2CO3应选择(“冷水”或“热水”)进行洗涤。
最近更新
- 我国饮用矿泉水的基本类别是碳酸水、硅酸水和锶水。此外还有锌、锂、溴、碘及硒矿泉水等,这里的锌、锂、溴、碘、硒是指(
- _____ he’s only been learning English for a year, he speaks
- 对有线性相关关系的两个变量建立的回归直线方程y=a+bx中,回归系数b( )A.可以小于0
- 已知函数 (1)若为奇函数,求的值和此时不等式的解集; (2)若不等式对恒成立,求实数的取值范围.
- 2011年4月11日央视《消费主张》曝光:上海华联等十多家超市多年来出售染色馒头.《食品安全法》规定:食品添加剂要符合食
- 根据句子意思和所给首字母或中文提示,在标有题号的横线上写出一个英语单词的完整、正确形式,使句意通顺。 76. Jones
- 根据下图可以看出农民家庭收入迅速增长,其主要原因是 A、土地改革的完成 B、中共八大路线、方
- There is no doubtthat this candidate’s advantage _____ his
- (1998年上海,20)如图7-13所示是观察水面波衍射的实验装置,AC和BD是两块挡板,AB是一个孔,O是波源,图中已
- During enjoying the Mid-autumn Festival, celebratingthe har
- 下列有关国家的叙述中,正确的是 A.国家是管理社会公共事务的公益机构 B.国家的性质是由生产力的发展水平决定的 C.同一
- 如图,已知抛物线y=x2+3x﹣8的图象与x轴交于A,B两点(点A在点B的右侧),与y轴交于点C. (1)求直线BC的解
- 苯分子不能使酸性高锰酸钾褪色的原因是()A.分子中不存在π键B.分子中存在6电子大π键,结构稳定C.分子是平面结构
- 在负的点电荷的电场中,有a,b,c三点,它们到点电荷的距离,则 A.c点电势比a点电势高 B.
- 内壁光滑,水平放置的玻璃圆环内,有一直径略小于环口径的带正电的小球,以速率v0沿逆时针方向匀速转动,如图所示.若在此空间
- 铜有两种常见的氧化物CuO和Cu2O.某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,
- 中央电视台《同一首歌》栏目准备举办一期以“纪念红军长征胜利结束”为主题的大型晚会,以下四地参与竞争,你认为最合适的城市应
- 阅读下面文言文,回答8―11题 司马芝字子华,河内温人也。少为书生,避乱荆州,于鲁阳山遇贼,同行者皆弃老弱走,芝独坐守老
- When I tidied up(整理)some old boxes under my bed, I found an
- 2012年继续大幅度增加“三农”投入,巩固完善强化强农惠农政策,切实做到财政支出重点向农业农村倾斜,确保用于农业农村的总



