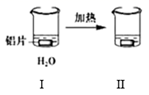
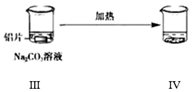
铝的化学性质 知识点题库
化学与生活密切相关,下列说法不正确的是( )
A . 为了防止食品受潮变质,常在食品包装袋中放入生石灰
B . 不可用铝制餐具长时间存放酸性或碱性食物
C . 光化学烟雾与氮氧化合物和碳氢化合物的大量排放有关
D . 为防止铁制品生锈,可以在铁制品的外层涂油漆或局部镀铜
把铝粉和某铁的氧化物(xFeO•yFe2O3)粉末配成铝热剂,分成两等份.一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应.前后两种情况下生成的气体质量比是5:7,则x:y为( )
A . 1:1
B . 1:2
C . 5:7
D . 7:5
常温下能用铝制容器盛放的是( )
A . 稀硫酸
B . 氢氧化钠溶液
C . 浓硫酸
D . 硫酸铜溶液
给定条件下,下列选项中所示的物质间转化均能通过一步反应实现的是( )
A . 0.1 mol•L﹣1 HCl  Cl2
Cl2 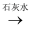 Ca(ClO)2(aq)
B . Al3+
Ca(ClO)2(aq)
B . Al3+ 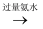 AlO2﹣
AlO2﹣  Al(OH)3
C . Al
Al(OH)3
C . Al  NaAlO2(aq)
NaAlO2(aq)  NaAlO2(s)
D . MgO(s)
NaAlO2(s)
D . MgO(s)  Mg(NO3)2(aq)
Mg(NO3)2(aq)  Mg(s)
Mg(s)
 Cl2
Cl2 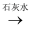 Ca(ClO)2(aq)
B . Al3+
Ca(ClO)2(aq)
B . Al3+ 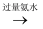 AlO2﹣
AlO2﹣  Al(OH)3
C . Al
Al(OH)3
C . Al  NaAlO2(aq)
NaAlO2(aq)  NaAlO2(s)
D . MgO(s)
NaAlO2(s)
D . MgO(s)  Mg(NO3)2(aq)
Mg(NO3)2(aq)  Mg(s)
Mg(s)
以Al2O3为原料制取氢氧化铝,最好的方法是( )
A . 将Al2O3溶于水
B . 将Al2O3先溶于盐酸中,之后滴加氢氧化钠溶液
C . 将Al2O3先溶于盐酸中,之后滴加氨水
D . 将Al2O3先溶于NaOH溶液中,之后再滴加盐酸
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | Na2O2能与二氧化碳、水反应放出O2 | Na2O2可用作呼吸面具的供氧剂 |
B | 铝比铁活泼 | 铝比铁更容易被腐蚀 |
C | 钠与水反应是放热反应 | 与水反应时,钠浮在水面上 |
D | 晶体硅熔点高硬度大 | 可用于制作半导体材料 |
A . A
B . B
C . C
D . D
根据下列实验现象,所得结论正确的是( )
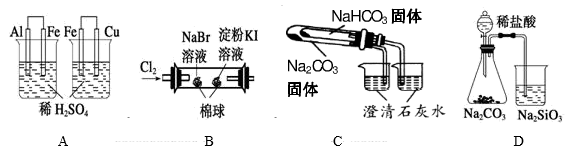
| 实验 | 实验现象 | 结论 |
| A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 氧化性:Al3+>Fe2+>Cu2+ |
| B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 右烧杯中澄清石灰水变浑浊,左边烧杯中无明显变化 | 热稳定性:Na2CO3>NaHCO3 |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
A . A
B . B
C . C
D . D
某化学小组的同学取一定量的Al和Fe2O3的混合物进行铝热反应,并探究熔落物的成分。请回答下列问题:
-
(1) Ⅰ.引发铝热反应的实验操作是
-
(2) 做铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是
-
(3) 反应的化学方程式为
-
(4) Ⅱ.已知:Al、Fe的熔、沸点数据如下:
物质
Al
Fe
熔点(℃)
660
1 535
沸点(℃)
2 467
2 750
某同学猜测,铝热反应所得到的熔落物是铁铝合金。理由:该反应放热能使铁熔化,而铝的熔点比铁低,所以铁和铝能形成合金。你认为他的解释是否合理?(填“合理”或“不合理”)。设计一个简单的实验方案,证明上述所得的熔落物中含有金属铝:
下列各组离子,在指定的环境中一定能大量共存的是( )
A . 某无色透明溶液中:NH4+、Ca2+、Cl-、CO32-
B . 与金属铝反应放出氢气的溶液:K+、NH4+、NO3-、Cl-
C . 滴加酚酞试液显红色的溶液:K+、Na+、CO32-、Cl-
D . c(Fe2+)=1mol/L的溶液:K+、NH4+、MnO4-、SO42-
下列反应没有氢气生成的是( )
A . 单质钠投入水中
B . 铝投入到氢氧化钠溶液中
C . 氧化钠投入水中
D . 往铁粉中通入水蒸气,并高温加热
金属及其化合物的转化关系是化学学习的重要内容之一。下列各组物质的各步转化关系中不能通过一步反应完成的是( )
A . Na→NaOH→Na2CO3
B . Fe→Fe(NO3)3→Fe(OH)3
C . Al→Al2O3→Al(OH)3
D . Mg→MgCl2→Mg(OH)2
将一定量的Mg、Al混合物投入200mL某浓度的盐酸中,金属完全溶解后,再逐滴加入2mol L-1的NaOH溶液至过量,所生成的沉淀与所加NaOH的关系如图所示。
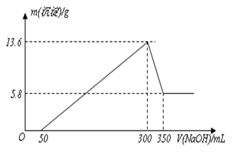
-
(1) 0~50mL段内,发生反应的离子方程式为。
-
(2) 300~350mL段内,发生反应的离子方程式为。
-
(3) 试计算该盐酸的浓度。(写出必要的计算过程)
从铝土矿(主要成分为Al2O3 , 还有少量杂质)中提取铝的工艺流程及步骤如下:
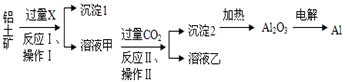
试回答下列问题:
-
(1) 试剂X为;
-
(2) 写出试剂X溶解Al2O3的化学方程式
-
(3) 操作Ⅰ、操作Ⅱ均为(填操作名称);
-
(4) 金属铝与氧化铁混合在高温下,会发生剧烈的反应,该反应的化学方程式为;
-
(5) 反应Ⅱ的离子方程式为;
-
(6) 电解熔融氧化铝制取金属铝,若有0.6 mol电子发生转移,理论上能得到金属铝的质量是g。
在含有Fe2+、Fe3+、Al3+、NH4+的溶液中加入足量的Na2O2固体,再加入过量的稀盐酸,完全反应后,离子数目几乎没有改变的是( )
A . Fe2+
B . Fe3+
C . Al3+
D . NH4+
下列指定反应的离子方程式正确的是( )
A . 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
B . 用铝粉和NaOH溶液反应制取少量H2:Al+2OH−=  +H2↑
C . 室温下用稀HNO3溶解铜:Cu+2
+H2↑
C . 室温下用稀HNO3溶解铜:Cu+2  +2H+=Cu2++2NO2↑+H2O
D . NaHCO3溶液与足量的NaOH溶液混合:
+2H+=Cu2++2NO2↑+H2O
D . NaHCO3溶液与足量的NaOH溶液混合:  +OH-=
+OH-=  +H2O
+H2O
 +H2↑
C . 室温下用稀HNO3溶解铜:Cu+2
+H2↑
C . 室温下用稀HNO3溶解铜:Cu+2  +2H+=Cu2++2NO2↑+H2O
D . NaHCO3溶液与足量的NaOH溶液混合:
+2H+=Cu2++2NO2↑+H2O
D . NaHCO3溶液与足量的NaOH溶液混合:  +OH-=
+OH-=  +H2O
+H2O
探究铝片与  溶液的反应。
溶液的反应。
 溶液的反应。
溶液的反应。 | | | |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验主要为 |
下列说法错误的是( )
A .  溶液中存在水解平衡:
溶液中存在水解平衡: 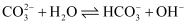 B . 对比Ⅰ、Ⅲ,说明
B . 对比Ⅰ、Ⅲ,说明  溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为:
溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为: 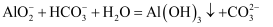 D . 加热及
D . 加热及  逸出对
逸出对  水解平衡移动方向的影响是相反的
水解平衡移动方向的影响是相反的
 溶液中存在水解平衡:
溶液中存在水解平衡: 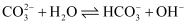 B . 对比Ⅰ、Ⅲ,说明
B . 对比Ⅰ、Ⅲ,说明  溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为:
溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为: 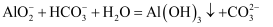 D . 加热及
D . 加热及  逸出对
逸出对  水解平衡移动方向的影响是相反的
水解平衡移动方向的影响是相反的
将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1 , 该溶液中溶质质量分数为( )
A . 82a/(46a+m)%
B . 8200a/(46a+2m) %
C . 8200a/(46a+m)%
D . 8200a/(69a+m) %
下列说法正确的是( )
A . 石墨转化为金刚石是化学变化
B . 常温下,铁、铝与浓硫酸不发生反应
C . 标准状况下,2.24LNO2中含有的氧原子的数目为0.2NA
D . 向硫酸铵溶液中加入氢氧化钡溶液。发生反应的离子方程式为Ba2++ =BaSO4↓
=BaSO4↓
 =BaSO4↓
=BaSO4↓
关于浓盐酸、浓硝酸、浓硫酸的说法中,正确的是( )
A . 都是含氧酸
B . 都具有氧化性
C . 都盛放在棕色瓶中贮存
D . 室温下都能与金属铝发生钝化反应
以下化学反应的产物与反应条件、反应物的浓度或者用量有关的是( )
A . AlCl3溶液中滴入NaOH溶液
B . Cu与硝酸反应
C . H2与Cl2反应
D . NaHCO3与盐酸反应
最近更新
- ----What’s the noise? ----Oh, my neighbour’s house ________
- 下列变化中,属于化学变化的是() A. 胆矾研碎 B. 品红扩散 C. 酚酞变红 D. 干冰升华
- 质量为m1和m2的两个物体,由静止从同一高度下落,运动中所受的空气阻力分别是F1和F2.如果发现质量为m1的物体先落地,
- 蓝藻属于自养型生物是因为 (
- 设Sn是等差数列{an}前n项和,且S10=110,a10-a6=8,Cn=.(1)求数列{Cn}的通项公式;(2)设f
- 下列物质不能跟金属钠反应的是 ( ) A.甲醇 B.乙醚 C.福尔马林 D.乙二醇
- Why do people buy art? To answer this question, ask yourself
- 燃烧法是测定有机物化学式的一种重要方法,现在完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸和浓氢氧化钠溶液,实验结束后
- 有一些部门和地方,电子政务的要领概念常被“简单化”,官方网站既无必要的经费,也无专门的技术维护人员,网站“一建了之”“长
- 溶液、胶体和浊液这三种分散系的根本区别是 A.是否是大量分子或离子的集合体 B
- (共5小题;每小题2 分,满分10 分) 根据短文内容,从短文后的选项中选出能填入空白处的最佳选项。选项中有
- 隋朝大运河,连接淮河和长江的一段是( ) A.永济渠 B.江南河 C.通济渠 D.
- “有志者事竟成,破釜沉舟百二秦关终属楚;苦心人天不负,卧薪尝胆三千越甲可吞吴。”此对联所涉及的历史事件分别发生在(
- 已知函数,则该函数是()A. 非奇非偶函数,且单调递增 B. 偶函数,且单调递减 C. 奇函数,且单调递增 D. 奇函数
- (1)将0.15 mol·L-1稀硫酸V1 mL与0.1 mol·L-1NaOH溶液V2 mL混合,所得溶液的pH为1,
- 探究不同的生态因素对鼠妇生活的影响就是利用动物的行为来获得结果的,这种探究使用的研究方法最好是( ) A.查阅资料法
- 首先发现通电导线周围存在磁场的物理学家是( ) A.安培 B.法拉第 C.
- 抗战老兵张步风回忆说:“在正太铁路附近,到底割了多少次电线,拔了多少根电杆,拆毁了多少铁轨,在公路上挖了多少个大坑,现在
- 下列图像中,能正确反映对应变化关系的是A.向一定量的二氧化锰中加入过氧化氢溶液 B.加热一定量的 高锰酸钾固体 C.向一
- 下列熟语中有错别字的一项是 A.上梁不正下梁歪 识时务者为俊杰 死马当做活马医 一个鼻孔出气