氧化还原反应的电子转移数目计算 知识点题库
请将下列反应的双线桥写出
-
(1) 8H++2NO3﹣+3Cu=Cu 2++2NO↑+4H2O
-
(2) KClO3+6HCl=KCl+3Cl2↑+3H2O.
用CH4催化还原NOx可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1
下列说法不正确的是( )
A . 若用标准状况下4.48 L CH4还原NO2生成N2和水蒸气,放出的热量为173.4 kJ
B . 由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) ΔH>-574 kJ/mol
C . 反应①②转移的电子数相同
D . 反应②中当0.2 mol CH4反应完全时转移的电子总数为1.60 mol
-
(1) 在盛有淀粉KI溶液(用H2SO4酸化)的试管中,滴加少量的次氯酸钠溶液,会立即看到溶液变成蓝色,相应的离子方程式为。在盛有淀粉和碘形成的蓝色溶液中,滴加Na2SO3溶液,又发现蓝色溶液逐渐消失,相应的离子方程式为。对比上述两组实验所得结果,可得出ClO-、I2、SO42-的氧化性由强到弱的顺序为 。
-
(2) 氯酸是一种强酸,氯酸的浓度超过40%,就会迅速分解,产生比它的酸性更强的酸,同时放出气体,该气体混合物经干燥后,平均分子量为47.6,它可以使带火星的木条复燃,并可使润湿的淀粉一碘化钾试纸变蓝。试完成下列各题:
(a)该气体的组成是,气体混合物中各成分的物质的量比为。
(b)写出氯酸分解的化学反应方程式,该反应的氧化产物是(写化学式)。
电解饱和食盐水,当阴极附近有0.8molNaOH生成时,导线中通过电子的物质的量是( )
A . 0.16mol
B . 0.2mol
C . 0.4mol
D . 0.8 mol
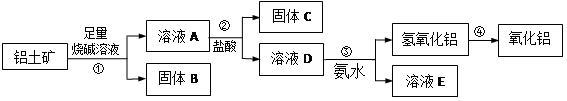
某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是Al2O3 , 杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
-
(1) 固体B的主要用途为(只写一种即可);
-
(2) 第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是:、;
-
(3) 第③步中,生成氢氧化铝的离子方程式是。若往A溶液中通入足量CO2 , 产生的沉淀为(填化学式);
-
(4) 工业上制取AlCl3常用Al2O3与C、Cl2在高温条件下反应,已知每消耗0.5mol碳单质,转移1mol电子,则该反应的氧化产物为(填化学式)。
NA代表阿伏加德罗常数的值,下列叙述正确的是( )
A . 0.1mol 熔融的 NaHSO4 中含有的离子总数为 0.3 NA
B . 标准状况下,2.24L HF和NH3分子所含电子数目均为NA
C . 常温时,56gAl与足量浓硝酸反应,转移的电子数目为3NA
D . 向含有 1mol FeI2 溶质的溶液中通入适量的氯气,当有 1molFe2+被氧化时,该反应转移电子的数目为 3NA
还原沉淀法是处理含铬(含Cr2O 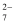 和CrO
和CrO  )工业废水的常用方法,过程如下:
)工业废水的常用方法,过程如下:
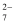 和CrO
和CrO  )工业废水的常用方法,过程如下:
)工业废水的常用方法,过程如下:
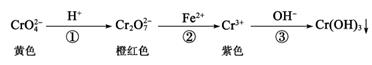
已知:转化过程中的反应为2CrO  (aq) +2H+(aq)
(aq) +2H+(aq)  Cr2O
Cr2O 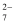 (aq)+H2O(I)。常温下Ksp[Cr(OH)3]=1×10-32。下列说法错误的是( )
(aq)+H2O(I)。常温下Ksp[Cr(OH)3]=1×10-32。下列说法错误的是( )
A . 反应①v正(CrO  ) =2v逆(Cr2O
) =2v逆(Cr2O 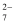 ) 时,反应处于平衡状态
B . 反应②转移0.6mole- , 则有0.2molCr2O
) 时,反应处于平衡状态
B . 反应②转移0.6mole- , 则有0.2molCr2O 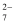 被还原
C . 除去废水中含铬离子的过程包括氧化还原反应和复分解反应
D . 常温下, 要使处理后废水中的c(Cr3+) 降至1×10-5mol·L-1 , 反应③应调溶液pH=5
被还原
C . 除去废水中含铬离子的过程包括氧化还原反应和复分解反应
D . 常温下, 要使处理后废水中的c(Cr3+) 降至1×10-5mol·L-1 , 反应③应调溶液pH=5
 ) =2v逆(Cr2O
) =2v逆(Cr2O 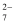 ) 时,反应处于平衡状态
B . 反应②转移0.6mole- , 则有0.2molCr2O
) 时,反应处于平衡状态
B . 反应②转移0.6mole- , 则有0.2molCr2O 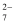 被还原
C . 除去废水中含铬离子的过程包括氧化还原反应和复分解反应
D . 常温下, 要使处理后废水中的c(Cr3+) 降至1×10-5mol·L-1 , 反应③应调溶液pH=5
被还原
C . 除去废水中含铬离子的过程包括氧化还原反应和复分解反应
D . 常温下, 要使处理后废水中的c(Cr3+) 降至1×10-5mol·L-1 , 反应③应调溶液pH=5
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 1mol单质Fe与足量的高温水蒸气反应,失去3NA个电子
B . 50mll2mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA
C . 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA
D . 27g铝中加入1L 1 mol/L  NaOH溶液,转移电子数是3NA
NaOH溶液,转移电子数是3NA
用双线桥标出电子转移的方向和数目,并指出氧化剂和还原剂,氧化产物和还原产物。
Fe2O3+3CO  2Fe+3CO2。
2Fe+3CO2。
氧化剂:;还原剂:;氧化产物:;还原产物:;用双线桥标出电子转移的方向和数目:。
钒元素在酸性溶液中有多种存在形式,其中VO2+为蓝色,VO 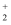 为淡黄色,VO
为淡黄色,VO 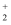 具有较强的氧化性,浓盐酸能把VO
具有较强的氧化性,浓盐酸能把VO 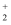 还原为VO2+。向VOSO4溶液中滴加酸性KMnO4溶液,溶液颜色由蓝色变为淡黄色。下列说法正确的是( )
还原为VO2+。向VOSO4溶液中滴加酸性KMnO4溶液,溶液颜色由蓝色变为淡黄色。下列说法正确的是( )
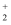 为淡黄色,VO
为淡黄色,VO 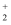 具有较强的氧化性,浓盐酸能把VO
具有较强的氧化性,浓盐酸能把VO 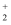 还原为VO2+。向VOSO4溶液中滴加酸性KMnO4溶液,溶液颜色由蓝色变为淡黄色。下列说法正确的是( )
还原为VO2+。向VOSO4溶液中滴加酸性KMnO4溶液,溶液颜色由蓝色变为淡黄色。下列说法正确的是( )
A . 在酸性溶液中氧化性:VO 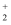 >
>  >Cl2
B . 向酸性(VO2)2SO4溶液中滴加Na2SO3溶液,溶液由淡黄色变为蓝色
C . 向0.1molKMnO4的酸性溶液中滴加1molVOSO4溶液,转移电子为1mol
D . 浓盐酸还原VO2+的离子方程式为2VO
>Cl2
B . 向酸性(VO2)2SO4溶液中滴加Na2SO3溶液,溶液由淡黄色变为蓝色
C . 向0.1molKMnO4的酸性溶液中滴加1molVOSO4溶液,转移电子为1mol
D . 浓盐酸还原VO2+的离子方程式为2VO 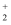 +4H++2Cl-=2VO2++Cl2↑+2H2O
+4H++2Cl-=2VO2++Cl2↑+2H2O
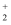 >
>  >Cl2
B . 向酸性(VO2)2SO4溶液中滴加Na2SO3溶液,溶液由淡黄色变为蓝色
C . 向0.1molKMnO4的酸性溶液中滴加1molVOSO4溶液,转移电子为1mol
D . 浓盐酸还原VO2+的离子方程式为2VO
>Cl2
B . 向酸性(VO2)2SO4溶液中滴加Na2SO3溶液,溶液由淡黄色变为蓝色
C . 向0.1molKMnO4的酸性溶液中滴加1molVOSO4溶液,转移电子为1mol
D . 浓盐酸还原VO2+的离子方程式为2VO 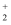 +4H++2Cl-=2VO2++Cl2↑+2H2O
+4H++2Cl-=2VO2++Cl2↑+2H2O
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 1mol/LFe(NO3)2溶液中,NO  的数目是2NA
B . 反应4FeS2+11O2
的数目是2NA
B . 反应4FeS2+11O2  2Fe2O3+8SO2 , 每生成1molFe2O3转移电子数目22NA
C . 标准状况下,2.24LNO2溶于足量水中充分反应,转移电子数0.1NA
D . 密闭容器中,2molSO2与2molO2充分反应,容器中分子总数为3NA
2Fe2O3+8SO2 , 每生成1molFe2O3转移电子数目22NA
C . 标准状况下,2.24LNO2溶于足量水中充分反应,转移电子数0.1NA
D . 密闭容器中,2molSO2与2molO2充分反应,容器中分子总数为3NA
 的数目是2NA
B . 反应4FeS2+11O2
的数目是2NA
B . 反应4FeS2+11O2  2Fe2O3+8SO2 , 每生成1molFe2O3转移电子数目22NA
C . 标准状况下,2.24LNO2溶于足量水中充分反应,转移电子数0.1NA
D . 密闭容器中,2molSO2与2molO2充分反应,容器中分子总数为3NA
2Fe2O3+8SO2 , 每生成1molFe2O3转移电子数目22NA
C . 标准状况下,2.24LNO2溶于足量水中充分反应,转移电子数0.1NA
D . 密闭容器中,2molSO2与2molO2充分反应,容器中分子总数为3NA
第十三届全国人民代表大会第四次会议政府工作报告指出“要扎实做好碳达峰、碳中和各项工作”,绿色氢能和液态阳光甲醇可助力完成碳中和目标。下列说法正确的是( )
A .  属于电解质
B . 用焦炭与
属于电解质
B . 用焦炭与  反应是未来较好获取氢能的方法
C .
反应是未来较好获取氢能的方法
C .  与
与  反应,每生成1mol
反应,每生成1mol  时转移4mol电子
D . 植树造林、节能减排等有利于实现碳中和
时转移4mol电子
D . 植树造林、节能减排等有利于实现碳中和
 属于电解质
B . 用焦炭与
属于电解质
B . 用焦炭与  反应是未来较好获取氢能的方法
C .
反应是未来较好获取氢能的方法
C .  与
与  反应,每生成1mol
反应,每生成1mol  时转移4mol电子
D . 植树造林、节能减排等有利于实现碳中和
时转移4mol电子
D . 植树造林、节能减排等有利于实现碳中和
NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 12g石墨中含有C-C键的数目为2NA
B . 标准状况下(STP),2.24LCHCl3中含有σ键的数目为0.4NA
C . 常温下,1L0.1mol·L-1HF(Ka=8.1×10-4)溶液中所含H+的数目约为9×10-3NA
D . 5.6gFe发生吸氧腐蚀,最终生成Fe2O3·xH2O,电极之间转移的电子数为0.3NA
下列用单、双线桥表示电子转移的方向和数目错误的是( )
A . 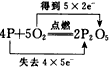 B .
B . 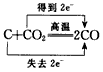 C .
C . 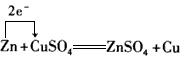 D .
D . 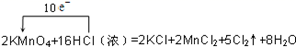
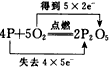 B .
B .  C .
C . 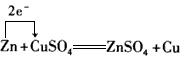 D .
D .
判断下列反应中,电子转移方法错误的是( )
A .  B .
B . 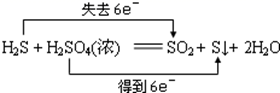 C .
C . 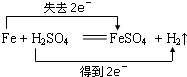 D .
D . 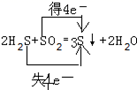
 B .
B .  C .
C .  D .
D . 
含氰化物的废液乱倒或与酸混合,均易生成有剧毒且易挥发的氰化氢。工业上常采用碱性氯化法来处理高浓度氰化物污水,发生的主要反应为:CN-+OH-+Cl2→CO2+N2+Cl-+H2O(未配平)。下列说法错误的是(其中NA表示阿伏加德罗常数的值)( )
A . Cl2是氧化剂,CO2和N2是氧化产物
B . 上述离子方程式配平后,氧化剂、还原剂的化学计量数之比为2:5
C . 该反应中,若有1molCN-发生反应,则有5NA电子发生转移
D . 若将该反应设计成原电池,则CN-在负极区发生反应
二氧化氯(ClO2)是国际上公认的安全、无毒、绿色消毒剂和去污剂,可用于饮用水和环境的消毒杀菌处理,可以除去水体或环境中的氰化物污染等,除去氰化物污染的反应原理2ClO2+2CN-=2CO2+N2+2Cl-。下列关于该反应的说法错误的是( )
A . 氧化剂只有ClO2
B . 氧化剂与还原剂的物质的量之比为1:1
C . 氧化产物只有CO2
D . 转移1 mol电子时,理论上生成6.72L(标准状况)气体
如图,甲是氢氧燃料电池示意图,a为正极;乙是惰性电极电解足量CuSO4溶液的示意图,电解时c电极上有红色固体物质析出。
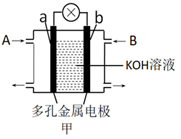
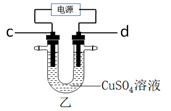
回答下列问题:
-
(1) 图甲中,从A口通入的气体是,b电极的电极反应式为。
-
(2) 图乙中,c电极通过导线与电源的极相连;理论上当c电极析出3.20g红色固体时,则d电极表面产生的气体在标准状况下的体积为mL。
纳米铁(直径一般从几纳米到几十纳米)可通过不同反应机制(吸附、还原、催化氧化)去除环境有机、无机污染物,通过番石榴叶提取液还原Fe3+制备纳米铁(Fe0)氧化去除As(Ⅲ)(罗马数字为元素的化合价)的过程如图所示。下列叙述不正确的是( )
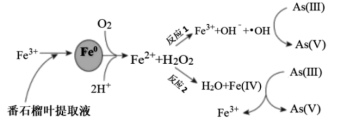
A . 将纳米铁与水形成分散系,可以发生丁达尔效应
B . 反应1的前半程,1 mol H2O2反应转移2 mol电子
C . 反应2中,Fe2+与H2O2的物质的量之比为1:1
D . 若要氧化去除1 mol As(Ⅲ),则至少需要112 g纳米铁
NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A . 标准状况下,22.4L CO2中共用电子对数目为2 NA
B . 标准状况下,46g NO2与N2O4的混合物中所含的原子总数目为3NA
C . 100g质量分数为49%的硫酸溶液,含有的氧原子数目为2NA
D . 一定条件下 ,0.2mol SO2与0.1mol O2充分反应后转移电子总数为0.4 NA
最近更新
- 设函数的定义域为集合,函数 的定义域为集合。 求: ⑴,; ⑵,。
- 《论语·学而》:“君子务本,本立而道生,孝弟也者,其为仁为本欤。”由此,可见孔子仁的学说的逻辑起点是( ) A.人
- 小明同学在实验室用大理石和稀盐酸反应制取二氧化碳完毕后,对废液中溶质的成分产生了兴趣。请你一同参与探究并回答下列问题:
- 9西方学者查尔斯·默里在《文明的解析》一书中以下图表示公元600~1800年中国绘画的发展状况,约每200年间出现一个高
- 某同学做“探究凸透镜成像规律”的实验,当他把蜡烛移到距离透镜36 cm的地方时,在光屏上观察到如图2-2-14所示的像,
- 读下列“历届联大讨论恢复中国在联合国的合法权利支持中国票数增长示意图”,对这一增长结果解读错误的是
- 已知函数f(x)=x(a+lnx),g(x)=(Ⅰ)若函数f(x)的最小值为,求实数a的值;(Ⅱ)当a>0,x>0时,求
- 设原命题为:“若空间两个向量与()共线,则存在实数,使得”则其逆命题、否命题、逆否命题为真的个数( ) A.1
- 3. The train had not come yet and the man ______ his watch a
- 电动自行车已成为大众化的一种交通工具,小乔对家里的电动自行车进行了测试,他骑车在平直的路面上由静止开始运动,获得如图所示
- — Can I help you? — Do you have any of Michael Jackson's CD
- 再宿武关 李涉① 远别秦城②万里游,乱山高下出商州。 关门不锁寒溪水。 一夜潺湲③送客愁。 【注】①李涉,唐宪宗至文
- 为了尽快适应新的学习生活,你认为合理的方法是 ①调整心态
- 如下图是一种水位自动报警器的原理示意图,当水位达到金属块A时,出现的情况是A.绿灯亮 B.红灯亮
- 近年来,随着我国经济从卖方市场转为买方市场,许多企典根据市场需求变化,积极开发和研制新产品,取得了良好的经济效益,但也有
- .“铁券”(图1)民间俗称“免死牌”,是封建帝王颁发给 功臣、重臣的一种带有奖赏和盟约性质的凭证。关于这种 现象出现的说
- 读下图,太平天国运动后期,太平军和清军争夺的重点是
- 长方体的共顶点的三个侧面面积分别为3,5,15,则它的体积为_____________.
- 网络中有一款风靡至今的虚拟游戏“开心农场”。如今,很多城里的人到周围农村租田种地,“开心农场”在现实中已经成为现实。结合
- 文化创造要“站在前人的肩膀上”,这表明() A.教育在文化传承中发挥重要作用 B.没有文化创造就不会有文化继承 C.没有



