离子方程式的书写 知识点题库
下列反应的离子方程式书写正确的是( )
A . 铁粉与稀盐酸的反应:Fe+2H+═Fe2++H2↑
B . 硫酸铝溶液与氨水的反应:Al3++3OH﹣═Al(OH)3↓
C . 氢氧化铜与稀硫酸的反应:OH﹣+H+═H2O
D . 钠与水的反应:Na+2H2O═Na++2OH﹣+H2↑
下列反应的离子方程式书写正确的是( )
A . 氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu
B . 稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑
C . 碳酸钙与盐酸反应:2H++CO32﹣=H2O+CO2↑
D . 氢氧化钡溶液与稀硫酸反应:Ba2++SO42﹣=BaSO4↓
下列反应的离子方程式正确的是( )
A . 用KIO3 氧化酸性溶液中的KI:5I﹣+IO3﹣+3H2O═3I2+6OH﹣
B . 向Ca(ClO)2溶液中通入过量CO2制次氯酸:ClO﹣+H2O+CO2═HClO+HCO3﹣
C . 向酸性KMnO 4溶液中滴入H 2O2:2MnO 4﹣+6H++3H2O2═2Mn 2++4O2↑+6H2O
D . 用Cl2与石灰乳反应制漂白粉:Cl2+2OH﹣═Cl﹣+ClO﹣+H2O
下列表示对应化学反应的离子方程式正确的是 ( )
A . 向稀HNO3中滴加Na2SO3溶液: SO32-+2H+=SO2↑+H2O
B . 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O=H2SiO3↓+SO32-
C . 向Al2(SO4)3溶液中加入过量的NH3·H2O: Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D . 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑
能正确表示下列反应的离子方程式是( )
A . Fe3O4 溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O
B . 硫化钠的水解反应:S2-+H3O+  HS-+H2O
C . 将0.2mol/L的NH4Al(SO4)2溶液与0.3mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
D . NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
HS-+H2O
C . 将0.2mol/L的NH4Al(SO4)2溶液与0.3mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
D . NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
 HS-+H2O
C . 将0.2mol/L的NH4Al(SO4)2溶液与0.3mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
D . NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
HS-+H2O
C . 将0.2mol/L的NH4Al(SO4)2溶液与0.3mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
D . NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。(部分产品未标出)
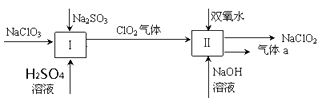
-
(1) Ⅰ中发生反应的还原剂是、Ⅱ中的氧化剂是(填化学式)。
-
(2) Ⅱ中反应的离子方程式是。
-
(3) ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:5NaClO2 + 4HCl = 5NaCl + 4ClO2↑+ 2H2O。
①该反应中氧化剂和还原剂的物质的量之比是。
②研究表明:在上述过程中会发生副反应:NaClO2 + 4HCl = NaCl + 2Cl2↑+ 2H2O,若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大。请推测其原因是。
下列离子方程式正确的是( )
A . 澄清的石灰水与盐酸反应:Ca(OH)2+2H+=Ca2++2H2O
B . 硫酸和氢氧化钡溶液反应:H++OH-=H2O
C . 铜片插入硝酸银溶液: Cu+Ag+=Cu2++Ag
D . 大理石溶于醋酸:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O
A,B,C,D是短周期元素形成的四种气体单质。E、F均为气体,且F为红棕色。有关的转化关系如下图所示(反应条件均已略去)。
请回答下列问题:
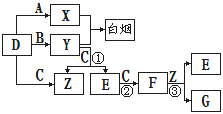
-
(1) D的化学式为 。
-
(2) 反应③的离子方程式为 。
-
(3) Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为 。
下列离子方程式正确的是( )
A . 向Na2S2O3溶液中通入足量氯气:S2O32-+ 2Cl2+3H2O=2SO32-+4Cl-+6H+
B . CuSO4溶液吸收H2S 气体:Cu2++H2S= CuS↓+2H+
C . AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D . 等体积、等浓度的Ba(OH)2稀溶液与NaHSO4稀溶液混合: Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
-
(1) 要确定铁的某氯化物FeClx的化学式。可用离子交换和滴定的方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预防处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量,并求出FeClx中x值。
-
(2) 现有一含有FeCl2和FeCl3的混合样品,采用上述方法测得n(Fe): n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为。在实验室中,FeCl2可用铁粉和反应制备,FeCl3可用铁粉和反应制备。
-
(3) FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为。
-
(4) 高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4 , 其反应的离子方程式为。
能用H+ + OH- = H2O 来表示的化学反应是:( )
A . Ba(OH)2溶液和HNO3溶液反应
B . NH3·H2O溶于稀H2SO4
C . KOH溶液和CH3COOH溶液反应
D . Ba(OH)2 溶液和H2SO4溶液反应
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)下列说法正确的是( )
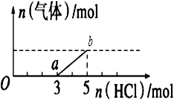
A . oa段反应的离子方程式为:H++OH-=H2O
B . O点溶液中所含溶质的化学式为NaHCO3、Na2CO3
C . 标准状况下,通入CO2的体积为4.48L
D . 原NaOH溶液的物质的量浓度为2.5mol•L﹣1
现有物质 ①铜 ②干冰
③盐酸
④液态醋酸 ⑤蔗糖
⑥NaHSO4 固体
⑦Ba(OH)2溶液
⑧ 熔融的
NaCl
-
(1) 能导电的是:属于电解质的是:
-
(2) 将NaHSO4固体溶于水,写出NaHSO4的电离方程式:
-
(3) ① 向Ba(OH)2溶液中逐滴滴加NaHSO4溶液至 Ba2+恰好完全沉淀,发生反应的离子方程式为: ;
②Ba2+恰好沉淀后继续滴加NaHSO4溶液时,发生反应的离子方程式为:
实验室为探究铁与浓硫酸的反应,并验证SO2的性质,设计如图所示装置进行实验。
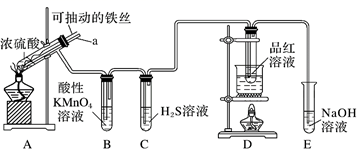
请回答下列问题:
-
(1) 装置B中酸性KMnO4溶液逐渐褪色,则装置B中发生反应的离子方程式是;装置C中发生反应的化学方程式是。
-
(2) 装置D的作用是;实验结束时需从导管a通入大量空气,其目的是。
-
(3) 实验时将导管a插入试管中,可使装置B中的溶液不发生倒吸。其原因是。
-
(4) 若装置A反应后的溶液中金属阳离子只含有Fe3+ , 则装置A中发生反应的化学方程式为。
亚硝酰氯( 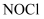 )是一种黄色气体,沸点为
)是一种黄色气体,沸点为 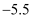 ℃。其液体呈红褐色。遇水发生反应:
℃。其液体呈红褐色。遇水发生反应: 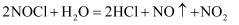 。某化学兴趣小组设计如图装置用
。某化学兴趣小组设计如图装置用  和
和  制备
制备 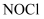 。回答下列相关问题:
。回答下列相关问题:
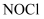 )是一种黄色气体,沸点为
)是一种黄色气体,沸点为 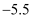 ℃。其液体呈红褐色。遇水发生反应:
℃。其液体呈红褐色。遇水发生反应: 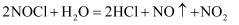 。某化学兴趣小组设计如图装置用
。某化学兴趣小组设计如图装置用  和
和  制备
制备 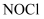 。回答下列相关问题:
。回答下列相关问题: 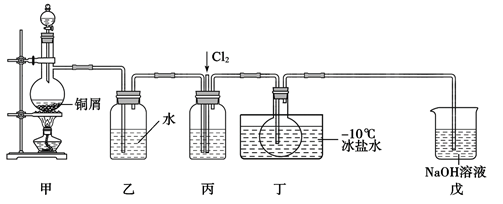
-
(1) 甲装置发生反应的离子方程式为,装置丙中的液体是浓硫酸。
-
(2) 实验时,先通入
 ,待丁中烧瓶内充满黄绿色气体时,再通入
,待丁中烧瓶内充满黄绿色气体时,再通入  ,这样做的目的是。
,这样做的目的是。
-
(3) 装置丁中冰盐水的作用是。
-
(4) 经分析该套装置设计上有一处明显缺陷,改进方法是。(用文字描述)
-
(5) 吸收尾气时,
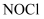 发生反应的化学方程式为。(已知:
发生反应的化学方程式为。(已知: 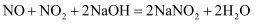 )
)
-
(6) 反应完成后,取烧瓶中所得产物mg溶于水,配制成
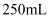 溶液,取出
溶液,取出 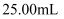 ,再加入
,再加入 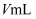
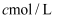
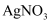 溶液恰好完全反应,则产物中
溶液恰好完全反应,则产物中 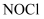 纯度(质量分数)的计算式为。
纯度(质量分数)的计算式为。
下列方程式与所给事实不相符的是( )
A . 向FeBr2溶液中通入过量Cl2:2Fe2++Cl2=2Fe3++2Cl-
B . 实验室制氨气:2NH4Cl+Ca(OH)2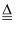 2NH3↑+CaCl2+2H2O
C . 铝溶于NaOH溶液:2Al+2OH-+2H2O=2AlO
2NH3↑+CaCl2+2H2O
C . 铝溶于NaOH溶液:2Al+2OH-+2H2O=2AlO +3H2↑
D . 将充满NO2的试管倒扣在水中:3NO2+H2O=2HNO3+NO
+3H2↑
D . 将充满NO2的试管倒扣在水中:3NO2+H2O=2HNO3+NO
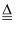 2NH3↑+CaCl2+2H2O
C . 铝溶于NaOH溶液:2Al+2OH-+2H2O=2AlO
2NH3↑+CaCl2+2H2O
C . 铝溶于NaOH溶液:2Al+2OH-+2H2O=2AlO +3H2↑
D . 将充满NO2的试管倒扣在水中:3NO2+H2O=2HNO3+NO
+3H2↑
D . 将充满NO2的试管倒扣在水中:3NO2+H2O=2HNO3+NO
回答下列问题:
-
(1) 某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图:
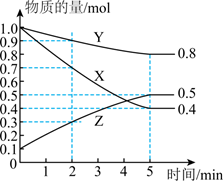
①该反应的化学方程式是。
②2min内X的转化率为。
-
(2) KMnO4是实验室中常用的一种试剂。回答下列问题:
①在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4弱酸)溶液,振荡,溶液紫色变无色。发生的化学反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+1OCO2↑+ 8H2O,若将该反应设计成原电池,则正极反应式为。
②在10mL 0.1 mol/L KMnO4溶液(含稀硫酸)中加入15 mL0.5 mol/L草酸溶液,收集到的CO2的量与时间的关系如图所示。AB段反应速率增大的原因可能是(填字母)。
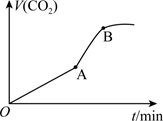
A.该反应是放热反应 B.反应物浓度增大
C.K2SO4起催化作用 D.MnSO4起催化作用
下列离子方程式书写正确的是( )
A . 过量的铁粉与稀硝酸反应: B . 实验室用氢氧化钙与氯化铵制备氨气:
B . 实验室用氢氧化钙与氯化铵制备氨气: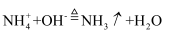 C . 向
C . 向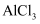 溶液中加入过量的氨水:
溶液中加入过量的氨水: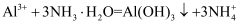 D . 将
D . 将 通入
通入 溶液产生黄色沉淀:
溶液产生黄色沉淀: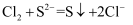
 B . 实验室用氢氧化钙与氯化铵制备氨气:
B . 实验室用氢氧化钙与氯化铵制备氨气: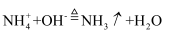 C . 向
C . 向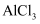 溶液中加入过量的氨水:
溶液中加入过量的氨水: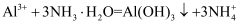 D . 将
D . 将 通入
通入 溶液产生黄色沉淀:
溶液产生黄色沉淀: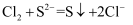
利用铜矿石(主要成分为 , 还含少量
, 还含少量 ,
,  , 制备
, 制备 晶体的流程如下图所示。已知
晶体的流程如下图所示。已知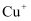 在酸性条件下不稳定,易生成金属
在酸性条件下不稳定,易生成金属 和
和 , 下列说法错误的是( )
, 下列说法错误的是( )
 , 还含少量
, 还含少量 ,
,  , 制备
, 制备 晶体的流程如下图所示。已知
晶体的流程如下图所示。已知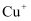 在酸性条件下不稳定,易生成金属
在酸性条件下不稳定,易生成金属 和
和 , 下列说法错误的是( )
, 下列说法错误的是( )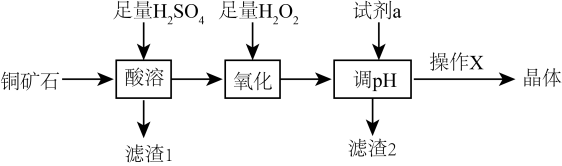
A . “滤渣1”的成分为 、
、 B . “氧化”过程中的离子方程式:
B . “氧化”过程中的离子方程式: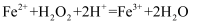 C . “调
C . “调 ”所用的试剂a可选用
”所用的试剂a可选用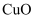 D . 操作X为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
D . 操作X为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
 、
、 B . “氧化”过程中的离子方程式:
B . “氧化”过程中的离子方程式: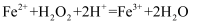 C . “调
C . “调 ”所用的试剂a可选用
”所用的试剂a可选用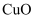 D . 操作X为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
D . 操作X为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
下列离子方程式正确的是( )
A . 向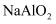 溶液中通入过量
溶液中通入过量 :
: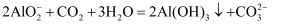 B .
B .  溶液中滴加足量的浓氨水:
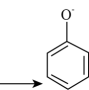
溶液中滴加足量的浓氨水: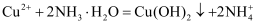 C . 向苯酚溶液中滴加
C . 向苯酚溶液中滴加 溶液:
溶液: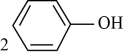
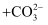
 D . 向氯化亚铁溶液中滴加稀硝酸:
D . 向氯化亚铁溶液中滴加稀硝酸: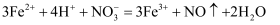
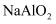 溶液中通入过量
溶液中通入过量 :
: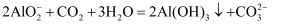 B .
B .  溶液中滴加足量的浓氨水:
溶液中滴加足量的浓氨水: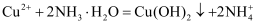 C . 向苯酚溶液中滴加
C . 向苯酚溶液中滴加 溶液:
溶液: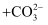

 D . 向氯化亚铁溶液中滴加稀硝酸:
D . 向氯化亚铁溶液中滴加稀硝酸: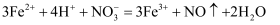
最近更新
- 在自然环境良好的情况下,群落演替过程中不可能发生的是() A. 群落中物种组不断变化 B.
- 下面这段文字有三句话,各有一处语病,请加以修改。①从06年开始,在每年6月的第二个星期六,被列为中国国家“文化遗产日”。
- ---Mrs. Brown, could you please tell us why your home---cook
- 有人认为秦始皇是“一代暴君”,但明代李贽称他为“千古一帝”。这个史上功过参半的君王,以下属于他统治时期所采取的措施有 ①
- 明朝,徽州人多地少,且自然条件恶劣,土地贫瘠,故几乎家家经商,但徽州贫瘠的土地价格上涨幅度却居全国之首,形成“田少而值昂
- 2011年10月25日,国家广电总局发布《关于进一步加强电视上星综合频道节目管理的意见》提出:从2012年1月1日起,包
- 中国领导的人民武装力量首次正式公开表明自己是工农群众利益代表的是 ( )A.南昌起义的部队
- 附加题(1)石墨晶体的层状结构,层内为平面正六边形结构(如图a),试回答下列问题:图中平均每个正六边形占有C原子数为__
- 多细胞动物进行细胞之间的信息传递,可分为直接传递和间接传递两种。下列哪类物质在细胞之间起间接传递信息的作用( )
- 下列分子属于手性分子的是()
- 常温下,向一定浓度的氨水中逐滴加入盐酸,关于溶液中各离子浓度大小关系叙述最准确的是 ( )
- 伴随着城市经济的发展,宋代出现了许多描绘民间风情的风俗画。其中,被誉为中华第一神品"的是 A.《敦煌飞天图》 B
- 计算:(- )÷
- 有机物分子中,所有原子不可能在同一平面上的是()
- 已知回归直线方程=0.50x-0.81,则当x=25时,y的估计值为 。
- 小明在藕片上滴加2滴碘酒,结果滴加碘酒的部分变成了深蓝色。这说明藕片里含有A.蛋白质B.脂肪C.淀粉D.维生素
- 下图为“我国某地农业结构调整示意图”。读图回答下列各题。 下列关于该地调整前后的农业生产特点的叙述,错误的是 A.调整前
- 在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,下列物质可选用: A.NaOH B.HC1
- (2013安徽宿州泗县质检)带电粒子在AB两极板间靠近A板中央附近S处静止释放,在两极板电压中加速,从小孔P平行CD极板
- (8分)A、B代表不同物质,都是H、N、O三种元素组成的强电解质,A、B的水溶液都呈酸性,且相同浓度时,A溶液抑制水的电



