物质的量浓度 知识点题库
下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是( )
A . 该试剂的物质的量浓度为9.2 mol/L
B . 该硫酸50mL与足量的铜反应生成标准状况下10.3 L SO2
C . 配制250mL、4.6 mol/L的稀硫酸需该硫酸62.5 mL
D . 该硫酸与等体积的水混合后所得溶液的质量分数小于49%
将5mol•L﹣1的盐酸10mL稀释到200mL,再取出5mL,这5mL溶液的物质的量浓度是( )
A . 0.05 mol•L﹣1
B . 0.25 mol•L﹣1
C . 0.10 mol•L﹣1
D . 0.50 mol•L﹣1
已知某溶液的:①体积;②密度;③溶质和溶剂的质量比;④溶质的摩尔质量,要根据溶质的溶解度计算其饱和溶液的物质的量浓度时,上述条件中必不可少的是( )
A . ①②③④
B . ①②③
C . ②④
D . ①④
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )

A . 该硫酸的物质的量浓度为9.2 mol/L
B . 1 mol Zn与足量该硫酸反应产生2 g氢气
C . 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL
D . 该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L
用标签所示浓盐酸配制250mL 0.4mol/L的稀盐酸,并进行有关实验.

请回答:
-
(1) 需要量取浓盐酸 mL.
-
(2) 配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有、.
-
(3) 若实验遇到下列情况,所配溶液的浓度会(填“偏高”、“偏低”、“不变”)
A、定容时仰视刻度线;
B、容量瓶内壁附有水珠而未干燥处理;
C、溶解后没有冷却便进行定容.
-
(4) 将所配制的稀盐酸倒入5.92g Na2CO3和NaHCO3的固体混合物中,恰好完全反应,则原混合物中Na2CO3的质量分数为.
下列溶液中,Cl﹣的物质的量浓度最大的是( )
A . 300 mL0.1 mol/L NaCl溶液
B . 100 mL0.1 mol/LFeCl3溶液
C . 标准状况下,4.48LHCl气体溶于水配成的1 L溶液
D . 向1 L0.2 mol/L BaCl2溶液中加入0.2 mol/L的H2SO4溶液到沉淀恰好完全时的溶液(忽略溶液混合时的体积变化)
标准状况下,将体积为V L充满氨气的圆底烧瓶倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm﹣3 . 下列说法错误的是( )
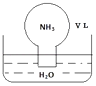
A . 水最终会充满整个烧瓶
B . 所得溶液的物质的量浓度为 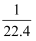 mol•L﹣1
C . 所得溶液的质量分数为
mol•L﹣1
C . 所得溶液的质量分数为 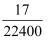 ρ
D . 将氨气换为二氧化氮,所得溶液的物质的量浓度也为
ρ
D . 将氨气换为二氧化氮,所得溶液的物质的量浓度也为 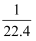 mol•L﹣1
mol•L﹣1
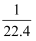 mol•L﹣1
C . 所得溶液的质量分数为
mol•L﹣1
C . 所得溶液的质量分数为 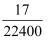 ρ
D . 将氨气换为二氧化氮,所得溶液的物质的量浓度也为
ρ
D . 将氨气换为二氧化氮,所得溶液的物质的量浓度也为 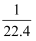 mol•L﹣1
mol•L﹣1
现将200mL0.01mol/LNaOH与50mL某浓度的Ca (OH)2溶液混合(混合后体积变化忽略不计),所得溶液中OH﹣的物质的量浓度是0.016mol/L,则Ca(OH)2溶液的物质的量浓度是mol/L.
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 所含共价键数均为0.2NA的白磷(P4)和甲烷的物质的量相等
B . 1L 1mol/LH2O2的水溶液中含有的氧原子数为2NA
C . 将1molFe 与一定量的稀硝酸充分反应,转移的电子数可能为2NA
D . 1L0.1mol/LCH3COONa溶液中含有的Na+和CH3COO-的总数为0.2NA
已知300mL某浓度的NaOH溶液中含60g溶质。现欲配制1 mol/L 的NaOH溶液,应取原溶液与蒸馏水的体积比约为 (忽略稀释时体积的变化) ( )
A . 1︰4
B . 1︰5
C . 2︰1
D . 2︰3
现有300mL某无色溶液,可能含有以下离子的若干种:Na+、Fe2+、Mg2+、NH4+、Cl-、SO42-、CO32- , 将该溶液分为三等份进行以下实验:①向第一份加入足量NaOH溶液后加热,收集到气体0.336L(标准状况);②向第二份加入AgNO3溶液,有白色沉淀产生;③向第三份加入足量BaCl2溶液,得到沉淀6.27g,经足量盐酸洗涤后,剩余2.33g。
试回答下列问题:
-
(1) 肯定不存在的离子有;
-
(2) 可能存在的离子是,判断该离子存在与否的操作是;
-
(3) 计算肯定存在的阳离子在原溶液中的物质的量浓度。
下列各组数据中,前者刚好是后者两倍的是( )
A . 2mol H2O的摩尔质量和1mol H2O的摩尔质量
B . 200mL1mol·L-1氯化钙溶液中c(Cl-)和100mL2mol·L-1氯化钾溶液中c(Cl-)
C . 称量16g硫酸铜配制250mL溶液的物质的量浓度和称量25g胆矾配制500mL溶液的物质的量浓度
D . 20%NaOH溶液的物质的量浓度和10%NaOH溶液的物质的量浓度
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A . 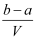 mol·L-1
B .
mol·L-1
B . 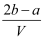 mol·L-1
C .
mol·L-1
C . 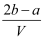 mol·L-1
D .
mol·L-1
D . 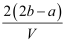 mol·L-1
mol·L-1
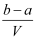 mol·L-1
B .
mol·L-1
B . 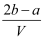 mol·L-1
C .
mol·L-1
C . 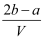 mol·L-1
D .
mol·L-1
D . 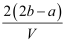 mol·L-1
mol·L-1
-
(1) 顺铂(化学名称为顺二氯二氨合铂(II),化学式为PtCl2(NH3)2 , 相对分子质量为:300)是一种用于治疗癌症的药物,一片顺铂药片所含顺铂的质量为6×10-4g,那么一片顺铂药片中N原子的物质的量mol;
-
(2) 乙烯气体(C2H4)是石油化工产品之一,也是最重要的有机化工基础原料之一,在标准状况下其密度为g•L-1;
-
(3) 现有一种矿泉水样品,1.0L的该矿泉水含有4.8×10-2gMg2+ , 则L矿泉水中含有1mol Mg2+;
-
(4) 某“84消毒液”1000mL,其有效成分为NaClO(式量:74.5),质量分数为14.9%,密度为1.2g/mL,其溶质的物质的量浓度为mol•L﹣1;
-
(5) 已知CO和CO2的混合气体7.2g,在标准状况下所占的体积为4.48L。则该混合气体中氧元素的质量为g;
-
(1) 0.5molCH4的质量是g,在标准状况下的体积为L;含有约个氢原子。
-
(2) 将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·mL-1 , 质量分数为w , 其中含有NH4+的物质的量是b mol,下列叙述正确的是( )
A . 溶质的质量分数w=a/(ρV-a)×100%
B . 溶质的物质的量浓度c=1000a/35V mol·L-1
C . 溶液中c(OH-)=1000b/V mol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
在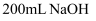 溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体
溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体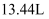 , 该
, 该 溶液的浓度为( )
溶液的浓度为( )
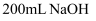 溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体
溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体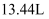 , 该
, 该 溶液的浓度为( )
溶液的浓度为( )
A . 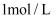 B .
B . 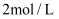 C .
C . 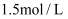 D .
D . 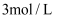
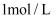 B .
B . 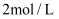 C .
C . 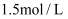 D .
D . 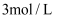
 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
A . 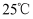 ,
, 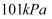 下,
下,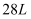 氢气中质子的数目为
氢气中质子的数目为 B .
B . 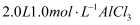 溶液中,
溶液中,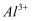 的数目为
的数目为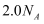 C .
C . 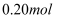 苯甲酸完全燃烧,生成
苯甲酸完全燃烧,生成 的数目为
的数目为 D . 电解熔融
D . 电解熔融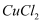 , 阴极增重
, 阴极增重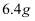 , 外电路中通过电子的数目为
, 外电路中通过电子的数目为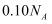
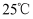 ,
, 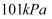 下,
下,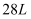 氢气中质子的数目为
氢气中质子的数目为 B .
B . 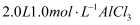 溶液中,
溶液中,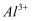 的数目为
的数目为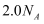 C .
C . 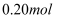 苯甲酸完全燃烧,生成
苯甲酸完全燃烧,生成 的数目为
的数目为 D . 电解熔融
D . 电解熔融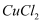 , 阴极增重
, 阴极增重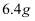 , 外电路中通过电子的数目为
, 外电路中通过电子的数目为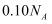
将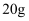 含杂质
含杂质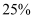 的大理石(杂质与盐酸不反应)投入
的大理石(杂质与盐酸不反应)投入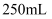 盐酸中恰好完全反应,计算:(写出计算过程)
盐酸中恰好完全反应,计算:(写出计算过程)
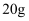 含杂质
含杂质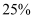 的大理石(杂质与盐酸不反应)投入
的大理石(杂质与盐酸不反应)投入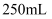 盐酸中恰好完全反应,计算:(写出计算过程)
盐酸中恰好完全反应,计算:(写出计算过程)
-
(1) 反应生成的
 的体积(标准状况)
的体积(标准状况)
-
(2) 原盐酸的物质的量浓度。
下列说法正确的是( )
A . 用浓硫酸配制一定物质的量浓度的稀硫酸时,量取浓硫酸时仰视量筒,会使所配溶液浓度偏小
B . 0.5L0.1mol/LMgCl2与0.2L0.1mol/LNaCl溶液中的Cl-的物质的量浓度之比为2:1
C . 同温同压下,20mLCH4和60mLO2所含的原子数之比为1∶3
D . 镁原子的摩尔质量等于它的相对原子质量
最近更新
- (浙江卷理9)已知,b是平面内两个互相垂直的单位向量,若向量满足,则的最大值是 (A)1 (B)2
- 如地球质量M可由表达式求出,式中G为引力常量,的单位是m/s,是的幂次,c的单位是m/s2,以下判断正确的是
- 固定不动的正点电荷A,带电量为Q=1.0×10-6C,点电荷B从距A无穷远的电势为零处移到距A为2cm、电势为3000V
- Jack, you______ play with the knife; you______ hurt yoursel
- ①当且仅当m为何值时,经过两点A(-m,6)、B(1,3m)的直线的斜率为12?②当且仅当m为何值时,经过两点A(m,2
- (9分)阅读材料,回答问题。小敏在小学时是班干部,学习成绩是全班最好的。进入中学后,她又被选为班长,这个班在她的带领下搞
- The police set about arresting the suspect ______ they found
- 30. _____in a science competition, the three students were a
- 一光滑圆环固定在竖直平面内,环上套着两个小球A和B(中央有孔),A、B间由细绳连接着,它们处于如图中所示位置时恰好都能保
- 下列关于物质性质的比较,不正确的是 A.酸性强弱:HIO4>HBrO4>HClO4 B.原子半径
- 有下列物质:①烧碱 ②浓硫酸 ③大理石 ④小苏打 ⑤甲烷 ⑥金刚石,请按下列要求填空(填序号):能用来划玻璃的
- 戊戌变法具有爱国和进步的意义,其进步性主要表现在 A.挽救民族危亡 B.要求变革一些旧制度 C.与顽固派进
- 已知函数f(x)=x2+2ax+2,x∈[-5,5].(1)当a=-1时,求函数f(x)的最大值与最小值;(2)求实
- 请根据下图填空: ⑴写出两种标号仪器的名称:①________,②________;做C图所示实验的目的是
- 2的相反数是 A. 2 B.-2 C.
- 从A、B、C、D四个选项中,选出可以填入空白处的最佳选项。 –Would you likesome drinks, bo
- 房屋征收与补偿涉及多方利益。假如你所在的班级要以此举办一次模拟听证会,以下是举办听证会过程的一般步骤,你认为最合理的(
- 下列属于化学变化的是A.蛋清溶液中滴加饱和硫酸铵溶液 B.日本核电站工作人员给核电机组注水降温C.炼油厂蒸馏原油获得汽油
- (08湖北襄樊)学习过“影响摩擦力大小的因素”后,小强发现实验室里有如图10所示的铁块和木块。他想比较一下铁块表面和木块
- 下列词语中没有错别字的一项是( ) A.浩翰 虔诚 心有余悸 融融泄泄 B.典范



