配制一定物质的量浓度的溶液 知识点题库
-
(1) 需量取浓硫酸的体积为 mL.
-
(2) 配制溶液时,一般可以分为以下几个步骤:①量取 ②计算 ③溶解 ④颠倒摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却,其正确的操作顺序为 ,本实验必须用到的仪器有量筒、玻璃棒、烧杯、胶头滴管、还有
-
(3) 在配制过程中,下列操作会引起浓度偏高的是 ,无影响的是 (填序号).
①没有洗涤烧杯和玻璃棒;
②转移溶液时不慎有少量洒到容量瓶外面;
③容量瓶不干燥,含有少量蒸馏水;
④定容时俯视刻度线;
⑤未冷却到室温就将溶液转移到容量瓶并定容;
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
-
(1) 完成该实验用到的仪器主要有:托盘天平、胶头滴管、,烧杯、玻璃棒、药匙.
-
(2) 如果用CuSO4固体来配制,应该称量固体的质量为.
-
(3) 下列操作对溶液的浓度有何影响?用“偏大”“偏小”或“无影响”填空.
①配制的过程中有少量的液体溅出烧杯.
②使用前容量瓶用蒸馏水洗涤,且没有干燥.
③定容时俯视液面..
-
(1) 容量瓶不能用于 (填序号).A . 配制一定体积准确浓度的标准溶液 B . 贮存溶液 C . 测量容量瓶规格以下的任意体积的液体 D . 用来加热溶解固体溶质
-
(2) 根据计算用托盘天平称取NaOH的质量为g.在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度0.1mol/L(填“大于”“等于”或“小于”,下同).若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度0.1mol/L.
-
(3) 根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为mL(计算结果保留一位小数)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是.在配制过程中,下列操作中,能引起误差偏高的有(填代号).
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
②定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
③定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④定容时,俯视刻度线.
-
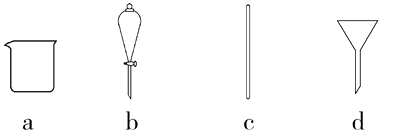
(1) 根据计算,配制上述溶液用托盘天平称取的NaOH固体质量为克,在下图所示仪器中,配制上述溶液肯定不需要的是(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是。
-
(2) 配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
-
(3) 关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是_________(填字母)。A . ②③④ B . ②③ C . ①②④ D . ①②③④
-
(4) 从该溶液中取出10 mL,其中NaOH的物质的量浓度为,含NaOH的质量为。
-
(5) 下面操作造成所配NaOH溶液浓度偏高的是____________(填字母)。A . 溶解后溶液没有冷却到室温就转移 B . 转移时没有洗涤烧杯、玻璃棒 C . 向容量瓶加水定容时眼睛俯视液面 D . 摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
-
(1) 写出下列仪器的名称:a.,
B.,
C.。
-
(2) 若利用装置分离酒精和水的混合物,还缺少的仪器是,冷凝水由口流出(填f或g)。
-
(3) 现需配制0.1mol/LNaOH溶液450mL,装置B是某同学转移溶液的示意图。
①图中的错误是。
②根据计算得知,所需NaOH的质量为。
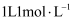 的NaCl溶液时,用托盘天平称量5.85gNaCl固体
D . 定容时,为防止液滴飞溅,胶头滴管应紧贴容量瓶内壁
的NaCl溶液时,用托盘天平称量5.85gNaCl固体
D . 定容时,为防止液滴飞溅,胶头滴管应紧贴容量瓶内壁
铝制易拉罐经稀硫酸微热溶解,加入H2O2溶液,调节pH=3.7,第一次过滤后向滤液中加入少量NaHCO3饱和溶液,第二次过滤出白色沉淀。趁热加入质量分数为a% H2SO4溶液和K2SO4固体,然后冷却、洗涤、第三次过滤,得到粗明矾。
完成实验报告:
-
(1) 实验准备:
①为了加快溶解,铝制易拉罐首先要;
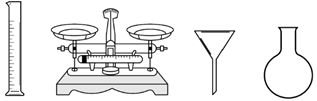
②配制a% H2SO4溶液的仪器:烧杯、玻璃棒、(从图中选择,写出名称)。
-
(2) 溶解、除杂(Fe2+、Fe3+):
①加入H2O2氧化Fe2+时,H2O2实际消耗量常超出氧化还原计算的用量,你预计可能的原因是;
②思考:在本实验中,含铁杂质在第次过滤中被去除。
-
(3) 沉铝:
①现象记录:“向滤液中加入少量NaHCO3饱和溶液”处理,溶液中产生。
②思考:(填“有”或“无”)必要用KHCO3替代NaHCO3。
-
(4) 明矾的制备与结晶(15℃时明矾溶解度为4.9 g/100 g H2O):
①加入a%H2SO4溶液时,a最好是(选填“20%”、“60%”或“98%”)。
②为了提高明矾收率,可采取、措施。
-
(5) 实验改进:
为减少试剂用量、方便除杂,设计制备明矾的新方案如下:
易拉罐经溶液微热溶解,过滤后向滤液中加入溶液,第二次过滤出白色沉淀。加入H2SO4溶液和K2SO4固体,然后冷却、洗涤、过滤,得到粗明矾。
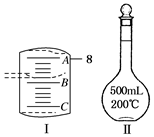
-
(1) 应该用托盘天平称取CuSO4·5H2Og。
-
(2) 如图Ⅰ表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为8,量筒中液体的体积是mL。
-
(3) 若实验中如图Ⅱ所示的仪器有下列情况,对配制溶液的浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.定容前容量瓶底部有水珠;
B.定容时加水超过刻度线;
C.最终定容时俯视观察液面。
-
(1) 在实验过程中,选用最合适的容量瓶为_______。A . 200 mL容量瓶 B . 250 mL容量瓶 C . 500 mL容量瓶
-
(2) 容量瓶上标有_______。(填字母)
①温度 ②物质的量浓度 ③容积 ④压强 ⑤刻度线
A . ①③⑤ B . ①③④ C . ②④ D . ②④⑤ -
(3) 通过计算,应该使用托盘天平称取胆矾g。
-
(4) 下列操作会使所配溶液浓度偏高的是。
①实验前,容量瓶用蒸馏水洗涤后未用标准液润洗;
②所用的胆矾晶体由于保存不善,导致失去部分结晶水;
③溶解时,不小心有少量溶液溅出;
④移液后,洗涤烧杯和玻璃棒2-3次,并将洗涤液也移入容量瓶;
⑤定容时,俯视液面;
⑥摇匀后,发现液面低于刻度线,又加水至刻度线。
-
(5) 将蓝色胆矾晶体加热会逐步失去结晶水,最终变为白色的硫酸铜粉末,则该变化过程为变化(填“物理”或“化学”)。
- 已知椭圆C:的离心率为,双曲线x²-y²=1的渐近线与椭圆有四个交点,以这四个交点为顶点的四边形的面积为16,则椭圆C的
- 下列分子或离子中,不存在sp3杂化类型的是:( ) A、H2O B、NH3 C
- 以下是有关现代生物技术的两个问题,请回答: Ⅰ:下列三图分别表示基因的结构示意图和利用基因工程培育抗虫棉过程示意图。请据
- Thereare __people in the park . A.many B. lot of C. much.
- 行进在大峡谷,满眼的大山架起凝重厚实的躯体,脚下的江水唤出低吟的浪涛。险恶的地理环境中,傈僳族同胞生息劳作在这里,除了江
- 经过点P(3,2)并且使两坐标轴上的截距的绝对值相等的直线方程是____________.
- 通过学习地理,我们了解了很多遥远的地区。对下图中各区域范围的描述,正确的是( ) A.美洲地区由北美洲和拉丁美洲两个
- 下列生活中常见的变化,属于化学变化的是 A.冰雪融化 B.菜刀生锈 C.灯泡发光
- 补写出下列名句名篇和文学常识的空缺部分。(6分) ①李白在《梦游天姥吟留别》中表明自己不愿意与权贵同流合污的句子
- 总书记在十七大报告中指出,我们所面临着的机遇前所未有,挑战也前所未有,机遇大于挑战。全党必须抓住和用好重要战略机遇期,求
- 已知抛物线型拱桥的顶点距水面2米,测量水面宽度为8米.当水面上升1米后,水面宽度为 ▲ 米. (
- 在地球上出现极昼、极夜现象的地方在 ( ) A. 寒带 B.赤道 C. 热带
- 已知则等于 ____ A.-1 B.1 C.14 D.7
- 如图:已知PA⊥⊙O所在的平面,AB是⊙O的直径,C是异于A、B的⊙O上任意一点,过A作AE⊥PC于E ,求证:AE⊥平
- 甲烷中有混有乙烯,欲除去乙烯得到纯净的甲烷,最好依次通过盛有_________试剂的洗气瓶()A.澄清石灰水,浓硫酸B.
- 读“中心点为地球某一极点的示意图”,M为某一地球同步通信卫星,箭头表示卫星绕地球转动的方向。关于该通信卫星运动特征的描述
- 假设200件产品中有3件次品,现在从中任意抽取5件,其中至少有2件次品的抽法有( )A.种
- 下列说法中正确的是A.冰醋酸溶于水时,分子中羧基上的氢氧共价键部分发生断裂B.原子及其离子的核外电子层数等于该元素所在的
- 下列现象中属于升华现象的是()A.湿衣服过一段时间会干B.放入衣箱中的樟脑丸变小C.用铁水浇铸工件D.冬天,洗热水澡时室
- 下列四幅生活中的图片,能反映出重要空气污染源的是 ( )A.丹顶鹤自由飞翔 B.公园风景如画 C.工厂烟囱林



