物质的分离与提纯 知识点题库
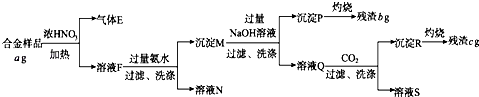
下列相关叙述正确的是( )
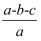 ×100%
D . 合金样品中Al的质量分数为
×100%
D . 合金样品中Al的质量分数为 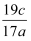 ×100%
×100%
原物质 | 所含杂质 | 除杂试剂 | 主要操作方法 | |
A | HNO3溶液 | H2SO4 | BaCl2溶液 | 过滤 |
B | CO2 | SO2 | 酸性KMnO4溶液、浓硫酸 | 洗气、干燥 |
C | SiO2 | Al2O3 | 稀盐酸 | 过滤 |
D | C2H5OH | CH3COOH | CaO | 蒸馏 |
-
(1) Na2SO4溶液(Na2CO3):所加试剂离子方程式
-
(2) O2(CO2):所加试剂离子方程式
-
(3) FeSO4溶液(CuSO4):所加试剂离子方程式
-
(4) Fe(Al)所加试剂离子方程式.
混合物 | 试剂 | 分离方法 | |
A | 苯(苯酚) | 溴水 | 过滤 |
B | 甲烷(甲醛) | 水、浓硫酸 | 洗气 |
C | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
D | 淀粉胶体(氯化钠溶液) | 蒸馏水 | 萃取 |
-
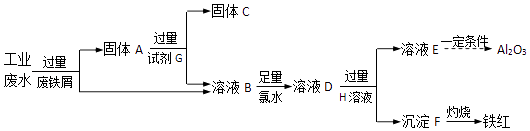
(1) 固体A的成分是(填化学式).
-
(2) 溶液B中的金属阳离子有.
-
(3) B→D反应的离子方程式是.
-
(4) 试剂G是(填名称).
-
(5) 溶液E焰色反应呈黄色,试剂H是.
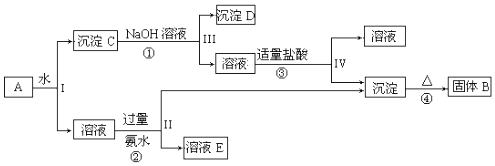
据此回答下列问题:
-
(1) KAl(SO4)2的电离方程式.
-
(2) 根据上述框图反应关系,写出下列C、E所含物质的化学式沉淀C.
-
(3) 写出①、②两步的化学反应方程式是
①.
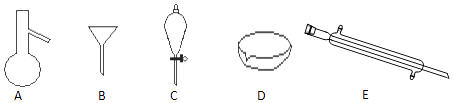
-
(1) 写出仪器A、C、E的名称
-
(2) 分离以下混合物应该主要选用什么仪器?(填字母符号)
食用油和酒精: 汽油和水:.
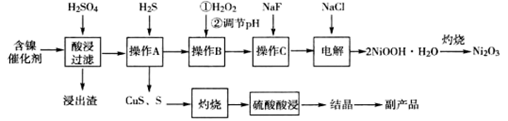
已知:①有关氢氧化物开始沉淀和沉淀完全的pH如表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.6 | 9.7 | 9.2 |
②常温下CaF2难溶于水,微溶于无机酸
-
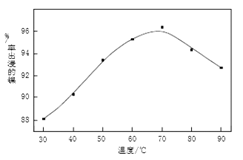
(1) 操作B中需调节pH范围为,使用Na2CO3调节pH过程中发生的反应有。实验人员发现温度不同时,镍的浸出率不同,浸出率与温度的关系如图所示。请解释当温度高于70℃时,浸出液中Ni2+含量降低的原因。
-
(2) 下列说法正确的是____A . 为提高酸浸效率,可充分搅拌或适当提高硫酸浓度 B . 操作A中应持续通入过量H2S气体使杂质Cu2+彻底沉淀 C . 浸出渣的主要成分为CaSO4•2H2O和BaSO4 D . 为得到副产品胆矾,应蒸发浓缩至出现大量晶体,用玻璃纤维代替滤纸进行趁热过滤
-
(3) 电解过程中,Cl-在阳极被氧化为ClO- , 但是反应前后溶液中Cl-浓度不变。写出生成沉淀反应的离子方程式。
-
(4) 操作C加入NaF后如何证明沉淀完全。
-
(5) 工业上也可通过将草酸镍(NiC2O4•2H2O)在热空气中干燥脱水,再在高温下煅烧三小时制得Ni2O3 , 同时获得混合气体。草酸镍受热分解的化学方程式为。
| 选项 | 物质 | 选用试剂(过量) | 操作方法 |
| A | CO(CO2) | NaOH溶液 | 洗气、浓硫酸干燥 |
| B | FeSO4溶液(CuSO4) | 铁粉 | 过滤 |
| C | NaBr溶液(Br2) | 四氯化碳 | 萃取、分液 |
| D | KNO3(KCl) | AgNO3溶液 | 溶解、过滤、蒸发、结晶 |
 形式存在,采用以下工艺流程可由黏土钒矿制备V2O5。
形式存在,采用以下工艺流程可由黏土钒矿制备V2O5。 已知:V2O5在碱性条件下以VO  形式存在。
形式存在。
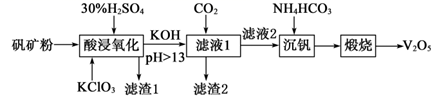
以下说法正确的是( )
 ,至少需要1molKClO3
B . 滤液1中主要的阴离子有[Al(OH)4]-和VO
,至少需要1molKClO3
B . 滤液1中主要的阴离子有[Al(OH)4]-和VO  C . “煅烧”时需要的仪器主要有蒸发皿、玻璃棒、三脚架、酒精灯
D . “煅烧”时,NH4VO3受热分解:2NH4VO3
C . “煅烧”时需要的仪器主要有蒸发皿、玻璃棒、三脚架、酒精灯
D . “煅烧”时,NH4VO3受热分解:2NH4VO3  V2O5+2NH3↑+H2O
V2O5+2NH3↑+H2O
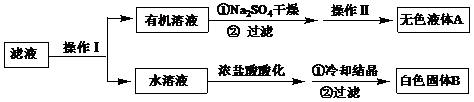
下列说法正确的是( )
-
(1) Ⅰ.海带中碘元素的确定
海带
 海带灰
海带灰 
 海带灰浸取液
海带灰浸取液取海带灰浸取液
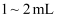 ,加入稀硫酸约
,加入稀硫酸约 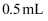 、5%的
、5%的  溶液约
溶液约 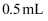 ,然后加入
,然后加入  约
约 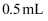 ,振荡后静置,可以观察到,证明海带中含有碘元素,该反应的离子方程式为。
,振荡后静置,可以观察到,证明海带中含有碘元素,该反应的离子方程式为。 -
(2) Ⅱ.海带提碘
海带灰浸取液
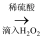 含I2的水溶液
含I2的水溶液 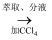 碘的有机溶液→晶体碘
碘的有机溶液→晶体碘若向
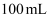 碘水L中加入
碘水L中加入 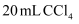 ,充分振荡、静置,此时碘在
,充分振荡、静置,此时碘在  中的物质的量浓度是水中的86倍,则萃取效率为%(结果保留小数点后两位)(萃取效率
中的物质的量浓度是水中的86倍,则萃取效率为%(结果保留小数点后两位)(萃取效率  )。
)。 -
(3) 萃取实验中,若要使碘尽可能地完全转移到
 中,可以采取的操作是。
中,可以采取的操作是。
-
(4) 某同学采取减压蒸馏(装置如图),可以很快完成碘和四氯化碳的分离,减压蒸馏时使用了克氏蒸馏头,克氏蒸馏头比普通蒸馏头增加了一个弯管,弯管的主要作用是。
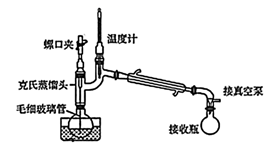
-
(5) Ⅲ.海带中碘含量的测定
若称取干海带
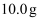 ,经灼烧、浸取、
,经灼烧、浸取、  氧化等过程后配制成
氧化等过程后配制成 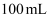 溶液,移取
溶液,移取 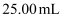 于锥形瓶中,用
于锥形瓶中,用  标准溶液滴定,待溶液由黄色变为浅黄色时,滴加两滴淀粉指示剂,继续滴定至蓝色刚好褪去,且半分钟内无变化,即为终点,平行滴定3次,记录所消耗的
标准溶液滴定,待溶液由黄色变为浅黄色时,滴加两滴淀粉指示剂,继续滴定至蓝色刚好褪去,且半分钟内无变化,即为终点,平行滴定3次,记录所消耗的  溶液的平均体积为
溶液的平均体积为 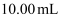 ,计算海带中含碘的质量分数为%(结果保留小数点后两位)(已知
,计算海带中含碘的质量分数为%(结果保留小数点后两位)(已知  )。若滴定结束读数时俯视刻度线,会导致测定结果(填“偏高”“偏低”或“不影响”)。
)。若滴定结束读数时俯视刻度线,会导致测定结果(填“偏高”“偏低”或“不影响”)。
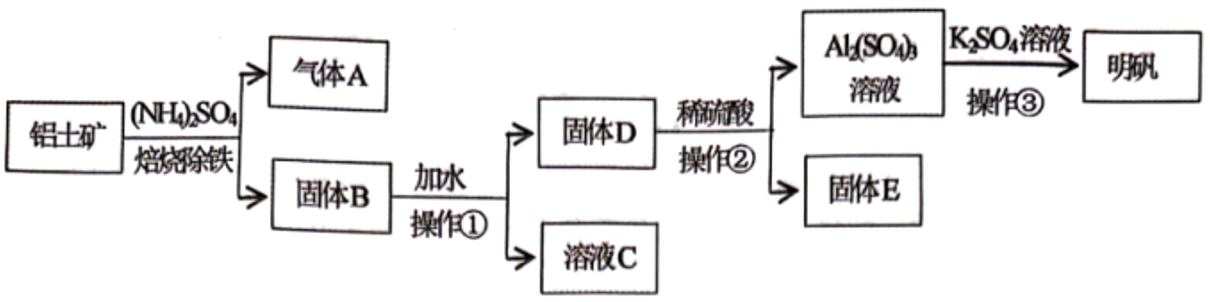
-
(1) 焙烧除铁反应:4(NH4)2SO4+Fe2O3
 2NH4Fe(SO4)2+3H2O+6A↑(Al2O3少部分发生类似反应)。气体A的化学式为。
2NH4Fe(SO4)2+3H2O+6A↑(Al2O3少部分发生类似反应)。气体A的化学式为。
-
(2) 操作①的名称是,操作①后,需洗涤固体D表面吸附的离子,判断固体D是否洗涤干净的实验方法是:取最后一次洗涤后的浸出液于试管中,滴加KSCN溶液,观察到,说明已洗涤干净。
-
(3) 固体D加稀硫酸反应的离子方程式为。
-
(4) 操作③的具体步骤是蒸发、、过滤、洗涤、干燥。
-
(5) 固体E与NaOH固体焙烧可制备防火材料,下列装置适合的是(填字母编号)。
a.
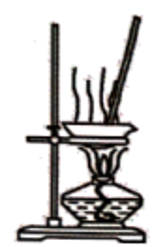 b.
b.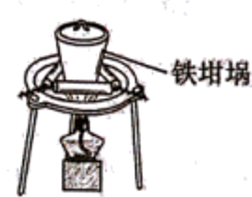 c.
c.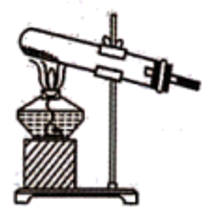 d.
d.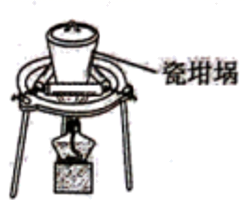
-
(6) 不计过程中的损失,投入5t铝土矿,理论上可制得明矾t(明矾的相对分子质量为474)。
物质 | 熔点/℃ | 沸点/℃ | 密度/g.cm-3 | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 | 83 | 1.4 | 易溶于水 | |
浓硫酸 | 338 | 1.84 | 易溶于水 |
实验步骤如下:
ⅰ.取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制混和酸,将混合酸小心加入B中。把18mL(15.84 g)苯加入A中。
ⅱ.向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
ⅲ.将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2 , 进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
-
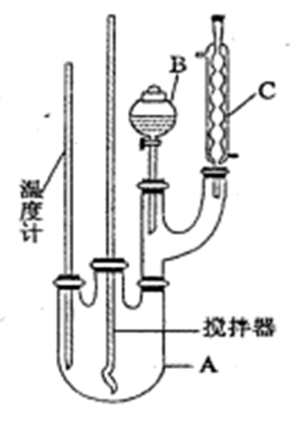
(1) 图中装置C的作用是。
-
(2) 制备硝基苯的化学方程式。
-
(3) 叙述配制混合酸操作:。
-
(4) 为了使反应在50℃~60℃下进行,常用的方法是。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是(用化学方程式说明),除去该有色物质选择的试剂是,分离提纯的方法为。
-
(5) 在洗涤操作中,第二次水洗的作用是。
-
(6) 在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用水直形冷凝管的原因是。
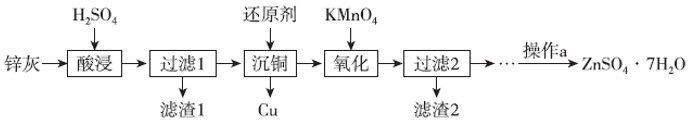
已知:①锌灰的主要成分为ZnO,还含有CuO、PbO、MnO和FeO;
②“滤渣2”的主要成分为Fe(OH)3和MnO(OH)2;
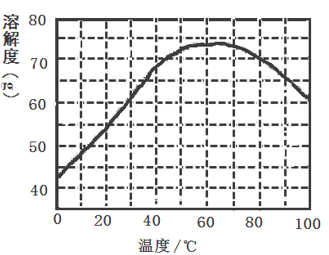
③已知ZnSO4的溶解度随温度变化如图。
请回答下列问题:
-
(1) “滤渣1”的主要成分为 。
-
(2) “氧化”时,Fe2+被氧化的离子方程式为
-
(3) 操作a涉及以下操作:a.在60℃蒸发溶剂;b.在100℃蒸发溶剂;c.蒸发至溶液出现晶膜,停止加热;d.冷却至室温;e.过滤。
以上操作的正确顺序为:(上述操作可重复使用)。
-
(4) ZnSO4·7H2O产品的纯度可用滴定法分析测定。下列关于滴定分析,正确的是____。
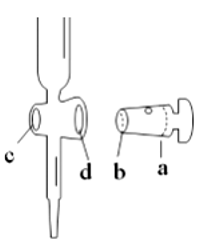 A . 如图中,应将凡士林涂在旋塞的b端和旋塞套内的d端 B . 滴定前,滴定管须用标准溶液润洗 C . 将标准溶液装入滴定管时,应借助漏斗转移防止溅出 D . 滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转 E . 滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测得的体积比实际消耗的小
A . 如图中,应将凡士林涂在旋塞的b端和旋塞套内的d端 B . 滴定前,滴定管须用标准溶液润洗 C . 将标准溶液装入滴定管时,应借助漏斗转移防止溅出 D . 滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转 E . 滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测得的体积比实际消耗的小 -
(5) 工业上采用惰性电极电解ZnSO4溶液可实现湿法炼锌,电解过程中的离子方程式为。
 溶液,用汽油萃取
B . 酸性
溶液,用汽油萃取
B . 酸性  溶液既可鉴别乙烷和乙烯,又可除去乙烷中少量的乙烯
C . 乙烷中有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷
D . 己烷中溶有溴单质,可加足量氢氧化钠溶液,完全反应后分液
溶液既可鉴别乙烷和乙烯,又可除去乙烷中少量的乙烯
C . 乙烷中有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷
D . 己烷中溶有溴单质,可加足量氢氧化钠溶液,完全反应后分液
- 在10mL 0.01mol·L-1的纯碱溶液中,逐滴加入1.2mL 0.05mol·L-1的盐酸并不断搅拌,完全反应后在
- I’m now in hospital ________(恢复)from liver failure.
- 地球的外部圈层包括( )①大气圈 ②水圈 ③生物圈 ④岩石圈A.
- “社会主义核心价值观”要求我们牢记心间,小明在“百度”搜索“社会主义核心价值观”,找到相关结果约为4280000个,数据
- 许多因素都会影响贫穷,教育也许是其中之一.在研究这两个因素的关系时,收集了美国50个州的成年人受过9年或更少教育的百分比
- 阅读下面一首唐诗,回答问题。 谢亭送别 许浑 劳歌一曲解行舟,红叶青山水急流。 日落酒醒人已远,满天风雨下西楼。 (注:
- 减数分裂与有丝分裂相比较,减数分裂所特有的是( ) A.DNA分子的复制 B.着丝点的
- 已知某植物光合作用和细胞呼吸的最适温度分别为25℃和30℃,如图为该植物在25℃条件下光合作用强度随光照强度变化的曲线图
- 设成等比数列,其公比为2,则的值为 ( ) A. B.
- 若某卫星在行星的万有引力作用下绕行星做匀速圆周运动,那么该卫星 A. 半径越大,加速度越大 B. 半
- They were swimming in the river ______ suddenly the storm st
- 下列叙述正确的是A.从海水中提取物质都必须通过化学反应才能实现 B.将盛满二氧化氮气体的试管倒立在水中,可观察到溶液充满
- 将两株植物放在封闭的玻璃罩内,用全素营养液置于室外进行培养(如甲图所示),假定玻璃罩内植物的生理状态和自然环境中相同,且
- 已知直三棱柱ABC—A1B1C1中,∠ABC=90°,AB=BC=a,AA1=2AB,M为CC1上的点.(1)当M在C1
- p{font-size:10.5pt;line-height:150%;margin:0;padding:0;}td{f
- 已知向量m=(sinA,cosA),n=,m·n=1,且A为锐角.(Ⅰ)求角A的大小;(Ⅱ)求函数的值域.
- They have to ______leaving for London because of the bad wea
- 在观察细胞有丝分裂过程中,分辨染色体形态和数目的最佳时期为() A.前期 B. 中期
- 细胞通过呼吸作用分解糖类并释放能量,主要是利用; A.麦芽糖 B.核糖 C.葡萄糖
- .2008年9月25日神舟七号载人航天飞船在我国甘肃省酒泉卫星发射中心被成功发射升空,次日16点43分(北京时间)航天员



