验证质量守恒定律 知识点题库
某反应的微观示意图如下,下列说法正确的是( )

-
(1) 图中瓶底铺细沙的作用是:.
-
(2) 白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡.结论是质量不守恒.待锥形瓶冷却后,重新放到托盘天平上称量,天平保持平衡.结论是:质量守恒.你认为结论正确的是( 填“前一种”或“后一种”).而导致另一种结论错误的原因是.
-
(3) 实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因是:.
-
(4) 由质量守恒定律可知,化学反应前后,一定不变的是.(填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类.

-
(1) 充分反应冷却后,天平仍然平衡的是(填写字母序号),该反应的化学方程式为.
-
(2) 由上述实验可知,在化学反应前后,一定不变的(填数字序号).
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质总质量
-
(3) 红热的铁能与水蒸气反应,放出气体X,同时生成固体Y.X气体靠近火焰点火时,能燃烧或发出爆鸣声.其反应的化学方程式为:3Fe+4H2O
 4X+Y.则X的化学式为,Y的化学式为.
4X+Y.则X的化学式为,Y的化学式为.
-
(1) 硝酸在工业生产中有广泛的应用,工业上制取硝酸的关键反应为:4NH3+5O2
 4NO+6R,其中R的化学式为 ;
4NO+6R,其中R的化学式为 ;
-
(2) 在小烧杯中加入硫酸铜溶液后,加入铁钉,称量总质量为m1 , 反应发生了一段时间后,再称量小烧杯及烧杯内物质的总质量为m2 , 则(填“=”、“>”或“<”)m1 m2;
-
(3) 如图所示装置,将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,一段时间后再把烧杯放在天平上称量,发现天平的指针偏右,其原因是 ,由这个实验推测:要验证质量守恒定律,有气体生成时,实验环境应在 (开放、密闭)体系中进行.


-
(1) 上述实验方案中,合理的是(填“实验1”或“实验2”)。
-
(2) 实验2中,天平的指针(填字母序号),并请解释原因。
A.向左偏转
B.不偏转
C.向右偏转
-
(3) 实验3中,点燃蜡烛后,电子秤示数逐渐减小。蜡烛减小的质量(填“大于”、“等于”或“小于”)燃烧后生成物的总质量。
-
(1) (实验回顾)
1756年,俄国化学家罗蒙诺索素夫将金属锡放在密闭容器里煅烧,冷却后在密闭容器里称量,发现总质量和煅烧前没有变化。
1774年,拉瓦锡将45.0份质量的氧化汞加热分解,恰好得到了41.5份质量的汞和3.5份质量的氧气,得到了与罗蒙诺索夫相同的结论,拉瓦锡还通过这个实验研究了,成就了化学史上的另一经典实验。
-
(2) (实验重现)
小英同学在老师的指导下,将铁粉、活性炭粉、食盐按一定比例加水混合后,涂在用铁片折成的连续的Z形架表面,然后放入盛满氧气的集气瓶中。通过如图所示装置对“化学反应中,反应物与生成物的质量关系”进行实验探究,实验过程中做到操作规范,准确称量和细致观察。
证明化学反应发生且体现质量守恒定律的现象有:,。
-
(3) 此实验用氧气替代空气的主要目的是。
-
(4) 实验室里现有过氧化氢溶液,二氧化锰粉末,以及下列仪器:

①写出编号仪器的名称:B。
②利用上述药品,仅器:制取少量纯净氧气,其简易制取装置应选择的仪器有(填序号),反应的化学方程式为,能否组装一套制氧气的装置,以控制反应的发生和停止。(填“能”或“否”),并说明理由。
-
(5) (总结与反思)
1663年,英国化学家波义耳将金属汞放在密闭容器里煅烧,冷却后称量时打开了盖,得出的结论是物质的总质量增加了,导致波义耳与质量守恒定律失之交臂,你认为质量增大的原因是:。
 B .
B .  C .
C .  D .
D . 

-
(1) A图中发生反应的化学方程式是;
-
(2) B图中把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有,这一性质在实际生活中的应用为;
-
(3) C图中通过对比,可以得出物质燃烧必须与充足的氧气接触;
-
(4) 某化学兴趣小组的同学用D图所示装置(气密性好),测定空气中氧气的含量时。装置的玻璃管中空气体积为30mL,反应前注射活塞位于10mL刻度处,反应完毕后,冷却至室温,将气球内的气体全部挤入玻璃管内,注器活塞位于2mL刻度处,则该实验测得空气中氧气的体积分数为。
-
(5) E图不能用来验证质量守恒定律,原因是。


-
(1) 实验A和B反应后天平依然平衡,由此小红认为这两个实验都能验证质量守恒定律,小亮认为小红是错误的,理由是。
-
(2) 实验B的反应化学方程式是,反应前后溶液颜色的变化是。
-
(3) 实验C反应后天平不平衡的原因是,该实验(填“符合”或“不符合”)质量守恒定律,改用装置可以直接验证质量守恒定律。
 B .
B .  C .
C .  D .
D . 

-
(1) 装置:锥形瓶的底部铺有一层细沙,其作用是。
-
(2) 燃烧前称量,锥形瓶的总质量为29.6g,则图中托盘天平中游码的读数为g。
-
(3) 白磷燃烧:白磷燃烧过程中看到的现象是。
-
(4) 燃烧后称量:发现托盘天平指针偏向右边,造成的原因可能是。
-
(5) 反思:白磷燃烧(填“遵守”或“不遵守”)质量守恒定律。

(提出问题)
两组实验都能验证质量守恒定律吗?
-
(1) (进行实验)
甲组同学在实验过程中发现,化学反应前后天平平衡,成功验证了质量守恒定律,其化学方程式为 。乙组同学在实验过程中发现天平指针向右倾斜,其原因是 。此反应 (填“遵循”或“不遵循”)质量守恒定律。
-
(2) (实验结论)
在验证质量守恒定律时,对于有气体参加或生成的化学反应,一定要在 装置中进行。
-
(3) (发现问题)
实验过后,两组同学对乙组烧杯中的废液进行了探究。废液中所含溶质是什么?
(猜想与假设)
猜想Ⅰ:只有NaCl;
猜想Ⅱ:NaCl、Na2CO3和HCl;
猜想Ⅲ:NaCl和HCl;
猜想Ⅳ:。
-
(4) (交流讨论)
经过讨论,甲组同学认为,猜想是错误的,原因是(用化学方程式回答)。
-
(5) (实验与结论)
甲组同学先将少量废液滴入试管中,然后滴入酚酞溶液,现象为 ,原因是 ,则猜想Ⅳ正确。乙组同学将少量废液滴入试管中,然后滴入氯化钡溶液,现象为 ,则猜想Ⅳ正确。
-
(6) (拓展与应用)
①若想验证猜想Ⅲ正确,可选择的试剂有(填字母序号)。
A.紫色石蕊溶液
B.铁粉
C.氢氧化钠溶液
D.碳酸钾溶液
②若猜想Ⅲ正确,想得到废液中的氯化钠固体,根据盐酸的性质,无需另加试剂,只需对废液进行操作即可。
-
(1) (实验回顾)1663年,英国化学家波义耳将汞放在密闭容器里煅烧,打开容器盖冷却后称量,得出的结论是物质的总质量增加了,导致波义耳与质量守恒定律失之交臂。
你认为质量增大的原因是。
-
(2) 1756年,俄国化学家罗蒙诺索夫将锡放在密闭容器里煅烧,冷却后在密闭容器里称量,发现总质量和煅烧前没有变化。
1774年,拉瓦锡将45.0份质量的氧化汞加热分解,恰好得到了41.5份质量的汞和3.5份质量的氧气,得到了与罗蒙诺索夫相同的结论。
(实验重现)九年级课外活动小组的同学们在期中复习时,来到化学实验室亲自对“质量守恒定律”进行了再次探究,如图是他们设计的实验,请你一起参与他们的探究活动,并回答相关问题:

实验1:称量镁条,点燃,待反应结束后,再称量。
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量。(化学方程式:Zn+2HCl=ZnCl2+H2↑)
实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量。(化学方程式:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4)
编号
实验1
实验2
实验3
反应前称重质量
9.6g
212.6g
118.4g
反应后称重质量
16.0g
212.4g
118.4g
实验1反应的化学方程式为。
-
(3) 实验1和实验2(填“符合”或“不符合”)质量守恒定律,实验正确反映了反应物与生成物的质量关系。
-
(4) 通过上述实验,可得到的启示:有气体参加或生成的反应,在验证质量守恒定律时应该注意的事项是:。
-
(5) 由质量守恒定律可知,化学反应前后,一定不变的是(填序号)。
①物质种类 ②元素的化合价 ③原子种类 ④分子种类 ⑤分子数目 ⑥原子数目
 B . 验证质量守恒定律
B . 验证质量守恒定律  C . 探究催化剂及催化作用
C . 探究催化剂及催化作用  D . 探究铁生锈的条件
D . 探究铁生锈的条件 
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1不相等;猜想2相等。
-
(1) (实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组
乙组
实验方案


实验现象
气泡产生,天平指针向右偏转
铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转
结论
猜想1正确
猜想2正确
反应的化学方程式
-
(2) (反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应,一定要在中进行。
-
(3) (优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是(填序号),理由是。

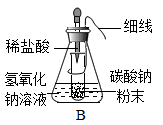
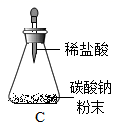
-
(4) (得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:的各物质的质量总和等于反应后生成的各物质的质量总和。
-
(5) (解释应用)解释:化学反应前后,原子的种类、数目、质量均不变,因此质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质则该固体物质一定由元素组成(填元素名称)。
 ;
;
 )
)


-
(1) 利用A实验验证质量守恒定律,气球的作用是。
-
(2) 利用B图实验不能验证质量守恒定律,因为部分生成物会以白烟的形式逸散到空气中,使得反应后质量变小,此反应的化学符号表达式为。
-
(3) 利用C、D、E实验探究,能成功验证质量守恒定律的是实验,不能验证的实验的原因是,。

①水是由氢气和氧气组成 ②该反应不遵守质量守恒定律 ③分子是在不断运动的 ④氧气能支持燃烧
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等; 猜想2:相等。
-
(1) (实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组
乙组
实验
方案


实验
现象
有气泡产生,天平指针向右偏转
铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有发生偏转
结论
猜想1正确,反应的化学方程式:
猜想2正确,反应的化学方程式:
-
(2) (反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出,导致指针向右偏转,得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在中进行。
-
(3) (优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是(填序号),从另外两种装置中任选一种指出其不足。(查阅资料知:二氧化碳易溶于NaOH溶液,生成碳酸钠)

-
(4) (得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论是的各物质的质量总和等于反应后生成的各物质的质量总和。
 B . 证明待测溶液呈碱性
B . 证明待测溶液呈碱性 C . 一氧化碳还原氧化铁
C . 一氧化碳还原氧化铁 D . 验证质量守恒定律
D . 验证质量守恒定律
- MONEY – SAVING TIPS FOR DISNEY WORLD Every time you visit Di
- .在数列{an}中,a1=,且Sn=n(2n-1)an.通过求a2,a3,a4,猜想an的表达式是________.
- 将正偶数排列如右表,其中第行第个数表示为, 例如,若,则 . 2 6 10 12 16
- 如图5-1-9所示的塔吊臂上有一可以沿水平方向运动的小车A,小车下装有吊着物体B的吊钩.在小车A与物体B以相同的水平速度
- 半坡人和河姆渡人生活的共同点是 A.普遍使用打制石器 B.制造陶器 C.种植粟、水稻
- 古诗文默写(每条横线上填写一句)(12分)(1)过尽千帆皆不是, 。(温庭筠《望江南》)(2) 马作的卢
- 已知向量a=(1,1),b=(1,-1),将下列向量表示成xa+yb的形式.(1)p=(2,3);(2)q=(-3,2)
- 等差数列的前项和为30,前项和为100,则它的前项和是( ) A.130 B.170
- Mr. White went to Hongkong and hesent me a letter.
- 小明在文峰大世界买了个MP5,开机后小喇叭里响起了动听的歌声,他说:“是周杰伦在演唱.”他的判断是根据声音的______
- “安”意义相同的一组是 A.风雨不动安如山 何故置某于安闲之地 B.然后得一夕之安寝 则宜抚安,与结盟
- 将6-―+写成省略加号的和的形式为 ( )A.-6-3+7-2 B. 6-3-7-2
- 近年来,我国东部沿海地区工业生产面临“用工荒”局面。根据相关知识和左下图,完成18-19题。 18.图中是4种工
- 13把第三大题文言文阅读材料中画线的语句翻译成现代汉语。 1)谢曰:“老母八十,疾病须养,居贫,朝夕无储,乞少置衣粮。”
- 汽车尾气是导致酸雨的重要原因之一,为减少有害气体的排放,人们在汽车排气管上安装“催化转换器”,发生反应的微观示意图如图G
- 董仲舒在改造儒家思想的过程中,主要吸收了 ① 法家的思想 ② 墨家的思想 ③ 道家的思想 ④ 阴阳五行
- That is Beckham. He was born ________ 1975. A. at
- 设函数的定义域为,如果对于任意的,存在唯一的,使得 成立(其中为常数),则称函数在上的均值为, 现在给出下列4个函数:
- 如图所示,在水平面上有一个质量为m的小物块,在某时刻给它一个初速度,使其沿水平面做匀减速直线运动,其依次经过A、B、C三
- 下列各组词语中,字形全都正确的一项是 () A.荣膺众望所归瞻顾韦编三绝 B.



