酸碱指示剂的性质及应用 知识点题库
选项 | 实验操作 | 现象 | 结论 |
A | 用黄铜片在铜片上刻画 | 铜片上有划痕 | 黄铜的硬度比铜大 |
B | 用小木棍蘸少量浓硫酸 | 木棍变黑 | 硫酸有强酸性 |
C | 向某溶液中滴入无色酚酞试液 | 无色酚酞试液不变色 | 无色溶液一定是酸 |
D | 向某溶液中滴入稀硫酸 | 有气泡产生 | 该物质一定含CO32﹣ |
选项 | 物质 | 目的 | 主要实验操作 |
甲 | CO、CH4气体 | 鉴别 | 点燃,火焰上方罩干冷烧杯,观察现象 |
乙 | Na2CO3(NaOH)溶液 | 检验 | 滴加酚酞试液,观察溶液颜色的变化 |
丙 | HCl(H2SO4)固体 | 除杂 | 加入适量BaCl2溶液 |
丁 | MnO2、KCl 固体 | 分离 | 溶解、过滤、洗涤、烘干、蒸发 |
-
(1) 维生素C(C6H8O6)的相对分子质量为176,其计算式为。
-
(2) 取维生素C片溶于水,滴入紫色石蕊溶液变红色,说明其溶液显(填“酸”或“碱”)性。

-
(1) 设备4中经过操作,将水和石膏固体进行分离。
-
(2) 设备1的作用是通过喷淋水脱去烟气中的SO2 , 生成一种酸——亚硫酸(H2SO3),该反应的化学方程式为。
-
(3) 若将二氧化硫气体通入紫色的石蕊溶液中,猜想可能出现的现象是。
-
(4) 脱硫工艺流程中。可以循环利用的物质是。
| 方案 | 实验目的 | 实验设计 |
| A | 除去KCl中混有的少量KClO3 | 取样,加入二氧化锰充分加热 |
| B | 除去氧化钙中少量的碳酸钙 | 取样,加入足量的水,溶解、过滤 |
| C | 除去氮气中含有少量的氧气 | 通过灼热的铜网 |
| D | 探究稀盐酸与氢氧化钠溶液是否恰好完全反应 | 向反应后的溶液中滴加酚酞溶液 |

-
(1) A实验中观察到的现象是
-
(2) B实验中发生反应的化学方程式为
实验完毕后,小亮同学在整理仪器时,将上述实验后的废液倒入同一个洁净的成液缸中,发现混合后的废液仍然浑浊并显红色,于是引起了他的质疑和探究兴趣。
-
(3) (提出问题)混合废液中可能含有的碱性物质有哪些?
(作出猜想)他断定混合废液中一定含有氢氧化钠,理由是;并对是否含有其它碱性物质作出猜想:猜想Ⅰ:
 ;猜想Ⅱ:
;猜想Ⅱ: 
-
(4) (实验验证)小亮认为只要用反应物(饱和石灰水和碳酸钠溶液)就可以验证猜想。于是他对混合废液进行过滤,并取少量滤液进行了下列实验:
实验操作
实验现象
实验结论
 M是
M是猜想Ⅱ错误
 N是
N是猜想Ⅰ正确
-
(5) (反思与交流)
验证完毕,小刚同学受到启发,于是他又设计了一个实验,进一步验证混合废液中含有的碱性物质。他取一定最的滤液于试管中,然后逐滴滴加稀盐酸至过量,反应过程和产生的现象如图所示。分析图象数据可以得出混合废液中含有的碱性物质一定是

-
(6) (拓展应用)为了把以上废液安全排放,你的做法是。

-
(1) 课外小组的同学自制一块多槽铁板,设计如图A所示装置,用以探究燃烧的条件。(说明:金属板上白磷足量)。请回答下列问题
①证明可燃物燃烧需要一定温度的依据是。
②将过氧化氢溶液滴入盛有MnO2的金属槽中,发生反应的化学方程式。
③有同学提出“将NaOH换成水,然后将水换成浓硫酸,也可以完成探究活动“,你认为是否可行,为什么?
-
(2) 如图B所示的装置进行验证质量守恒定律,试剂a可以是(写出一种即可)。证明质量守恒定律成立的现象是。
-
(3) 根据如图C所示实验,Y烧杯中溶液由红色变为无色。
①该实验可证明微粒具有的性质是。
②请用化学方程式表示红色变为无色的原因。
③该实验得出氢氧化钡的化学性质有。
|
物质 |
①水 |
②水垢清除剂 |
③肥皂水 |
④白醋 |
⑤雪碧 |
|
颜色 |
紫色 |
红色 |
蓝色 |
红色 |
红色 |
判断上述物质中,显酸性的有(填序号)。

试管编号 | ① | ② | ③ | ④ |
试管内试剂 | NaOH溶液 | MgCl2溶液 | Na2CO3溶液 | Ba(NO3)2溶液 |
加入稀硫酸后的现象 | 无明显现象 | 无明显现象 | 产生气泡 | 白色沉淀生成 |
-
(1) 根据以上实验现象,可以判断试管③④中发生了复分解反应。小明同学向盛有NaOH溶液的试管中先加了一种试剂,再加稀硫酸,从而能说明试管①中也发生了反应,这种试剂是。
-
(2) 为了验证试管②中是否发生复分解反应,小明同学进行了如下探究。
[提出猜想]
猜想1:试管②中没有发生复分解反应,溶液中有MgCl2 , 即Mg2+和Cl﹣同时存在溶液中。
猜想2:试管②中发生了复分解反应,溶液中无MgCl2。
老师提示
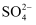 会对Cl﹣的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了如图实验方案。
会对Cl﹣的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了如图实验方案。[设计方案]

沉淀A的化学式是。老师评价该方案时指出:设计思路正确,但试剂选择有误,你认为证明猜想1正确,修改后的实验方案是。(写出操作和现象)
-
(3) [实验反思]小明反思进行步骤Ⅲ时,加NaOH溶液采用了滴加的方式,但没有立即观察到任何现象,你认为其中的原因是。

-
(1) 第一步后,溶液为无色的孔穴有(填孔穴序号)。
-
(2) 第二步后,孔穴1中发生反应的化学方程式为。
-
(3) 第二步后,孔穴2、3的溶液均变成红色,说明Na2CO3溶液显(填“酸”或“碱”)性,此时孔穴2的溶液中含有的溶质是。
- 22.在下面一段文字横线处补写恰当的语句,使整段文字语意完整连贯,内容贴切,逻辑严密。每处不超过12个字。一个人总是上网
- 可一次鉴别出氧气、空气、二氧化碳三瓶气体的方法是 A.加入紫色石蕊试液 B.
- 某有机物分子,仅由 C、H、O 三种元素组成,分子中含13 个原子,其分子中的电子总数为 42。充分燃烧该有机物,所生成
- 下图中的材料反映了林则徐:A.热爱和平的愿望 B.对贪生怕死的鄙
- 细胞是生物体结构和功能的基本单位,下列关于真核生物的细胞叙述正确的是 A.有中心体的细胞一定是动物细胞
- 如图12-6-5所示是水平面上两列频率相同的波在某时刻的叠加情况,图中实线为波峰,虚线为波谷.已知两列波的振幅均为2 c
- 除去H2中的HCl和水蒸气,下列装置和药品均正确的是( )
- 某同学在实验室做如下实验。 A
- 艺术创作反映了时代特征,下图可以直接用于研究的主题是 ( ) A.三大改造和“一五
- 下图为巴厘岛示意图,其中最高点的海拔3142米。读图回答16-17题。16.据图推测,巴厘岛山地走向为A.东西走向 B
- 先化简,再求值:(1+a)(1-a)+(a-2)2,其中a=-3.
- 已知抛物线与双曲线有相同的焦点,点是两曲线的一个交点,且⊥轴,则双曲线的离心率为 .
- (8分)将食物保存方法与原理对应起来(填序号,每个1分) 序号 A B C D E F G H 答案
- 请结合下列装置图回答问题:① 若向A装置中通入纯净的氢气,为检验反应产物,A装置的右边应与上面的 (21) (填字母)
- 阅读下面文字,完成17一20题。(18分)明天是农历“小年”。再过几天,“大年”在即。对过年,一方面,人们盼年、望年,千
- 《权利法案》、《独立宣言》和《人权宣言》的共同之处是 A.为改造封建制度提供了法律依据 B.都强调保障人的自由
- 若所要观察的物像位于显微镜视野的右下方,要把物象移到视野中央,应往哪个方向移动玻片标本( ) A.左上方
- 据统计,在某银行的一个营业窗口等候的人数及其相应的概率如下: 排队人数0人1人2人3人4人5人及5人以上概率0.050.
- 如下图甲所示,当开关S从点2转到1时,电流表和电压表对应的示数如图乙所示,由图甲和图乙中的信息可知,电源电压是 ▲
- 认识自然现象有助于把握人体自身生命活动规律我国古代写成的医书中反复强调“天人相应”,“人与天地相参”,医者“上至天文,下



