金属及其化合物之间的转化 知识点题库
下列哪种金属氧化物溶于水不能得到相应的碱( )
A . Na2O
B . CaO
C . K2O
D . CuO
铜片在酒精灯上加热后表面变黑,有同学认为黑色物质是氧化铜(CuO),也有同学认为黑色物质是酒精不完全燃烧生成的炭黑(C)。在下列试剂中,只要一步反应即可判断哪种观点正确的是( )
A . 蒸馏水
B . 稀硫酸
C . 氯化钡溶液
D . 氢氧化钠溶液
将CO通入盛有12g Fe 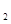 O
O 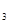 的试管内,加热反应一段时间后,停止加热,继续通入CO至试管冷却,此时试管内残留固体的质量为9.6g,则反应生成铁的质量为( )
的试管内,加热反应一段时间后,停止加热,继续通入CO至试管冷却,此时试管内残留固体的质量为9.6g,则反应生成铁的质量为( )
A . 2.4g
B . 5.6g
C . 8.4g
D . 9.6g
下列转化不能一步实现的是( )
A . CO2→O2
B . CaCO3→Ca(OH)2
C . Fe2O3→Fe
D . Cu2(OH)2CO3→CuCl2
某研究小组利用如图装置探究温度对 CO 还原 Fe2O3 的影响(固定装置略)

信息 1.难溶的碳酸盐受热易分解为氧化物和 CO2
信息 2.CO2 能与 Zn 反应生成 CO 气体
信息 3.酒精灯的加热温度 400-500℃,酒精喷灯的火焰温度可达 1000℃左右
-
(1) D 装置的加热必须在 A 和 B 装置加热一段时间后再进行,这样做的原因是;
-
(2) 装置 C 的作用是,从实验安全或环保角度考虑,上述实验装置可采取的改进措施是 。
-
(3) 将研究小组分为两组,按上图所示装置进行对比实验,甲组在用酒精灯、乙组用酒精喷灯对装置 D 加热,反应产物均为黑色粉末(纯净物)。两组分别用产物进行以表实验:
步骤
操作
甲组现象
乙组现象
1
取黑色粉末加入盐酸
溶解,无气泡
溶解,有气泡
2
取步骤1中溶液,滴
加KSCN溶液
变红
无现象
则乙组装置 D 中反应的化学方程式。
在甲物质中,逐滴加入乙物质的溶液至过量,下列甲、乙组合中不能正确反映右图中生成沉淀或气体的质量(m1)与加入乙溶液的质量(m2)的关系是( )

选项 | 甲 | 乙 |
A | 部分变质的烧碱溶液 | HCl |
B | 少量硝酸酸化的硫酸铜溶液 | NaOH |
C | 少量硝酸酸化的硫酸镁溶液 | Ba(OH)2 |
D | 久置空气中的铝片 | H2SO4 |
A . A
B . B
C . C
D . D
黄铜(由铜和锌形成的合金)有较强的耐磨性能,在生活中有广泛的用途。晓军同学为 了测定黄铜屑样品组成,分四组取样品与稀硫酸反应,其实验数据记录如下表:
样 品 | 第 1 份 | 第2份 | 第3份 | 第4份 |
取样品质量(g) | 25.0 | 25.0 | 25.0 | 25.0 |
取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
产生气体质量(g) | 0.2 | 0.4 | 0.5 | m |
试计算:
-
(1) 上表中 m 的数值是;
-
(2) 通过分析上述数据可知,当黄铜样品和稀硫酸的质量比为时,两者恰好完全 反应;
-
(3) 求所用稀硫酸中硫酸的质量分数?
根据图示变化,回答问题:

-
(1) 写出氧化铜和稀硫酸反应的化学方程式;
-
(2) 下列有关分析合理的是 。(选填字母)A . 烧杯②中溶液一定含有硫酸 B . 烧杯③中溶液一定没有硫酸 C . 烧杯③中溶液一定为硫酸亚铁溶液 D . 烧杯③中的固体一定含铜
根据图甲、乙、丙三种物质的转化关系,推测甲为( )

A . 铜
B . 碳酸钠
C . 氧化铜
D . 氢氧化钡
下图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“一”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。

-
(1) A物质是 (填化学式)。
-
(2) C与E反应的基本类型是。
-
(3) 从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有(填序号)。
①2类 ②3类 ③4类 ④5类
下列选项所示的物质转化均能一步实现的是( )
A .  B .
B .  C .
C .  D .
D . 
在实验室里进行物质制备,下列从原料及有关试剂分别制取相应的最终产物的设计中, 理论上正确、操作上可行、经济上合理的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
如图,给出了三种物质可能存在的转化关系,根据所学的物质性质及化学变化规律,判断下列选项正确的是( )

A . 实现①转化,可加入氧化铜
B . 实现②转化,可通入CO2
C . 实现③转化,可加入稀盐酸
D . 能一步实现转化的是④
小科同学在学习了金属、金属氧化物和碱之间的相互关系后,发现如下规律:金属+O2→金属氧化物,金属氧化物+H2O→碱。请你根据这一规律,写一个金属氧化物和水反应生成碱的化学方程式:。
是不是所有的金属氧化物都能和水反应生成对应的碱?(选填“是”或“不是”)。
建兰中学兴趣小组同学要从含有氯化钠、氯化铜和氯化亚铁的某废液中,回收铜并得到铁红(主要成分Fe2O3),设计了如图所示实验方案,要求全过程不引入其他金属元素,请回答:

-
(1) A物质是(写化学式)。
-
(2) 步骤②中加入过量盐酸的目的是。
-
(3) 溶液丙中溶质是(写化学式)
下面是制取MgSO4的四种方法不可行的是( )
A . Mg+H2SO4═MgSO4+H2↑
B . MgO+H2SO4═MgSO4+H2O
C . MgCO3+H2SO4═MgSO4+H2O+CO2↑
D . Mg(OH)2+CuSO4═Cu(OH)2↓+MgSO4
如图中“—”表示相连的物质之间可以发生反应,“”表示一种物质可以转化成另一种物质,下列各组物质按甲、乙、丙的顺序不符合图示要求的是( )

A . C、CO、O2
B . Mg、MgCl2、ZnSO4
C . Ca(OH)2、CaCl2、Na2CO3
D . BaCl2、BaCO3、H2SO4
某化工厂排放的废液中只含有ZnCl2和CuCl2两种溶质,为回收金属Cu并得到ZnCl2固体,某科学实验小组的同学们设计并进行了如下实验,请回答下列问题

-
(1) 步骤一中,加入的物质A的目的是。
-
(2) 步骤二中,加过量的稀盐酸后滤液Ⅱ所含的溶质有。
-
(3) 步骤三蒸发结晶时用到玻璃棒,玻璃棒的作用是。
在盐酸中加入过量的某种金属粉末,反应的微观模型如图所示,图中圆圈表示该反应前后溶液中存在的主要离子。

-
(1) 该金属粉末可能是 。A . Cu B . Mg C . Al D . Na
-
(2) 图中“
 ”所代表的离子是(填离子符号)。
”所代表的离子是(填离子符号)。
Fe(OH)2是白色难溶于水的物质,可用于制颜料、药物等,但很容易被空气中的氧气氧化为Fe(OH)3 , 氧化过程中白色沉淀转化为灰绿色沉淀,最后变为红褐色沉淀。现用铁片、稀盐酸、氢氧化钠溶液、水等试剂制取少量的Fe(OH)2 , 装置如图。

-
(1) 检查气密性。关闭阀门A和B,让1中液体进入到容器2中。虚线框所在装置,发生的反应的化学方程式是。
-
(2) 容器 2 中充满氢气后,打开阀门 A, 关闭阀门 B, 应出现的现象是。
-
(3) 实验完毕,关闭阀门A和B,制得的Fe(OH)2在容器(选填“3”或“4”) 中。
-
(4) 本实验中所有配制溶液的水需煮沸,容器2、3均密闭,其主要原因是。
最近更新
- 关于《繁星·春水》,下列说法有误的一项是(2分)( ) A、作者冰心,以宣扬“爱的哲学”著称。 B、诗作以“小
- 电荷量为3e的带正电的微粒,自匀强磁场a点如图甲射出,当它运动到b点时,与一个静止的电荷量为e的带负电的微粒碰撞并结合
- 目前,活跃在城乡的以小型企业、微型企业、城乡个体工商户、创业者和农户为主的“草根经济”群体,是我国社会经济中最具活力的部
- 正八边形的每个内角为()A.120º B.135º C.140º
- 用 a, an, the ,\ 填空 1. What ______ fine weather we havetoday!
- 函数的反函数的定义域为 ( ) A. B. C.
- 一般来说,当经济过热、物价上涨幅度过大时,政府为抑制社会总需求,保持经济稳定增长所采取的手段中属于财政政策的是
- 对于已知直线a,如果直线b同时满足下列三个条件:①与直线a异面;②与直线a所成的角为定值③与直线a的距离为定值d,那么这
- 关于物体的重心,下列说法中正确的是( )A.重心就是物体上最重的一点B.任何形状规则的物体,它的重心一定在几何中心
- 函数, (1)用定义证明是偶函数; (2)解不等式:.
- 设y=-2exsinx,则y′等于()A.-2excosxB.-2exsinxC.2exsinxD.-2ex(si
- 从海带中提取碘要经过灼烧、浸取、过滤、氧化、萃取、分液、蒸馏等操作,下列对应的装置合理,操作规范的是( )
- 阅读下面的文字,完成ll一l4题。 文人的“面子”与文化的“底子” 王呈伟 (1)这个时代的一些文化名人很讲究面
- 下列句子没有语病的一句是( ) A.他以瑰丽的语言,优美的表达技巧,深刻感人的情愫,在诗中表达了人民群众对美好
- 下列物质中硫元素的化合价为+4价的是 A. S B.H2S
- 某英文网站正在开展关于“高二是否该分文理科”的讨论。请你根据下面所给的要点提示,用英语写一篇短文,描述目前存在的两种看法
- 2013年7月,国务院常务会议研究推进政府向社会力量购买公共服务,根据会议要求,各地要在准确把握公众需求的基础上,制定政
- ---Where do you work? --- Pardon. --- Could y
- 下列关于实验室用高锰酸钾制取氧气的说法正确的是()。 A.发生装置选用长颈漏斗和锥形瓶 B.反应不需要加热 C.实验时先
- 1.下列各句中加横线成语的使用,全部都正确的一项是( ) A.父亲收藏的那些产于不同时代、具有不同造型、来自不同国家



