质量守恒定律及其应用 知识点题库
实验一:称量镁条,点燃,待反应结束后,再称量;
实验二:将盛有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,充分反应后再称量。
实验三:将盛有氢氧化钠溶液的试管放入盛有硫酸铜溶液的烧杯中,称量,然后设法使两种溶液混合,充分反应后再称量。三位同学得到的实验数据如下表:
编号 | 实验一 | 实验二 | 实验三 |
反应前 | 4.8 g | 112.6 g | 118.4 g |
反应后 | 8.0 g | 112.4 g | 118.4 g |
-
(1) 从表面上看,这三个实验中,发生化学反应前后物质的质量(填“增大”、“减小”或“不变”):实验一,实验二,实验三;
-
(2) 造成上述结果的原因可能是;
-
(3) 在三个实验中,实验正确地反映了反应物与生成物之间的质量关系;
-
(4) 由此可得出结论:用实验研究化学反应前后反应物与生成物之间的质量关系时,必须在体系中进行。
物 质 | a | b | c | d |
反应前的质量(g) | 6.4 | 3.2 | 4.0 | 2.8 |
反应后的质量(g) | 5.2 | X | 7.2 | 2.8 |
①原子的数目 ②分子的数目 ③元素的种类 ④物质的总质量 ⑤物质的种类⑥原子的种类 ⑦原子的质量.
物质 | A | B | C | D |
反应前质量/g | 4 | 6 | 111 | 4 |
反应后质量/g | 待测 | 15 | 0 | 84 |

 B .
B .  C .
C .  D .
D . 
|
物质 |
甲 |
乙 |
丙 |
丁 |
|
反应前质量(g) |
18 |
20 |
10 |
30 |
|
反应后质量(g) |
2 |
20 |
50 |
X |
-
(1) 反应后丁物质的质量X=g;
-
(2) 该反应中甲和丙两种物质变化的质量比为;
-
(3) 该反应属于反应(填“化合”或“分解”)。
-
(1) ①设想以植物性食物为主的中国人平均食用牛肉的水平与美国人相当,则每年需增加粮食3.4亿吨(这相当于美国一年的粮食产量),如果每吨粮食生产需提供0.1吨氮元素,并且全部由尿素[CONH2)2]提供,则中国每年将需要多供应多少吨尿素?
②尿素生产原理为:CO2+2NH3
 CO(NH2)2+H2O
CO(NH2)2+H2O据此计算:为增产尿素,需建年产20万吨合成氨的工厂多少座?
-
(2) 设想中国每个家庭都有轿车,则每天需供应8000万桶石油(目前全世界每天的产油量为6700万桶),如果每7桶石油为1吨,每吨石油能提炼出70%(质量分数)的燃油,以燃油中平均含C、H原子比例为10:22计算,中国由于轿车燃油将可能每天排放温室气体多少吨?
-
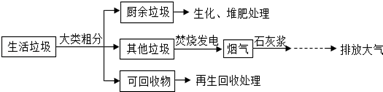
(1) 厨余垃圾“生化厌氧产沼”是指厨房垃圾经过微生物的无氧呼吸(发酵)产生CH4和二氧化碳气体,设垃圾中有机物的化学式为(CH2O)n,请写出这一反应的化学方程式
-
(2) 具有哪些特点的其他垃圾适合焚烧发电?

[查阅资料]碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质。
[进行实验]为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氯钠到制片上加热,如右图所示。
-
(1) 加热一段时间后,观察到烧杯内壁有水珠。充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊。写出该反应的化学方程式:。
-
(2) 兴趣小组的同学认为充分加热后的这种固体产物可能是NaOH或Na2CO3。
①他们猜想的理论依据是 。
②请设计实验来检验反应后的固体产物是NaOH还是Na2CO3 , 并填入下表:
实验操作
预期实验现象
结论
方案一:取少量反应后的固体产物溶于水,加入适量氯化钙溶液
固体产物是Na2CO3 , 而不是NaOH。
方案二:
产生大量气泡
固体产物是Na2CO3 , 而不是NaOH。


⑴澄清石灰水通入二氧化碳变浑浊 ⑵铁丝在氧气中剧烈燃烧
⑶实验室利用分解高锰酸钾制取氧气 ⑷用氢氧化钠溶液吸收二氧化硫气体
⑸实验室利用石灰石和稀盐酸制取二氧化碳 ⑹硫酸铜溶液和氢氧化钠反应
其中属于分解反应的是(填编号)
反应(2)的实验现象 反应(6)的实验现象


实验主要操作如下:
Ⅰ.检查装置气密性后装入剪碎的塑料瓶;断开丙、丁装置
Ⅱ.打开甲中分液漏斗活塞,注入双氧水后,关闭活塞
Ⅲ.一段时间后连接丙、丁装置,点燃酒精灯,观察到塑料燃烧,充分然烧后丙装置有固体残留。
Ⅳ.熄灭酒精灯,继续通入氧气直至玻璃管冷却实验测定数据如下:
|
丙中固体 |
丁装置 |
戊装置 |
己装置 |
|
|
实验前 |
5.0g |
118.2g |
224.6g |
148.0g |
|
实验后 |
m |
123.6g |
237.8g |
148.0g |
-
(1) 己装置的作用是。
-
(2) 操作Ⅳ中通入氧气的作用是。
-
(3) 若该实验不用纯氧气,而是通入空气,依据丙、丁装置质量变化计算会使测定的C、H元素的质量比(“偏大”、“偏小”或“无影响”),原因是。
-
(4) m的值为。
 ZnO+CO2↑;②C+2ZnO
ZnO+CO2↑;②C+2ZnO  2Zn+X↑。下列说法正确的是( )
2Zn+X↑。下列说法正确的是( )
-
(1) 此反应前后,该催化剂的化学性质和保持不变。
-
(2) 只用CO2一种反应物通过该催化剂 (选填“能”或“不能”)转化成甲酸(CH2O2),理由是。
- 分子式为C63H103O45N17S2的化合物很可能是()A. 肌糖元 B. 蛋白质 C. 核酸 D. 脂类
- 某肽链由51个氨基酸组成,如果用肽酶把其分解成1个二肽、2个五肽、3个六肽、3个七肽,则这些短肽的氨基总数的最小值、肽键
- 我国少数民族数目最多的省区是( )A .河南省B .内蒙古自治区C .新疆维吾尔自治区D .云南省
- 下面是一同学搜集到的单元知识卡片,请你按要求帮他修正错误。(7分) ①在我国诸葛亮是家喻户晓的人物,有关他的成语、俗语、
- 7.下列说法不正确的一项是( ) A.《杜工部集》(杜甫)以官爵命名,《范文正公集》(范仲淹)以谥号命名,《贾长沙集》
- 蛋白质是细胞内最重要的生命物质之一,具有多样性和特异性,其结构与功能是相适应的。下列蛋白质类物质与其功能对应正确的是()
- 若多项式x2+kx-2x+3中不含有x的一次项,则k=_______.
- 你身边的每个人对你来说都具有特殊的意义。请以“My special ________”为题用英语写一篇短文,描述你家庭的
- If it looks like a fish and swims like a fish, it usually is
- Hawking became world-famous in _______. A.his thirties in th
- 村民自治的基础和村民参与民主管理的主要途径是A.自己选举当家人 B.制定村
- 一质点分别受到下列几组共点力的作用,一定能使质点产生加速度的是( )A.25N,15N,40N B.10N,15N
- —Thecompany has been performing poorly during the past few y
- 24.阅读下面材料,根据要求作文。(60分) 正方形和圆形是生活中最常见图形,人们也由此联想到人自身的一些品格——有人认
- 下列物质中由同种分子构成的是( ) A.冰水混合物 B.水银 C.空气 D.稀有气
- 改革是需要智慧的,措施出台的先后顺序,推进步伐的轻重缓急等等都很重要,这些细节可能会决定或影响改革的成与败。阅读材料,回
- 铝能制成铝箔是因为铝具有 A.延展性 B.导热性 C.导电性 D.抗腐蚀性
- 如图所示的电路中,电池的电动势为E,内阻为r,电路中的电阻R1、R2和R3的阻值都相同。在电键S处于闭合状态下,若将电键
- 下列句子中,没有语病的一项是 ( )(2分) A.在大家的百般劝慰下,他终于打消疑虑,道出了难言之隐的苦衷。 B.
- —Whichdo you prefer, rice or noodles? —__________, thanks



