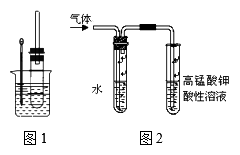
溴乙烷的制取 知识点题库
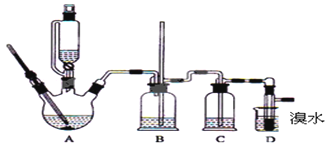
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g•cm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣l30 | 9 | ﹣1l6 |
回答下列问题:
-
(1) 烧瓶A中发生的主要的反应方程式:
-
(2) 安全瓶B可以防倒吸,并可以检查实验进行时试管D是否发生堵塞.请写出发生堵塞时瓶B中的现象:
-
(3) 在装置C中应加入 (填字母),其目的是
a.水 b.浓硫酸 c.氢氧化钠溶液
-
(4) 若产物中有少量未反应的Br2 , 最好用 洗涤除去.(填字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
-
(5) 若产物中有少量副产物乙醚,可用 的方法除去.
-
(6) 反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是
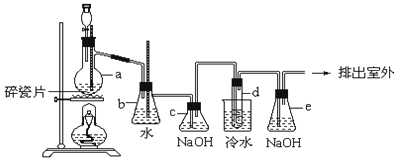
-
(1) 请写出烧瓶a中发生的化学反应方程式:
-
(2) 安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象:
-
(3) c装置内NaOH溶液的作用是 ;e装置内NaOH溶液的作用是
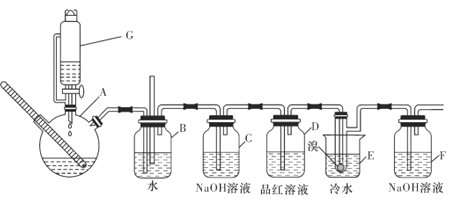
有关数据列表如下:
乙醇 | 1.2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g/cm) | 0.79 | 2.2 | 0.71 |
沸点/ | 78.5 | 132 | 34.6 |
熔点/ | ﹣130 | 9 | ﹣116 |
请按要求回答下列问题:
-
(1) 装置G的名称为 ,G中药品为1,3的无水乙醇和浓硫酸混合液,写出制备乙烯的化学反应方程式:
-
(2) 装置B中长直导管的作用是
-
(3) 反应过程中应用冷水冷却装置E中大试管,但又不能过度冷却(如用冰水),其原因是
-
(4) 某学生发现反应结束时,G中试剂消耗量大大超过理论值(装置不漏气),其原因是
-
(5) 有学生提出,装置F中可改用足量的四氯化碳液体吸收多余的气体,其原因是
-
(6) 若消耗无水乙醇的体积为100mL,制得1,2一二溴乙烷的体积为40mL,则该反应的产率为
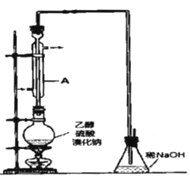
-
(1) 装置A的作用是
-
(2) 反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生,该气体的分子式是
-
(3) 反应结束后,得到的粗产品呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的 (填写上正确选项的字母).
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳
-
(4) (3)中实验操作中所需的主要玻璃仪器是 (填仪器名称)
-
(5) 要进一步制得纯净的溴乙烷,司继续用蒸馏水洗涤,分液后,再加入无水CaCl2 , 然后进行的实验操作是 (填写正确选项的字母).
a.分液 b.蒸馏 c.萃取
-
(6) (6)为了检验溴乙烷中含有溴元素,通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号).
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液.
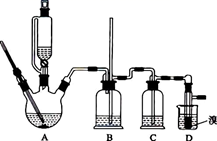
实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5﹣OH+HBr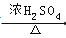 C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30mol NaBr(s);0.25mol C2H5OH(密度为0.80g/cm3);36mL浓H2SO4(质量分数为98%,密度为1.84g/mL);25mL水.试回答下列问题:
-
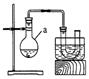
(1)
该实验应选择下图中的a装置还是b装置? .(填字母)
-
(2) 反应装置中的烧瓶应选择下列哪种规格最合适 (填字母)
A.50mL B.100mL C.150mL D.250mL
-
(3) 冷凝管中的冷凝水的流向应是 (填字母)
A.A进B出 B.B进A出 C.从A进或B进均可
-
(4) 实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是
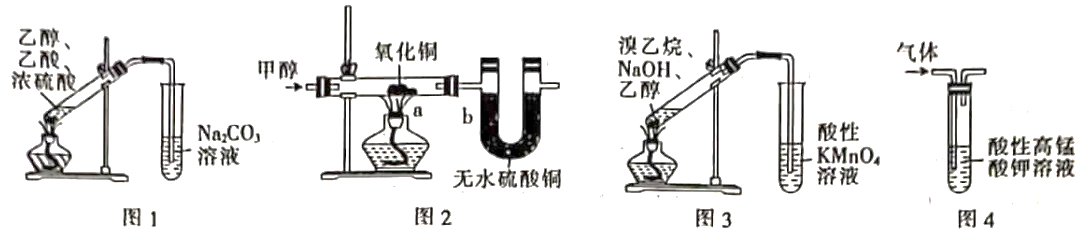
实验原理:CH3CH2Br+NaOH CH2+NaBr+H2O
CH2+NaBr+H2O
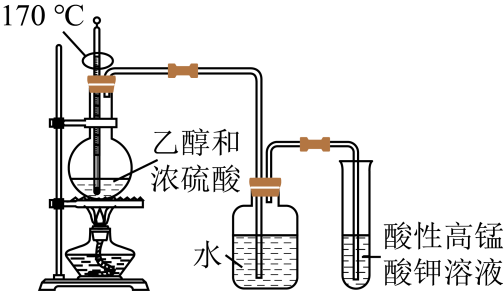
实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象.一段时间后,观察到酸性KMnO4 . 溶液颜色褪去.
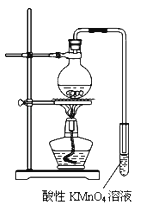
-
(1) 甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因:
-
(2) 丙同学认为只要对实验装置进行适当改进,即可避免对乙烯气体检验的干扰,改进方法:
-
(3) 改进实验装置后,再次进行实验,却又发现小试管中溶液颜色褪色不明显.该小组再次查阅资料,对实验进行进一步的改进.
资料一:溴乙烷在55℃时,在饱和氢氧化钠的乙醇溶液中发生取代反应的产物的百分比为99%,而消去反应产物仅为1%.
资料二:溴乙烷发生消去反应比较适宜的反应温度为90℃~110℃,在该范围,温度越高,产生乙烯的速率越快.
资料三:溴乙烷的沸点:38.2℃.
(3)结合资料一、二可知,丙同学改进实验装置后,溶液颜色褪色不明显的原因可能是 此时发生反应的化学方程式为:
-
(4) 结合资料二、三,你认为还应该在实验装置中增加的两种仪器是:① ,②
如图是实验室用乙醇与浓硫酸和溴化钠反应制备溴乙烷的装置,图中省去了加热装置.有关数据见表:
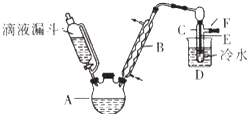
乙醇、溴乙烷、溴有关参数
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度/g•cm﹣3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
-
(1) 制备操作中,加入的浓硫酸必需进行稀释,其目的是.
a减少副产物烯和醚的生成 b.减少Br2的生成c减少HBr的挥发 d.水是反应的催化剂
-
(2) 加热的目的是(从速率和限度两方面回答);应采取的加热方式是.
-
(3) 为除去产品中的一种主要杂质,最好选择下列溶液来洗涤产品.A . 氢氧化钠 B . 碘化钠 C . 亚硫酸钠
-
(4) 第(3)步的实验所需要的主要玻璃仪器是.
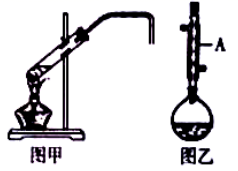
-
(1) 仪器a的名称是。
-
(2) 在大烧杯中加入冰水的目的是。
-
(3) 加入碎瓷片的作用是。
-
(4) 为了更好的控制温度,选择常用的加热方式为。
-
(5) 反应时若温度过高,可看到有红棕色气体产生,该气体分子式为,生成的无色刺激性气味气体的分子式为。
-
(6) U形管内可观察到的现象是。
-
(7) 反应结束后,U形管内粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可以选择下列试剂中的________(填序号)。A . Na2SO3溶液 B . H2O C . NaOH溶液 D . 苯
-
(8) 检验溴乙烷中溴元素的实验步骤是:取少量溴乙烷于试管中,加入NaOH溶液,加热煮沸一段时间,冷却,。
NaBr+H2SO4═HBr+NaHSO4 ①
C2H5﹣OH+HBr⇌C2H5﹣Br+H2O ②
CH3CH2CH2CH2﹣OH+HBr⇌CH3CH2CH2CH2﹣Br+H2O ③
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br﹣被浓硫酸氧化为Br2等。有关数据列表如下;
| 乙醇 | 溴乙烷 | 正丁醇 | 1﹣溴丁烷 | |
| 密度/g•cm﹣3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 111.6 |
请回答下列问题:
-
(1) 图乙中仪器A的名称为。
-
(2) 乙醇的沸点高于溴乙烷的沸点,其原因是。
-
(3) 将1﹣溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在(填“上层”、“下层”或“不分层”)。
-
(4) 制备操作中,加入的浓硫酸必需进行稀释,其目的是_____。(填字母)A . 减少副产物烯和醚的生成 B . 减少Br2的生成 C . 减少HBr的挥发 D . 水是反应的催化剂
-
(5) 欲除去溴代烷中的少量杂质Br2 , 下列物质中最适合的是_____。(填字母)A . NaI B . NaOH C . NaHSO3 D . KCl
-
(6) 制备溴乙烷(图甲)时,采用边反应边蒸出产物的方法,其有利于;但制备1﹣溴丁烷(图乙)时却不能边反应边蒸出产物,其原因是。
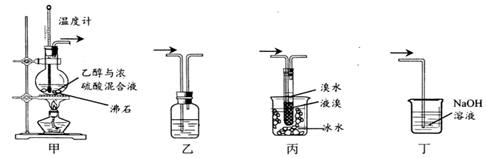
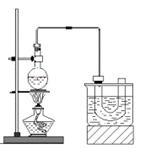
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。
请回答下列问题:
-
(1) 已知烧瓶中制备溴乙烷时包含两个反应,写出反应②:
①NaBr+H2SO4=HBr+NaHSO4
②
-
(2) 溴乙烷的水溶性(填“大于”“等于”或“小于)乙醇的水溶性,其原因是。
-
(3) 反应时若温度过高,会有多种有机副产物生成,写出相应的化学方程式(任写一个)
-
(4) 反应结束后,U形管中制得的溴乙烷呈棕黄色。为了除去产品中的杂质,可选择下列试剂中的填序号)。
A.H2O B.Na2SO3溶液 C.CCl4 D.NaOH溶液
除杂所需的主要玻璃仪器是(填仪器名称)
-
(5) 检验溴乙烷中溴元素:取少量溴乙烷,然后(按正确的操作顺序填序号)。
①加热:②加入AgNO3溶液:③加入稀HNO3酸化; ④冷却;⑤加入NaOH溶液
有关数据列表如下:
| 物质名称 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/(g·cm -3) | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
-
(1) 装置A 中发生的化学方程式为 ,反应类型为 ,在此制备实验中,要尽可能迅速地把反应温度提高到 170 ℃左右,其最主要目的是 (填字母)。
a.引发反应 b.防止乙醇挥发 c.减少副产物乙醚生成 d.加快反应速率
-
(2) 装置B 的作用是 ,在装置C 中应加入 (填字母),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
-
(3) 装置D 中实验现象为 。
-
(4) 将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 (填“上”或“下”)层。
-
(5) 反应过程中应用冷水冷却装置 D,其主要目的是 ;不用冰水原因 。
-
(6) 若制得的产物中混有乙醚,得到纯净的产物的操作是。
选项 | 目的 | 方案设计 | 现象和结论 |
A | 探究乙醇消去反应的产物 |
| 酸性高锰酸钾溶液褪色,说明乙醇消去反应的产物是乙烯 |
B | 比较乙酸、碳酸和苯酚的酸性强弱 |
| 若a装置中有气泡,c装置中出现浑浊,说明酸性:乙酸>碳酸>苯酚 |
C | 检验1-溴丁烷中的溴元素 | 向试管中加入几滴1-溴丁烷,加入2mL5%的NaOH溶液,振荡后加热。反应一段时间后停止加热,静置后取数滴水层液体于另一只试管中,加入几滴2% | 若出现淡黄色沉淀,说明有机物中有溴元素 |
D | 检验淀粉在稀硫酸作用下是否发生了水解 | 向试管中加入0.5 g淀粉和4 mL 2 mol/L | 若未出现砖红色沉淀,说明淀粉未发生水解 |
下列说法错误的是( )
 溶液)→水洗”可除去大部分杂质
溶液)→水洗”可除去大部分杂质
- 实验测得小麦、大豆、花生三种生物干种子中三大类有机物含量如图,有关叙述正确的是A.选用花生检验细胞中有脂肪存在时需要使用
- 解放战争时期,我军开始在数量上超过敌人是在 A.粉碎敌人重点进攻后
- 已知,则的值等于_______
- 农田生态系统属于人工生态系统。 ( )
- 下列各项中,属于中华民国第一届参议院的历史贡献的是
- 如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是(
- 下列关于细胞内蛋白质和DNA 的叙述,正确的是( )A .组成元素相同B .都有特定空间结构C .都在核糖体上合成D .
- 丝瓜俯视着南瓜说:“我的藤蔓很长,可以爬得很高。清晨能看到朝阳冉冉升起,傍晚能看到夕阳徐徐落下。”南瓜说:“我的果实很重
- 如图所示,物体m静止放在粗糙的斜面上。一平行斜面的推力F作用在物体上,现让F逐渐增大至某一值,物体始终保持静止状态。则在
- 小明家新买了一台饮水机,小明的父母经常为夜间是否要关闭饮水机而发生争执:妈妈认为关机可以节省电能,理由是饮水机在夜间无人
- 生物界在基本组成上的高度一致性表现在 ( ) ①组成生物体的化学元素基本一致 ②各种生物体的核酸都相同 ③构成核酸的碱基
- 下面句子的横线上,应填入的词语最恰当的一项是 ①、廊子大多是两边无所_________的,实际是隔而不离,界而未界。 ②
- 下列设计的实验方案能达到实验目的是 A.制备Fe(OH)2:用图1所示装置,向试管中加入NaOH溶液,振荡 B.测
- 如图,在⊿ABC中,AB=BC。以AB为直径作圆⊙O交AC于点D,点E为⊙O上一点,连接ED并延长与BC的延长线交于点F
- 利用蛋白质工程改造天然蛋白质,进而改变其功能,获得毒副作用很小、专一性增强、药效加强、稳定性增强的理想的药物。如胰岛素是
- 下列关于传染病的叙述中,正确的是( )A.肝炎是由病原体引起的 B.艾滋病能通过握手传播C.红
- 物价与人民生活息息相关,同时也是反映国民经济运行与发展的重要指标,是国民经济运行与发展的“晴雨表”。回答下面试题。 34
- 在光电效应现象中,要增大光电子射出的初速度,最可行的办法是A.增大入射光的强度,选用极限频率大的材料B.增大入射光的强度
- 科学家观察发现,有一种俗称“熊虫”的动物,若进入“隐生状态”(这时它们的代谢速率几乎可降至0),能耐受零下271℃的冰冻
- 用化学用语填空: (1)人体胃液中帮助消化的酸是 ; (2)2个碳酸根离子 ; (3)消石灰的主要成分 ; (4)

 溶液
溶液 溶液,加热。待冷却后向试管中加入少量新制
溶液,加热。待冷却后向试管中加入少量新制 , 加热
, 加热


