溴乙烷的制取 知识点题库
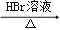
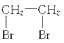 B . CH3CH2Br
B . CH3CH2Br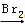 CH2BrCH2Br
C . CH3CH2Br
CH2BrCH2Br
C . CH3CH2Br CH2=CH2
CH2=CH2 CH2BrCH3
CH2BrCH3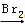 CH2BrCH2Br
D . CH2=CH2
CH2BrCH2Br
D . CH2=CH2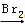 CH2BrCH2Br
CH2BrCH2Br
-
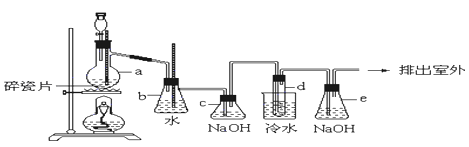
(1) 烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速升高到170℃,否则容易产生副反应.请你写出乙醇的这个消去反应方程式:
-
(2) 写出制备1,2﹣二溴乙烷的化学方程式:
-
(3) 安全瓶b可以以上倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象:
-
(4) 容器c中NaOH溶液的作用是:
-
(5) 某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因:
-
(6) e装置内NaOH溶液的作用是
已知1,2﹣二溴乙烷的主要物理性质如表:
熔点 | 沸点 | 密度 | 溶解性 |
9.79℃ | 131.4℃ | 2.18g/cm3 | 难溶于水,易溶于醇、醚等 |
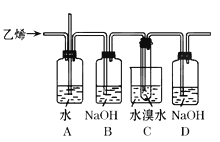
如图为实验室用乙烯与液溴作用制取1,2﹣二溴乙烷的部分装置图.
-
(1) A、C中都盛有水,这两个装置的作用分别是
-
(2) B和D装置都盛有NaOH溶液,它们的作用分别是
-
(3) 试写出以乙醇、浓硫酸、液溴为主要原料生成1,2﹣二溴乙烷的主要化学反应方程式
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是 .实际通常是用溴化钠与一定浓度的硫酸和乙醇反应.某课外小组欲在实验室制备溴乙烷的装置如图,实验操怍步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应.
请问答下列问题.
(2)装置A的作用是 .
(3)反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生,该气体的分子式是 .
(4)反应结束后,得到的粗产品呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的 (填写上正确选项的字母).a.稀氢氧化钠溶液 b.乙醇c.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称).
(5)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水CaCl2 , 然后进行的实验操作是 (填写正确选项的字母).a.分液 b.蒸馏 c.萃取
(6)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因是 .通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号).
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液.
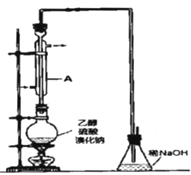
滴液漏斗已知:R﹣OH+HX→R﹣X+H2O
如图是实验室用乙醇与浓硫酸和溴化钠反应制备溴乙烷的装置,图中省去了加热装置.有关数据见表:
乙醇、溴乙烷、溴有关参数
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度/g•cm﹣3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
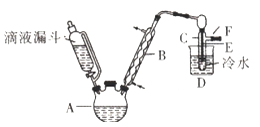
-
(1) 制备操作中,加入的浓硫酸必需进行稀释,其目的是
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂 -
(2) 加热的目的是 (从速率和限度两方面回答);应采取的加热方式是
-
(3) 为除去产品中的一种主要杂质,最好选择下列溶液来洗涤产品
A.氢氧化钠 B.碘化钠 C.亚硫酸钠
-
(4) 第(3)步的实验所需要的主要玻璃仪器是
完成下列填空:
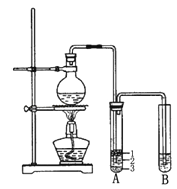
-
(1) 圆底烧瓶中加入的反应物是溴化钠、 和1:1的硫酸.
-
(2) 写出加热时烧瓶中发生的主要反应的化学方程式
-
(3) 将生成物导入盛有冰水混合物的试管A中,试管A中的物质分为三层(如图所示),产物在第 层.
-
(4) 用浓硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是 (选填编号).
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的有机物的名称是
已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
溶解性(本身均做溶剂) | 沸点(℃) | 密度(g/mL) | |
水混溶,易溶于有机溶剂 | 78.5 | 0.8 | |
难溶于水,易溶于有机溶剂 | 38.4 | 1.4 |
某研究性学习小组的同学将乙醇、80%的硫酸、NaBr固体按一定比例混合后(总体积约140mL)置于图1
的反应容器B中后进行加热(两个装置中的加热、固定装置及沸石均省略).
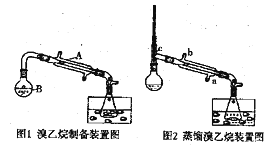
-
(1) ①仪器A的名称是: ;②容器B的容积是:
a.150mL b.200mL c.250mL
-
(2) 两个水槽中的液体均是冰水,使用冰水的目的是
-
(3) HBr与乙醇反应生成目标产物的化学方程式
-
(4) 图1中收集到的产品中含有一定量的杂质Br2 . 为除去该杂质,可先向混合液中加入适量的(从下面所给试剂中选取) ,然后再进行 操作即可.
a.四氯化碳 b.碳酸钠稀溶液 c.无水CaCl2 d.无水MgSO4
-
(5) 经过(4)处理后的目标产物中还含有少量的水等杂质,可通过向产品中加入一定量的 (从上面的a~d中选取),充分作用后,过滤,将滤液使用图2中的装置进行提纯,冷却水应从 口(填a或b)进入.
-
(6) 若实验中使用的无水乙醇的体积是46mL,蒸馏后得到的纯溴乙烷的体积是50rnL,则溴乙烷的产率为 %.
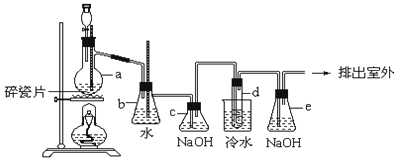
-
(1) 写出制备1,2﹣二溴乙烷的化学方程式:
-
(2) 请写出烧瓶a中发生反应的化学方程式:
-
(3) 安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象:
-
(4) 某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因.
-
(5) c装置内NaOH溶液的作用是 ;e装置内NaOH溶液的作用是

-
(1) 圆底烧瓶中加入的反应物是溴化钠、 和1:1的硫酸(浓硫酸与水的体积比为1:1),配制1:1硫酸时所用的定量仪器为 (选填编号)
a.天平 b.量筒c.容量瓶 d.碱式滴定管
-
(2) 加热时烧瓶中发生两个主要反应,请补充完整反应的化学方程式:
①NaBr+H2SO4
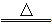 HBr↑+NaHSO4
HBr↑+NaHSO4②
-
(3) 将生成物导入盛有冰水混合物中,冰水对产物冷却并液封,试管A中的物质分为三层(如图 所示),产物在第 层
-
(4) 试管A中除了产物和水之外,还可能存在 (化学式,任意写出一种)
-
(5) 用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是 (填序号)
a.蒸馏b.用NaOH溶液洗涤 c.用CCl4萃取 d.用Na2SO3溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称是
-
(6) 实验员老师建议把上述装置中的仪器连接部分的橡胶管改成标准玻璃接口,橡胶塞最好用锡箔包住,其原因是
-
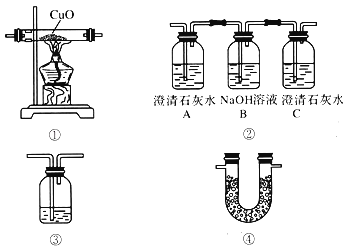
(1) 用图所示的装置确证乙醇燃烧产物中有CO、CO2、H2O,应将乙醇燃烧产物依次通过以下装置,按气流从左到右的顺序填写装置编号:
-
(2) 实验时可观察到装置②中A瓶的石灰水变浑浊.A瓶溶液的作用是 ,B瓶溶液的作用是 ;C瓶溶液的作用
-
(3) 装置①的作用是 .装置③中所盛的是 溶液,作用是
-
(4) 装置④中所盛固体药品是 ,它可确证的产物是
-
(5) 尾气应
-
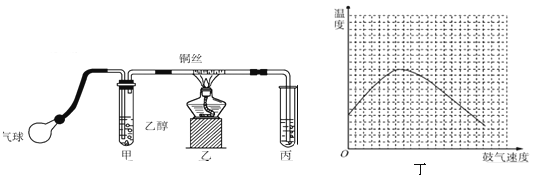
(1) 检验乙醛的试剂是 (填字母).
A.银氨溶液 B.碳酸氢钠溶液 C.新制Cu(OH)2 D.氧化铜
-
(2) 乙醇发生催化氧化反应的化学方程式为:
-
(3) 实验时,常常将甲装置浸在70~80℃的水浴中,目的是 ,由于装置设计上的缺陷,实验进行时可能会
-
(4) 反应发生后,移去酒精灯,利用反应自身放出的热量可维持反 应继续进行.进一步研究表明,鼓气速度与反应体系的温度关系曲线如图丁所示.试解释鼓气速度过快,反应体系温度反而下降的原因 ,该实验中“鼓气速度”这一变量你认为可用 来估量.
-
(5) 该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色.该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应.请你设计一个简单的实验,探究哪一种猜想正确?
NaBr+H2SO4=HBr+NaHSO4①
R—OH+HBr ![]() R—Br+H2O②
R—Br+H2O②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下:
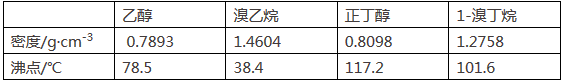
请回答下列问题:
-
(1) 溴乙烷和1溴丁烷的制备实验中,下列仪器最不可能用到的是(填字母)。
a.圆底烧瓶
b.量筒
c.锥形瓶
d.布氏漏斗
-
(2) 溴代烃的水溶性(填“大于”、“等于”或“小于”)相应的醇,其原因是。
-
(3) 将1溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在(填“上层”“下层”或“不分层”)。
-
(4) 制备操作中,加入的浓硫酸必须进行稀释,其目的是(填字母)。
a.减少副产物烯和醚的生成
b.减少Br2的生成
c.减少HBr的挥发
d.水是反应的催化剂
-
(5) 欲除去溴乙烷中的少量杂质Br2 , 下列物质中最适合的是(填字母)。
a.NaI
b.NaOH
c.NaHSO3
d.KCl
-
(6) 在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于;但在制备1溴丁烷时却不能边反应边蒸出产物,其原因是。
根据题意完成下列填空:
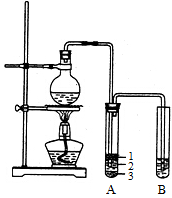
-
(1) 圆底烧瓶中加入的反应物是溴化钠、和1:1的硫酸。配制体积比1:1的硫酸所用的定量仪器为(选填编号)。
a.天平 b.量筒 c.容量瓶 d.滴定管
-
(2) 写出加热时烧瓶中发生的主要反应的化学方程式。
-
(3) 将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是。试管A中的物质分为三层(如图所示),产物在第层。
-
(4) 试管A中除了产物和水之外,还可能存在、(写出化学式)。
-
(5) 用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是(选填编号)。
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称是。
-
(6) 实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:。
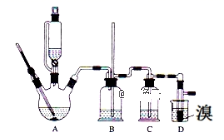
| 乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm﹣3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
-
(1) 用少量的溴和足量的乙醇、浓硫酸制备1,2﹣二溴乙烷的需分两步进行,第一步需要在冰水浴下混合浓硫酸和乙醇,混合时加入试剂的顺序是,使用冰水浴降温的目的是,第二步反应的化学方程式。
-
(2) 在此实验中,要在A中加入,防止,反应温度提高到170℃左右,其最主要目的是(填正确选项前的字母)。
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
-
(3) 装置B的作用是,在装置C中应加入,其目的是吸收反应中可能生成的酸性气体(填正确选项前的字母)。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
-
(4) 判断D中反应结束的方法是,将D中1,2﹣二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”、“下”)。
-
(5) 若产物中有少量副产物乙醚,可用的方法除去。
-
(6) 反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是。
NaBr+H2SO 4 =HBr+NaHSO4 ①
R—OH+HBr→ R—Br+H2O②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br- 被浓硫酸氧化为 Br2等。有关数据列表如下:
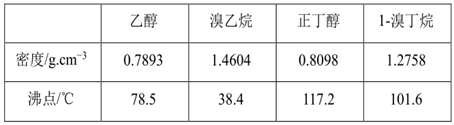
请回答下列问题:
-
(1) 在蒸馏过程中,仪器选择及安装都正确的是(填标号)。
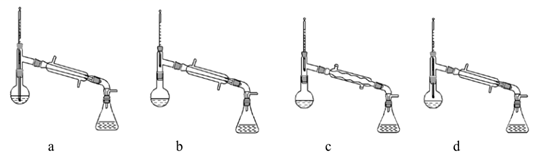
-
(2) 醇的水溶性(填“大于”、“等于”或“小于”)相应的溴代烃。
-
(3) 将 1溴丁烷粗产品置于分液漏斗中加水,振荡后静置,水在(填“上层”“下层”或“不分层”)。
-
(4) 制备操作中,加入的浓硫酸必须进行稀释,其目的是(填字母)。
a.水是反应的催化剂 b.减少 Br2 的生成
c.减少 HBr 的挥发 d.减少副产物烯和醚的生成
-
(5) 欲除去溴乙烷中的少量杂质 Br 2 ,下列物质中最适合的是(填字母)。
a.NaI b.KCl c.NaOH d.NaHSO 3
-
(6) 在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于;但在制备 1溴丁烷时却不能边反应边蒸出产物,其原因是。
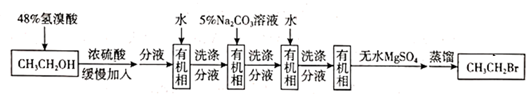
下列说法错误的是( )
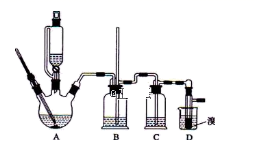
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
-
(1) 写出由乙醇制备乙烯的化学方程式,乙烯制备1,2-二溴乙烷的化学方程式。
-
(2) 在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是;(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
-
(3) 在装置A中除了浓硫酸和乙醇外,还应加入,其目的是装置A中生成副产物乙醚的化学反应方程式 。
-
(4) 实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放 ,
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液 d.品红和酸性KMnO4
-
(5) 将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”、“下”);若产物中有少量副产物乙醚。可用的方法除去。
|
乙醇 |
溴乙烷 |
液溴 |
|
|
相对分子质量 |
46 |
109 |
160 |
|
状态 |
无色液体 |
无色液体 |
深红色液体 |
|
密度/(g·cm3) |
0.79 |
1.44 |
3.1 |
|
沸点/℃ |
78.5 |
38.4 |
59 |
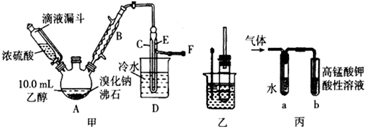
-
(1) I. 溴乙烷的制备
反应原理如下,实验装置如上图(加热装置、夹持装置均省略):
H2SO4+NaBr
 NaHSO4+HBr↑ CH3CH2OH+HBr
NaHSO4+HBr↑ CH3CH2OH+HBr  CH3CH2Br+H2O
CH3CH2Br+H2O图甲中A 仪器的名称,图中B 冷凝管的作用为。
-
(2) 若图甲中A 加热温度过高或浓硫酸的浓度过大,均会使 C 中收集到的粗产品呈橙色,原因是A 中发生了副反应生成了;F 连接导管通入稀NaOH 溶液中,其目的主要是吸收等尾气防止污染空气
-
(3) II. 溴乙烷性质的探究
用如图实验装置验证溴乙烷的性质:
在乙中试管内加入 10mL6mol·L -1NaOH 溶液和 2mL 溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为。
-
(4) 若将乙中试管里的 NaOH 溶液换成NaOH 乙醇溶液,为证明产物为乙烯,将生成的气体通入如图丙装置。a 试管中的水的作用是;若无 a 试管,将生成的气体直接通入 b 试管中,则 b中的试剂可以为 。
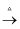 CH3CH2CH2CH2Br+NaHSO4+H2O,反应后混合物经水洗、干燥、蒸馏等操作可得到精制产品.部分操作装置如图所示:
CH3CH2CH2CH2Br+NaHSO4+H2O,反应后混合物经水洗、干燥、蒸馏等操作可得到精制产品.部分操作装置如图所示: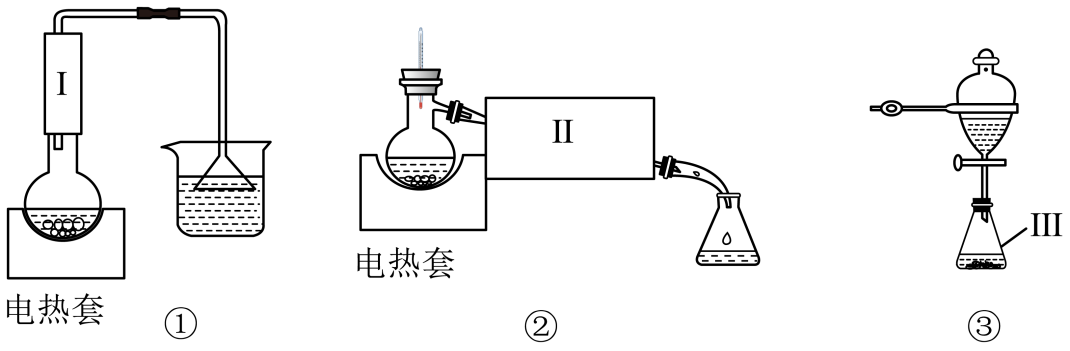
下列说法中正确的是( )
- 右图为植物细胞亚显微结构模式图,请据图回答:(1)该细胞中8和9所示结构依次代表______、_____。 (2)在细胞
- 南京夫子庙地区有两千的历史,屡建屡毁,屡毁屡建,至1983的重建夫子庙地区,融建筑文化、饮食文化、戏剧文化、商业文化于一
- 斜面倾角为θ,长为L,在其顶点水平抛出一个小球,如图5-3-4所示,小球刚好落在斜面的底端,那么小球的初速度v0多大?
- 化学就在我们身边,它与我们的生活息息相关。请从以下物质:A.天然气;B.干冰;C.碳酸氢钠;D.氧气中选择适当的字母序号
- 下列各组物质中,依次属于单质、酸、盐的一组是( )A.氢气、硝酸、碳酸钠 B.氧气、盐酸、氧化钙C.冰
- Wow! Theseflowers very nice. Do you likethem?
- 已知是α锐角,且sin (α-10°)= ,则α= 。
- “一五”计划中大规模的工业化建设,初步奠定了社会主义工业化和现代化的基础,构筑了牢不可破、巍然屹立的新生共和国的“钢筋铁
- 阅读下文,完成文后各题。 朋 党 论欧阳修 ①臣闻朋党之说,自古有之,惟幸人君辨其君子小人而已。大凡君子与君子,以同道为
- “千淘万漉虽辛苦,吹尽黄沙始见金”给我们的哲学启示是 ①应坚持一分为二的观点 ②要重视量的积累 ③办事情要成功必须充分发
- 大革命失败后,中国对民主革命道路进行了新的探索,这条新道路指的是( ) A.领导工人阶级进行武装斗争
- 已知为等差数列,其前n项和为Sn,若a3=6,S3=12,则公差d等于( ) A.1 B
- 下列叙述,不正确的是 ()。 A.人类定居初期,受生产力水平的限制,村落通常出现在靠近河流水源的地方 B.平原地区土壤肥
- Brazil has________ land and water resources,and these days i
- 属于纯净物的是( ) A.澄清的石灰水 B.矿泉水 C.洁净的空气 D.氢气
- ________ several times, Bill made up his mind not to watch
- 牙膏中配有氟化物添加剂能防止龋齿,原因是,长期使用加氟牙膏在牙齿表面生成了一层质地硬、溶解度小的氟磷酸钙。已知氟磷酸钙化
- 解决我国水资源空间分布不均的主要措施是( ) A、兴建水库 B、跨流域调水 C、建防洪大
- 下列实验现象和对应的结论描述都正确的是() A.向某固体上滴加稀盐酸,有气泡产生一一该固体一定是碳酸盐 B.向某无色溶液
- —Did you see a man in black pass by just now? —No,sir.I ___



