物质的量与其浓度和气体摩尔体积的综合应用 知识点题库
设NA为阿伏加德罗常数值.下列说法正确的是( )
A . 常温常压下,4.4g乙醛所含σ键数目为0.7NA
B . 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA
C . 12g石墨烯(单层石墨)中含有六元环的个数为0.5NA
D . 50ml浓度为18.4mol•L﹣1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
对一定量气体体积的探究.
已知1 mol不同气体在不同条件下的体积.
化学式 | 条件 | 1mol气体体积 |
H2 | 0℃,101kPa | 22.4 |
O2 | 0℃,101kPa | 22.4 |
CO | 0℃,101kPa | 22.4 |
H2 | 0℃,202kPa | 11.2 |
CO2 | 0℃,202kPa | 11.2 |
N2 | 273℃,202kPa | 22.4 |
NH3 | 273℃,202kPa | 22.4 |
-
(1) 从上表分析得出的结论:①1 mol任何气体在标准状况下的体积都约为.
②1 mol不同的气体,在不同的条件下,体积(填“一定”、“一定不”或“不一定”)相等.
-
(2) 理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是:①,②.
-
(3) 应用:在标准状况下,48g O3的体积为多少升?(写出计算过程)
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A . 1molOH﹣所含质子数为10NA
B . 常温常压下,28克CO和N2的混合气体所含原子数为2NA
C . 4g氢气中含有的原子数为2NA
D . 标准状况下,11.2L酒精含有的分子数为0.5NA
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A . 1mol由Na2O和Na2O2组成的混合物中,含有的离子数为3NA
B . 1L1mol·L-1饱和氯化铁溶液滴入沸水中完全反应生成氢氧化铁胶粒数为NA
C . 1L 12mol•L-1浓盐酸和足量MnO2在加热条件下充分反应,生成的气体的分子数为3NA
D . 等物质的量的H2O和CO2所含原子数均为3NA
-
(1) 1.5NA个H3PO4的摩尔质量为,含氧原子的物质的量为。
-
(2) a mol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为。
-
(3) 25.2g Na2RO3含Na+0.4mol,则Na2RO3的摩尔质量为,R的相对原子质量为。含R的质量为1.6g的Na2RO3 , 其物质的量为。
-
(4) 相同条件下,比较下列物质中氢原子数目多少(填“>”“<”或“=”):
①4.9g H2SO43.6g H2O ②1.6L CH42.4L H2
电解原理和原电池原理是电化学的两个重要内容,引起了人们的研究兴趣。
-
(1) 现有以下三种乙醇燃料电池
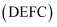 。
。 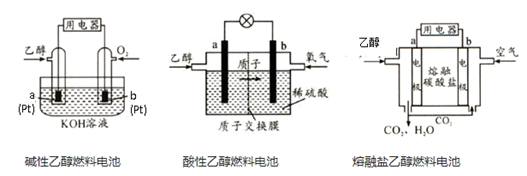
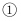 碱性乙醇燃料电池中,电极a上发生的电极反应式为。
碱性乙醇燃料电池中,电极a上发生的电极反应式为。 熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电极b上发生的电极反应式为。
熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电极b上发生的电极反应式为。 -
(2) 0.4molCuSO4和
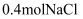 溶于水,配成1L溶液,用惰性电极进行电解,当一个电极得到
溶于水,配成1L溶液,用惰性电极进行电解,当一个电极得到 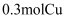 时,另一个电极上生成的气体在标准状况下的体积为L。
时,另一个电极上生成的气体在标准状况下的体积为L。
-
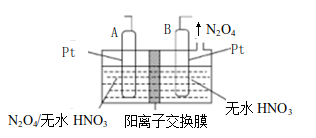
(3) 新型绿色硝化剂
 可以
可以  为原料用电解法制备,实验装置如图所示,则电极B接直流电源的极,电解池中生成
为原料用电解法制备,实验装置如图所示,则电极B接直流电源的极,电解池中生成  的电极反应式为
的电极反应式为 
-
(4) 依据电化学知识,解决下列问题:
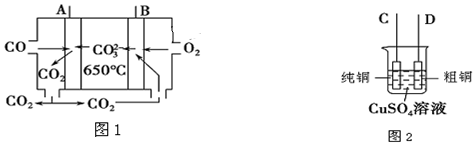
图1是一种新型燃料电池,以CO为燃料,一定比例的
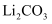 和
和  的熔融混合物为电解质,图2是粗铜精炼的装置图,现用该燃料电池为电源进行粗铜的精炼实验。
的熔融混合物为电解质,图2是粗铜精炼的装置图,现用该燃料电池为电源进行粗铜的精炼实验。要用燃料电池为电源进行粗铜的精炼实验,则 B极应该与极
 填“C”或“D”
填“C”或“D”  相连。当消耗标准状况下
相连。当消耗标准状况下 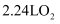 时,C电极的质量变化为。
时,C电极的质量变化为。
设NA代表阿伏加德罗常数的数值,则下列说法正确的是( )
A . 1.8gD2O含有NA个中子
B . 用5mL 3mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015NA
C . 在Na2O2与CO2的反应中,每转移NA个电子时,消耗22.4L的CO2
D . 25℃时,7gC2H4和C3H6的混合气体中,含有NA个C-H键
-
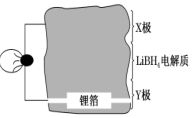
(1) 全固态锂离子电池的结构如图所示,放电时电池反应为 2Li+MgH2=Mg+2LiH。放电时,X 极作极。充电时,Y 极反应式为。
-
(2) 电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子)。
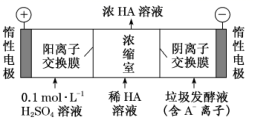
①阳极的电极反应式为
②简述浓缩室中得到浓乳酸的原理:
③电解过程中,采取一定的措施可控制阳极室的 pH 约为 6~8,此时进入浓缩室的OH-可忽略不计。400 mL 10 g∙L −1 乳酸溶液通电一段时间后,浓度上升为 145 g∙L −1 (溶液体积变化忽略不计),阴极上产生的 H2 在标准状况下的体积约为L。(乳酸的摩尔质量为90 g•mol-1)
在标准状况下,10gCO和CO2的混合气体的体积为6.72L,则此混合气体中CO和CO2的物质的量之比是( )
A . 2:1
B . 1:2
C . 1:1
D . 3:4
NA表示阿伏加德罗常数,下列叙述正确的是( )
A . 标准状况下,1mol H2O的体积约为22.4L
B . 0.1mol NH4+中含有NA个质子
C . 同温同压下两种气体的摩尔质量之比等于密度之比
D . 物质的量浓度为0.5 mol•L﹣1的MgCl2溶液中,含有Cl﹣个数为NA
下列叙述中正确的是( )
A . 22.4LN2中一定含有2molN
B . 58.5gNaCl固体中有1mol的NaCl分子
C . S2和S8的混合物共6.4g,所含硫原子数一定为0.2mol
D . 标准状况下,11.2LCl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 标况下,22.4L CHCl3中含有的氯原子数目为3NA
B . 向恒容密闭容器中充入2moI NO和1molO2 , 充分反应后容器中分子总数一定为2NA
C . 1L硫酸铝溶液中,SO  的浓度为1.5a mol·L-1 , 则Al3+数目为a·NA
D . 用惰性电极电解100mL0.1mol·L-1的CuSO4溶液,当阴、阳两极产生相同条件下等体积的气体时,电路中转移电子数为0.04NA
的浓度为1.5a mol·L-1 , 则Al3+数目为a·NA
D . 用惰性电极电解100mL0.1mol·L-1的CuSO4溶液,当阴、阳两极产生相同条件下等体积的气体时,电路中转移电子数为0.04NA
 的浓度为1.5a mol·L-1 , 则Al3+数目为a·NA
D . 用惰性电极电解100mL0.1mol·L-1的CuSO4溶液,当阴、阳两极产生相同条件下等体积的气体时,电路中转移电子数为0.04NA
的浓度为1.5a mol·L-1 , 则Al3+数目为a·NA
D . 用惰性电极电解100mL0.1mol·L-1的CuSO4溶液,当阴、阳两极产生相同条件下等体积的气体时,电路中转移电子数为0.04NA
设  为阿伏加德罗常数的值。下列说法错误的是( )
为阿伏加德罗常数的值。下列说法错误的是( )
 为阿伏加德罗常数的值。下列说法错误的是( )
为阿伏加德罗常数的值。下列说法错误的是( )
A . 常温下,8g  中含有的原子总数为
中含有的原子总数为  B . 标准状况下,2.24L由
B . 标准状况下,2.24L由  和
和  组成的混合气体中含有的分子数为
组成的混合气体中含有的分子数为  C . 1 mol
C . 1 mol  被还原为
被还原为 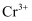 时转移的电子数为
时转移的电子数为  D .
D . 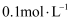 的
的  溶液中含有的阳离子数为
溶液中含有的阳离子数为 
 中含有的原子总数为
中含有的原子总数为  B . 标准状况下,2.24L由
B . 标准状况下,2.24L由  和
和  组成的混合气体中含有的分子数为
组成的混合气体中含有的分子数为  C . 1 mol
C . 1 mol  被还原为
被还原为 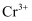 时转移的电子数为
时转移的电子数为  D .
D . 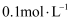 的
的  溶液中含有的阳离子数为
溶液中含有的阳离子数为 
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 11.2 LCl2通入足量的NaOH 溶液中充分反应 ,转移的电子数为 0.5NA
B . 4.4 g 由 CO2 和 N2O 组成的混合气体中含有的电子总数为 2.2NA
C . 常温下 ,1.0L p H=1 的 H2SO4溶液中含有H+的数目为 0.2NA
D . 11.5 g乙醇分子中含有C- H键的数目为1.5NA
NA是阿伏加德罗常数的值。下列说法正确的是( )
A . 10g质量分数为34%的H2O2溶液含有的氢原子数为0.2NA
B . 0.1mol Na2O2和Na2O的混合物中含有的离子总数等于0.4NA
C . 标准状态下,11.2LSO2含有的氧原子数为NA
D . 100 mL 0.1 mol/L醋酸中含有的醋酸分子数是0.01NA
工业除去电石渣浆[含 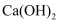 ]上层清液中的
]上层清液中的  (
(  浓度为
浓度为 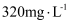 ),并抽取石膏(
),并抽取石膏(  )的常用流程如图,其中
)的常用流程如图,其中  常用空气代替。下列说法错误的是( )
常用空气代替。下列说法错误的是( )
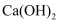 ]上层清液中的
]上层清液中的  (
(  浓度为
浓度为 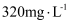 ),并抽取石膏(
),并抽取石膏(  )的常用流程如图,其中
)的常用流程如图,其中  常用空气代替。下列说法错误的是( )
常用空气代替。下列说法错误的是( ) 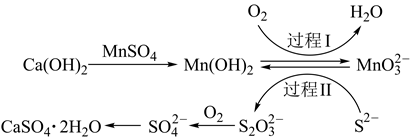
A . 在普通硅酸盐水泥中,常添加石膏用来调节水泥的硬化速度
B . 过程Ⅰ中,氧化剂与氧化产物的物质的量之比为2∶1
C . 将10L上层清液中的  转化为
转化为  ,理论上共需标准状况下空气约22.4L
D . 过程Ⅱ中,反应的离子方程式
,理论上共需标准状况下空气约22.4L
D . 过程Ⅱ中,反应的离子方程式 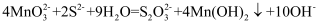
 转化为
转化为  ,理论上共需标准状况下空气约22.4L
D . 过程Ⅱ中,反应的离子方程式
,理论上共需标准状况下空气约22.4L
D . 过程Ⅱ中,反应的离子方程式 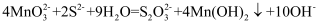
设  表示阿伏加德罗常数的值,下列叙述错误的是( )
表示阿伏加德罗常数的值,下列叙述错误的是( )
 表示阿伏加德罗常数的值,下列叙述错误的是( )
表示阿伏加德罗常数的值,下列叙述错误的是( )
A . 常温常压下, 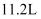 氮气所含的原子数目为
氮气所含的原子数目为  B . 常温常压下,
B . 常温常压下, 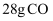 中所含原子数为2
中所含原子数为2  C .
C . 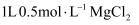 溶液中,含有
溶液中,含有  的个数为
的个数为  D .
D . 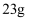 钠与氧气充分反应,转移电子数为
钠与氧气充分反应,转移电子数为 
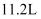 氮气所含的原子数目为
氮气所含的原子数目为  B . 常温常压下,
B . 常温常压下, 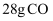 中所含原子数为2
中所含原子数为2  C .
C . 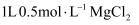 溶液中,含有
溶液中,含有  的个数为
的个数为  D .
D . 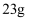 钠与氧气充分反应,转移电子数为
钠与氧气充分反应,转移电子数为 
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A . 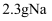 与氧气充分反应生成
与氧气充分反应生成 和
和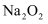 , 转移电子数为0.1NA
B . 标准状况下,
, 转移电子数为0.1NA
B . 标准状况下,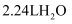 中含有的共价键数为0.2NA
C .
中含有的共价键数为0.2NA
C . 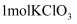 溶液中,含有
溶液中,含有 的个数为NA
D . 常温常压下,
的个数为NA
D . 常温常压下,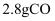 和
和 混合气体中含原子数小于0.2NA
混合气体中含原子数小于0.2NA
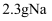 与氧气充分反应生成
与氧气充分反应生成 和
和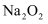 , 转移电子数为0.1NA
B . 标准状况下,
, 转移电子数为0.1NA
B . 标准状况下,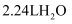 中含有的共价键数为0.2NA
C .
中含有的共价键数为0.2NA
C . 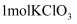 溶液中,含有
溶液中,含有 的个数为NA
D . 常温常压下,
的个数为NA
D . 常温常压下,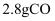 和
和 混合气体中含原子数小于0.2NA
混合气体中含原子数小于0.2NA
用 表示阿伏加德罗常数的值,下列叙述错误的是( )
表示阿伏加德罗常数的值,下列叙述错误的是( )
 表示阿伏加德罗常数的值,下列叙述错误的是( )
表示阿伏加德罗常数的值,下列叙述错误的是( )
A . 在标准状况下,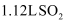 中所含原子总数为
中所含原子总数为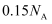 B .
B .  中含有非极性共价键的数目为
中含有非极性共价键的数目为 C .
C . 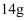 聚乙烯中含有碳碳双键的数目为
聚乙烯中含有碳碳双键的数目为 D .
D . 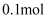 苯中含有碳碳双键的数目为
苯中含有碳碳双键的数目为
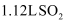 中所含原子总数为
中所含原子总数为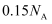 B .
B .  中含有非极性共价键的数目为
中含有非极性共价键的数目为 C .
C . 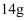 聚乙烯中含有碳碳双键的数目为
聚乙烯中含有碳碳双键的数目为 D .
D .  苯中含有碳碳双键的数目为
苯中含有碳碳双键的数目为
如图,同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2 , 进行喷泉实验。经充分反应后,瓶内溶质的物质的量浓度为(不考虑瓶内溶液向烧杯中扩散)( )
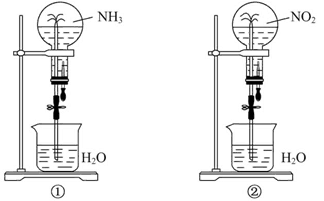
A . ①>②
B . ①<②
C . ①=②
D . 不能确定
最近更新
- 下面一段文字中有四处用词不当,请找出来并加以修改。 现在,越来越多的家长感触听不懂自己孩子常用的词语,交
- 法国作家巴尔扎克的《人间喜剧》堪称资本主义的“社会百科全书”,主要是因为它( )A、展现了19世纪上半期法国社会生活
- 如图表示胰岛素分子(分泌蛋白)中一条多肽链,其中有3个甘氨酸(R基:﹣H)且分别位于第8、20、23位.下列叙述正确的是
- 北京时间3月4日8时18分,在中国台湾高雄县、屏东县交界(北纬22.9度,东经120.6度)发生6.7级地震。另据台湾媒
- 两根足够长的金属导轨竖直放置,间距为L,底端接阻值为R的电阻。将质量为m的金属棒悬挂在一个固定的轻弹簧下端,金属棒和导轨
- 的算术平方根是( ) A. B. C. D.
- 在我国,公民和国家之间是和谐统一的关系,公民享有广泛的政治权利和自由。据此回答1-2题。 1.在我国,人民成为国家和社会
- 袋中有大小相同的5只钢球,分别标有1、2、3、4、5五个号码.任意抽取2个球,设2个球号码之和为ξ,则ξ所有可能值的个数
- 某反应使用催化剂后,其反应过程中能量变化如图所示。下列说法错误的是( ) A. 该反应的总反应为放热反应 B. 使
- 2011年4月14日,“金砖国家”巴西、俄罗斯、印度、中国和南非领导人第三次正式会晤在三亚举行。“金砖国家”的崛起,提升
- 分裂期细胞的细胞质中含有一种促进染色质凝集为染色体的物质。将某种动物的分裂中期细胞与G1期(DNA复制前期)细胞融合后,
- 用单色光做杨氏双缝干涉实验时,在屏上呈现清晰的明暗相间的条纹,若将光屏稍微前移或后移一点,则A.光屏上都将出现模糊的条纹
- 已知平面上点P∈{(x,y)|(x-2cosα)2+(y-2sinα)2=16(α∈R)},则满足条件的点P在平面上所组
- 电感线圈中的电流在0.6 s时间内改变了1 A,在这段时间内线圈中产生的感应电动势为0.2 mV,求由这个线圈和1.4×
- (08年苏州)现用质量分数为98%的浓硫酸(密度是1.84g·cm-3)配制560g质量分数为14%的稀硫酸时,下列有关
- 下列关于内环境及其稳态的说法不正确的是 A.内环境的存在一定程度上说明了生命诞生的历史,内环境稳态是生物进化的结果 B.
- ---How was your job interview yesterday? --- Oh, I couldn’
- 在右图所示的电路中观察三只小灯泡亮度变化和两只电压表的变化情况,如果滑线变阻器的触片P由a端滑至b端,电压表V1示数变化
- 求数列,,,,…的通项公式,并求其前n项和.
- 《长江商报》9月2日披露,湖北京山县大竹水电站“竣工即废”,引起省、市、县有关部门高度重视,目前已经组织调查组进行调查。



