氧化还原反应的电子转移数目计算 知识点题库
亚氯酸钠( 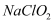 )是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产
)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产 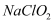 的主要流程如下:
的主要流程如下:
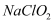 )是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产
)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产 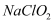 的主要流程如下:
的主要流程如下: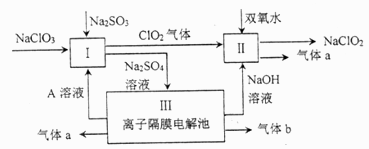
-
(1) I中发生反应的还原剂是(填化学式)。
-
(2) II中反应的离子方程式是。
-
(3) III中离子隔膜电解池的装置如下:
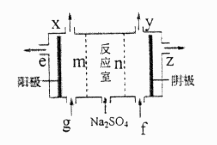
①A的化学式是,A在口产生。
②m为(填“阴”、“阳”)离子交换膜。
③结合化学用语和文字说明解释
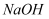 产生的原因:。
产生的原因:。 -
(4)
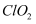 是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备: 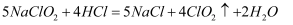
①该反应中氧化剂和还原剂的物质的量之比是。
②研究表明:若反应开始时盐酸浓度越大,则气体产物中
 的含量越大,运用氧化还原反应规律分析其原因是。
的含量越大,运用氧化还原反应规律分析其原因是。 -
(5)
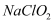 变质可分解为
变质可分解为 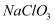 和
和 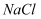 。取等质量变质前后的
。取等质量变质前后的 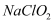 试样均配成溶液,分别与足量
试样均配成溶液,分别与足量 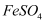 溶液反应时,消耗
溶液反应时,消耗 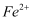 的物质的量前者(填>、<、=)后者。
的物质的量前者(填>、<、=)后者。
将磁性氧化铁放入稀HNO3中发生反应:3Fe3O4+ 28HNO3=9Fe(NO3)x+NO↑+14H2O。下列判断合理的是()
A . Fe(NO3)x中的x为2
B . 反应中每生成0.2 mol 还原产物,就有0.6 mol 电子转移
C . 稀HNO3 在反应中只作氧化剂
D . 磁性氧化铁中的铁元素全部被氧化
高温下焙烧CuFeS2的反应之一为2CuFeS2+7O2=CuSO4+CuO+Fe2O3+3SO2 , 下列关于该反应的叙述正确的是( )
A . CuFeS2中硫的化合价为-1
B . CuFeS2发生还原反应
C . 1molCuFeS2完全反应转移13mol电子
D . CuSO4和SO2既是氧化产物,又是还原产物
-
(1) 147gH2SO4的物质的量是;
-
(2) 氧化铜在高温下发生分解反应:4CuO
 2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为mol。
2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为mol。
-
(3) 反应:2FeCl3+2KI=2FeCl2+2KCl+I2 , 其中元素化合价升高,则该元素被,元素化合价降低;作还原剂,发生还原反应。
-
(4) 钠在空气中燃烧的化学方程式:,1mol钠完全燃烧转移电子的个数为(阿伏加德罗常数为NA)。
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A . 1mol白磷(P4)分子中所含化学键的数目为4 NA
B . 标准状况下,11.2 L SO3中含有分子0.5 NA
C . 16.9 g过氧化钡(BaO2) 固体中阴、阳离子总数为0.2 NA
D . 某密闭容器盛有0.1mol N2和0.3mol H2, 在一定条件下充分反应,转移电子的数目为0.6 NA
已知反应:3Cu+8HNO3(稀) = 3Cu(NO3)2 + 2NO↑+ 4H2O。下列说法错误的是( )
A . Cu被氧化,NO是还原产物
B . 氧化剂和还原剂的物质的量比为8:3
C . HNO3体现氧化性和酸性
D . 若反应掉32gCu,转移电子数为6.02×1023
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A . 2.8g14N2与14C16O的混合物中,中子数目为 l.4NA
B . 含 0. 1 molFeCl3的溶液与0.1 mol 锌充分反应,转移电子数为0.1 NA
C . 标准状况下,5.6gC4H8中 C-C 的数目可能为0.4NA
D . 某温度下,1LpH=9 的 Na2CO3 溶液中,水电离产生的OH-数目为10-5 NA
已知:将 Cl2通入适量 NaOH 溶液,产物中可能有 NaCl、NaClO、NaClO3 , 且 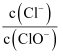 的值仅与温度高低有关。当n(NaOH)=6a mol 时,下列有关说法错误的是( )
的值仅与温度高低有关。当n(NaOH)=6a mol 时,下列有关说法错误的是( )
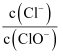 的值仅与温度高低有关。当n(NaOH)=6a mol 时,下列有关说法错误的是( )
的值仅与温度高低有关。当n(NaOH)=6a mol 时,下列有关说法错误的是( )
A . 参加反应的氯气的物质的量 3amol
B . 改变温度,产物中NaCl 的最小理论产量为 3a mol
C . 改变温度,反应中转移电子的物质的量 n 的范围:3a mol≤n≤5a mol
D . 某温度下,反应后 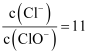 ,则溶液中
,则溶液中 
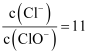 ,则溶液中
,则溶液中 
已知:2H2O(l)=2H2(g)+O2(g)ΔH=+571.0kJ/mol。以太阳能为热源分解Fe3O4 , 经热化学铁氧化合物循环分解水制H2的过程如图:
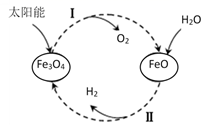
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g)ΔH=+313.2kJ/mol
过程Ⅱ:……
下列说法错误的是( )
A . 过程Ⅰ中每消耗232gFe3O4转移2mol电子
B . 过程Ⅱ热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s)ΔH=-128.9kJ/mol
C . 过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能
D . 铁氧化合物循环制H2具有成本低、产物易分离等优点
凭借清洁、储量大、能量转换率高、运行稳定等优势,氢能被现代工业视为最理想、潜力最大的新能源。2020 年上海进博会展览中,诸多氢能源汽车纷纷亮相。氢燃料电池被誉为氢能源汽车的心脏。某种氢燃料电池的内部结构如图,下列说法正确的是( )
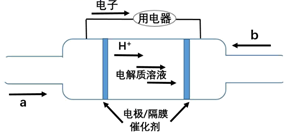

A . 电池每消耗 11.2L氢气,电路中通过的电子数目为NA
B . a 处通入的是氧气
C . 右侧电极发生的反应为:O2+4e-+4H+=2H2O
D . 右侧电极为电池的负极
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂,易溶于水且不与水反应。实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,试回答下列问题。
-
(1) 该反应中氧化剂的化学式是。
-
(2) 用双线桥标出上述反应的电子转移情况。
-
(3) 标准状况下44.8 mL的ClO2恰好能与50 mL 0.1 mol·L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4 , 氯元素在产物中的化合价为,此过程说明ClO2具有(填“氧化”或“还原”)性。
-
(4) ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的倍。
-
(5) 新制备的ClO2中常含有少量Cl2 , 检验其中是否含有Cl2的实验方法是。
HCOOH燃料电池的工作原理如图所示。下列说法正确的是( )
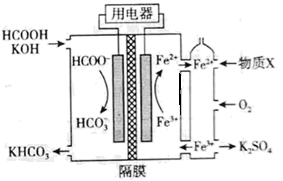
A . 放电时K+通过隔膜向左迁移
B . 正极电极反应式为 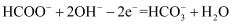 C . 放电过程中需补充的物质X为
C . 放电过程中需补充的物质X为  D . 每转移
D . 每转移 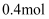 电子,理论上消耗标准状况下
电子,理论上消耗标准状况下 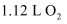
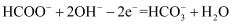 C . 放电过程中需补充的物质X为
C . 放电过程中需补充的物质X为  D . 每转移
D . 每转移 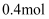 电子,理论上消耗标准状况下
电子,理论上消耗标准状况下 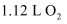
设 NA 为阿伏加德罗常数的值,下列说法正确的是( )
A . 0.1molCH4 与 P4 的混合物中所含共价键数目为 0.4NA
B . 25℃时,pH=1 的 CH3COOH 溶液中所含 H+数目为 0.1NA
C . 0.1molN2 与 0.3molH2 反应生成的 NH3 的分子数为 0.2NA
D . 实验室制 H2 时,生成 0.1molH2 转移电子数为 0.2NA
BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚(化学式为CHQO),原理如图所示。
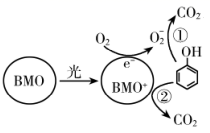
下列说法错误的是( )
A . 反应②中 BMO+转化为 BMO
B . 该过程说明氧化性:BMO+比 O2 弱
C . 若有 1molO2 参与反应,则总反应中有 6mol 电子转移
D . 反应①和②中被降解的苯酚的物质的量之比为 3∶1
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 1molO2与足量钾反应生成KO2时,转移的电子数为4NA
B . 1L0.1mol·L-1NH4HSO4溶液中阴离子的数目大于0.1NA
C . 标准状况下,22.4L癸烷中含非极性键的数目为9NA
D . 78g由Na2S和Na2O2组成的混合物中含阴离子的总数为1.5NA
可闻声波诱导液体振动产生的法拉第波可以调节氧气分子在水中的溶解,从而诱导有差别的时空分布,有的区城呈氧化性,而同时有的区域呈还原性。研究人员选择了如图所示的氧化还原平衡体系。已知:声波频率提高可促进氧气的溶解。
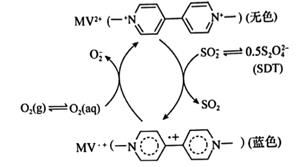
下列说法错误的是( )
A . MV2+被  还原形成自由基阳离子MV·+的过程伴随着颜色的改变
B . 开启可闻声波能够促进MV2+再生
C . 持续补充SDT才能维持蓝色
D . 向体系中加入1 mol SDT,转移电子为2 mol
还原形成自由基阳离子MV·+的过程伴随着颜色的改变
B . 开启可闻声波能够促进MV2+再生
C . 持续补充SDT才能维持蓝色
D . 向体系中加入1 mol SDT,转移电子为2 mol
 还原形成自由基阳离子MV·+的过程伴随着颜色的改变
B . 开启可闻声波能够促进MV2+再生
C . 持续补充SDT才能维持蓝色
D . 向体系中加入1 mol SDT,转移电子为2 mol
还原形成自由基阳离子MV·+的过程伴随着颜色的改变
B . 开启可闻声波能够促进MV2+再生
C . 持续补充SDT才能维持蓝色
D . 向体系中加入1 mol SDT,转移电子为2 mol
NaH是一种良好的生氢剂,与水反应的化学方程式为NaH+H2O=NaOH+H2↑,下列有关该反应的说法错误的是( )
A . NaH中H的化合价为-1价
B . H2既是氧化产物,又是还原产物
C . 氧化剂和还原剂的物质的量之比为1∶1
D . 电子转移的方向和数目可以表示为: 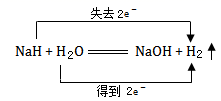

对于反应MnO2+4HCl(浓)  MnCl2+2H2O+Cl2↑,下列说法正确的是( )
MnCl2+2H2O+Cl2↑,下列说法正确的是( )
 MnCl2+2H2O+Cl2↑,下列说法正确的是( )
MnCl2+2H2O+Cl2↑,下列说法正确的是( )
A . MnO2发生氧化反应,HCl发生还原反应
B . 每反应4个HCl分子,转移2个电子
C . 每生成1个Cl2分子,转移4个电子
D . 反应中锰元素将电子转移给氯元素
阅读下面一段材料并回答问题。

-
(1) K2FeO4中铁元素的化合价为。
-
(2) 制备 K2FeO4需要在(填“酸性”、“碱性”或“中性”)环境中进行。
-
(3) 下列关于K2FeO4的说法中,错误的是。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
-
(4) 将K2FeO4与水反应的化学方程式补充完整:4K2FeO4+_H2O=_Fe(OH)3(胶体)+ _+ _KOH,。
-
(5) 消毒净化500 m3水,至少需要K2FeO4的质量为kg。
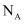 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
A . 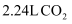 中含有的原子数一定为
中含有的原子数一定为
 B .
B . 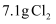 被足量
被足量
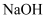 稀溶液吸收,转移电子数为
稀溶液吸收,转移电子数为
 C . 标况下,
C . 标况下,
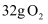 和
和
 混合气体的体积约为
混合气体的体积约为
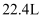 D .
D . 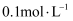 的
的
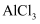 溶液中含有的
溶液中含有的
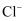 数为
数为

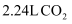 中含有的原子数一定为
中含有的原子数一定为
 B .
B . 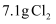 被足量
被足量
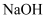 稀溶液吸收,转移电子数为
稀溶液吸收,转移电子数为
 C . 标况下,
C . 标况下,
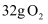 和
和
 混合气体的体积约为
混合气体的体积约为
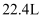 D .
D . 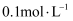 的
的
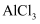 溶液中含有的
溶液中含有的
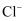 数为
数为

最近更新
- 中国古代讲究“同姓不婚”。已知春秋时秦晋两国世为婚姻(故称两姓联姻为“喜结秦晋之好”),而鲁晋两国不可通婚。结合所学关于
- (本小题满分10分)选修4-4:坐标系与参数方程 已知直线C1:(t为参数),C2:(为参数), (Ⅰ)当=
- (2013江苏徐州摸底)如图所示,水平桌面上一小钢球沿直线运动.若在钢球运动的正前方A处或旁边B处放一块磁铁,下列关于小
- 用下列实验装置进行的实验,能达到相应实验目的的是( )A.装置甲:防止铁钉生锈
- 为防止硝酸厂产生的氮氧化物污染环境,通常用NaOH溶液吸收这些氮氧化物,反应的化学方程式为:NO+NOx+2NaOH=2
- 某恒星附近有一颗卫星,它绕该恒星做匀速圆周运动的周期是T,设万有引力常量为G,则该恒星的平均密度为_______.
- 如下图所示是某质点v-t图象,0—2 s内加速度是________,2—4 s内加速度是________,4—5 s内加
- 把形状、大小、质地完全相同的4张卡片分别标上数字﹣1、﹣4、0、2,将这4张卡片放入不透明的盒子中搅匀.求下列事件的概率
- 下列混合物的分离和提纯方法中,主要是从溶解性的角度考虑的是 A.蒸发 B.蒸馏 C.过滤
- 已知函数f(x)是定义在R上的奇函数,其最小正周期为3,且x∈(-,0)时,f(x)=log2(-3x+1),则f(20
- 下列关于生物膜的叙述,不正确的是 ( ) A.细胞完成分
- 读“地球赤道面与公转轨道面示意图”,完成下列各题。25.图中代表黄赤交角的是( ) A.① B.
- — Whyhaven’t you asked her to come here? — She _______ an i
- 设等差数列前项和为,若,,则公差为 ( ) A. B. C.
- 显微镜对光完成后,从目镜中看到的视野应该是 ( )A.黑暗的B.刺眼的C.灰暗的D.白亮的
- 如图,已知A、B两点的坐标分别为(2,0)、(0,4),P是△AOB外接圆⊙C上的 一点,且∠AOP=45°,则点P的坐
- 右图是一个陆地生态系统食物网的结构模式图,下列叙述中不正确的是 A.在该食物网中,共有5条食物链
- 若a=-2×3 b=(-2×3) c=-(2×3)而下列大小关系正确的是( ) A、a>b>c
- 在世界上最早种植粟的原始人类是 A元谋人 B.北京人
- 下列各组词语中,有错别字的一项是 ( ) A.装潢



