酯化反应 知识点题库
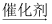 CH3CH2Cl 加聚反应
B . CH3COOH+CH3CH2OH
CH3CH2Cl 加聚反应
B . CH3COOH+CH3CH2OH 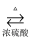 CH3COOCH2CH3+H2O 酯化反应
C .
CH3COOCH2CH3+H2O 酯化反应
C . -
(1) 乙烯通入溴水中:
-
(2) 2﹣氯丙烷与氢氧化钠水溶液共热:
-
(3) 乙醇和乙酸在浓硫酸作用下反应:
-
(4) 苯酚与甲醛在加入浓盐酸作用下发生缩聚反应:.
乙烯 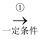 甲
甲  乙
乙  PVC
PVC
-
(1) 乙是PVC的单体,其结构简式为;
-
(2) 反应③的化学方程式为;
-
(3) 写出以下反应类型:
反应①;
反应②。
-
(4) 邻苯二甲酸辛酯(DOP)是国家标准中允许使用的增塑剂之一,邻苯二甲酸
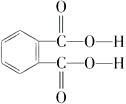 是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,其结构简式为。
是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,其结构简式为。
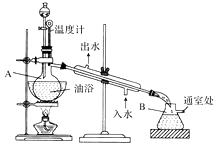
试回答:
-
(1) 实验中的硫酸的主要作用是。
-
(2) 用过量乙醇的主要目的是_,
边加料,边加热蒸馏的目的是。
-
(3) 用饱和Na2CO3溶液洗涤粗酯的目的是,
如果用NaOH浓溶液代替Na2CO3 , 将引起的后果是。
-
(4) 用饱和CaCl2溶液洗涤粗酯的目的是_。
-
(5) 加入无水硫酸钠,其目的是。
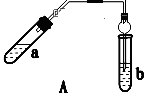
请回答下列问题:
-
(1) 步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:。
-
(2) A装置中使用球形管除起到冷凝作用外,另一重要作用是,步骤⑤中分离乙酸乙酯必须使用的一种仪器是。
-
(3) 为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图A所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管b再测有机层的厚度,实验记录如下:
实验
编号
试管a中试剂
试管b中试剂
测得有机层的厚度/cm
A
3 mL乙醇、2 mL乙酸、1mL 18mol·L-1浓硫酸
饱和Na2CO3溶液
5.0
B
3 mL乙醇、2 mL乙酸
0.1
C
3 mL乙醇、2 mL乙酸、6 mL 3mol·L-1H2SO4
1.2
D
3 mL乙醇、2 mL乙酸、盐酸
1.2
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是mL和mol·L-1。
②分析实验(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是。
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是。
④分离出乙酸乙酯层后,经过洗涤,为了干燥乙酸乙酯可选用的干燥剂为 (填字母)。
A.P2O5
B.无水Na2SO4
C.碱石灰
D.NaOH固体
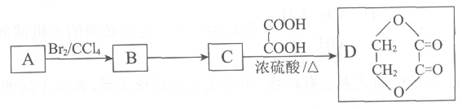
-
(1) A→B的反应类型是。
-
(2) B→C反应的试剂及条件是。
-
(3) C→D反应的化学方程式是。
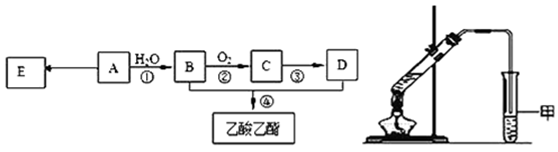
-
(1) 0.1mol该烃A能与g溴发生加成反应;加成产物需mol溴蒸气完全取代;
-
(2) B中官能团的名称是,B通过两次氧化可得到D,也可通过加入的氧化试剂为(任填一种)直接氧化为D。
-
(3) E是常见的高分子材料,写出E的结构简式;合成E的反应类型;
-
(4) 某同学用如图所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
①实验开始时,试管甲中的导管不伸入液面下的原因是;
②上述实验中饱和碳酸钠溶液的作用是。
③乙醇与乙酸反应的化学方程式是:,浓硫酸的作用是。
 )
)
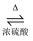 CH3COOC2H5+H218O
B . 镁离子的结构示意图:
CH3COOC2H5+H218O
B . 镁离子的结构示意图:  Na++Cl−
Na++Cl−
|
实验 |
装置 |
试剂a |
现象 |
|
① |
|
Ca(OH)2溶液(含酚酞) |
溶液褪色,产生白色沉淀 |
|
② |
少量NaHCO3溶液 |
产生气泡 |
|
|
③ |
酸性KMnO4溶液 |
紫色溶液褪色 |
|
|
④ |
C2H5OH和浓硫酸 |
加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式错误的是( )
 +5
+5  +16H+=2Mn2++10CO2↑+ 8H2O
D . H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH
+16H+=2Mn2++10CO2↑+ 8H2O
D . H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH 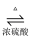 C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
-
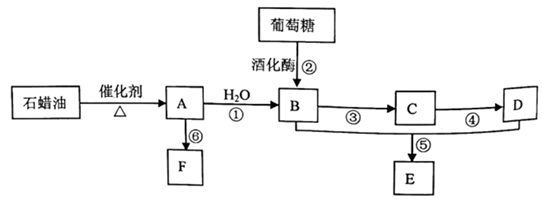
(1) ①的反应类型为;③的反应条件是;F的结构简式为。
-
(2) B和D中官能团的名称分别是和。
-
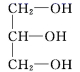
(3) 仿照反应⑤,写出CH3COOH与HOCH2CH2OH按物质的量之比为2:1反应的化学方程式。
-
(4) 写出含有-COOH的E的所有同分异构体的结构简式。
-
(5) 下列有关A~F的说法正确的是。
a.A中所有原子共平面
b.B中有3种氢原子
c.B,C,D均能与钠反应放出氢气
d.E难溶于水且密度比水大;
e.F在自然界中易降解
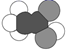 能发生酯化反应
B . 用燃烧法鉴别毛织品和棉织品
C . 用淀粉溶液无法直接鉴别加碘食盐和不含碘的食盐
D . 能用加酶洗衣粉洗涤蚕丝织品
能发生酯化反应
B . 用燃烧法鉴别毛织品和棉织品
C . 用淀粉溶液无法直接鉴别加碘食盐和不含碘的食盐
D . 能用加酶洗衣粉洗涤蚕丝织品
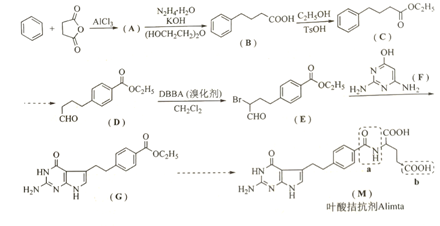
叶酸拮抗剂 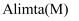 是一种多靶向性抗癌药物。以苯和丁二酸酐为原料合成该化合物的路线如下:
是一种多靶向性抗癌药物。以苯和丁二酸酐为原料合成该化合物的路线如下:
回答下列问题:
已知:① 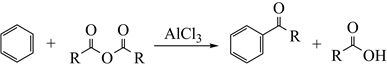
② 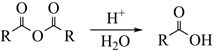
-
(1) A的结构简式为;
-
(2)
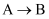 ,
, 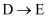 的反应类型分别是,;
的反应类型分别是,;
-
(3) M中虚线框内官能团的名称为a,b;
-
(4) B有多种同分异构体,同时满足下列条件的同分异构体有种(不考虑立体异构)
①苯环上有2个取代基②能够发生银镜反应③与
 溶液发生显色发应
溶液发生显色发应其中核磁共振氢谱有五组峰,且峰面积之比为6:2:2:1:1的结构简式为;
-
(5) 结合上述信息,写出丁二酸酐和乙二醇合成聚丁二酸乙二醇酯的反应方程式;
-
(6) 参照上述合成路线,以乙烯和
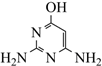 为原料,设计合成
为原料,设计合成 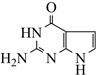 的路线(其他试剂任选)。
的路线(其他试剂任选)。
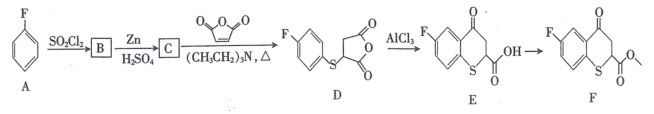
已知:-SO2Cl  -SH。
-SH。
回答下列问题:
-
(1) A的名称为;E中含氧官能团的名称为。
-
(2) B的结构简式为;C→D的反应类型为。
-
(3) 一定条件下,D与水反应生成二元羧酸的化学方程式为。
-
(4) 反应E→F所需的试剂及反应条件分别是,F中有个手性碳(注:连有4个不同的原子或基团的碳为手性碳)。
-
(5) 某温度下,对A→B反应的产物成分进行研究发现,其-SO2Cl基化的不同位置的产物成分的含量如下表所示:
与F的相对位置
邻
间
对
其他
含量/%
38.8
3.66
57.25
0.29
请找出规律:
-
(6) G为E与1 mol H2完全反应后的产物,G的同分异构体中能同时满足以下条件的有种(不考虑立体异构)。
I.苯环上只有三个取代基且处于邻位,且-SH、-F直接与苯环相连;
II.能发生银镜反应;
III.能与NaHCO3溶液反应。
 能够发生如图所示的一系列转化。并且经核磁共振氢谱仪测定,发现化合物
能够发生如图所示的一系列转化。并且经核磁共振氢谱仪测定,发现化合物 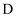 的分子中含两种氢原子。
的分子中含两种氢原子。
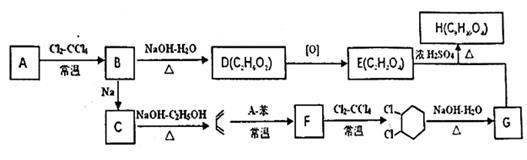
已知:① 
② 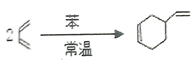 (
( ![]() 不能发生反应)
不能发生反应)
试回答下列问题:
-
(1) H的结构简式为,D、E中所含的官能团名称分别为。
-
(2) 图中的转化过程里;属于加成反应的有个。
-
(3) 下列关于有机物
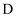 的说法中,正确的是。
的说法中,正确的是。
A .难溶于水 B .能够使酸性
 溶液褪色 C .能发生取代、氧化、缩聚等反应 D. 能与
溶液褪色 C .能发生取代、氧化、缩聚等反应 D. 能与 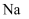 和
和  反应,且消耗二者物质的量之比为 1:1
反应,且消耗二者物质的量之比为 1:1 -
(4) 在
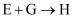 的反应里,浓硫酸的作用是。
的反应里,浓硫酸的作用是。
-
(5)
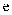 和
和 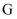 作用,也能够得到高分子化合物,请写出该化学方程式。
作用,也能够得到高分子化合物,请写出该化学方程式。
-
(6) 已知
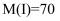 ,则I作为A的同系物的所有同分异构体有种,其中核磁共振氢谱有4组吸收峰的分子有种,用系统命名法为其命名。
,则I作为A的同系物的所有同分异构体有种,其中核磁共振氢谱有4组吸收峰的分子有种,用系统命名法为其命名。
-
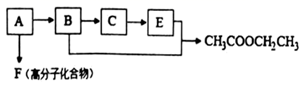
(1) A物质的结构简式是。
-
(2) B是A与H2O在加热加压、催化剂的条件下生成的。下列物质中与B互为同分异构体的是(填字母)。
a.CH3OH b.CH3OCH3 c.CH3CHO
-
(3) C物质能直接转化为B,该反应的化学反应方程式为。
-
(4) 物质A可在一定条件下直接转化为高分子化合物F,F的结构简式是,由A生成F的反应类型是反应。
-
(5) B和E在一定条件下反应生成CH3COOCH2CH3的化学方程式是。
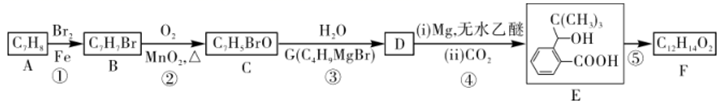
已知:①RX+Mg  RMgX(X=Cl、Br、I)
RMgX(X=Cl、Br、I)
②RMgBr+CO2→RCOOH
③RMgBr+R'CHO 
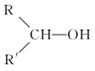
回答下列问题:
-
(1) B的化学名称为(用系统命名法表示),E中官能团的名称为。
-
(2) 用*标出E中的手性碳原子,G的结构简式为。
-
(3) 步骤②反应的化学方程式为,E→F的反应类型为。
-
(4) F有多种同分异构体,写出一种满足下列条件的同分异构体的结构简式:。
①除苯环外无其他环
②能发生银镜反应
③核磁共振氢谱为4组峰,峰面积比为9∶2∶2∶1
-
(5) 参照上述合成路线,以乙烯和甲苯为原料,设计制备
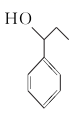 的合成路线: (其他试剂任选)。
的合成路线: (其他试剂任选)。
- 已知数列满足,若,则_____.
- 生活处处有化学.下列变化属于化学变化的是() A.葡萄酿成酒 B.水果榨成果汁 C.蔗糖溶于水
- In 2015, a bill allowing every couple to have two children w
- 规范的操作是实验成功的前提,实验操作正确的是()A. 蒸发操作时,蒸发皿必须放在石棉网上,用酒精灯外焰加热 B. 取少量
- 如图是三个对数函数的图象,则a、b、c的大小关系是() A.a>b>c B.c>b>a C.c>a>b
- 下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是() A.氢氧化钠与盐酸;氢氧化钠与碳酸 B.BaCl2溶液
- 关于分子的热运动,下列说法正确的是( )A.分子的热运动就是布朗运动B.布朗运动是液体分子的无规则运动C.温度越高
- 阅读下面一首唐诗,然后回答问题。 江汉 杜甫 江汉思归客,乾坤一腐儒。 片云天共远,水夜月同孤。 落日心犹壮,秋风病欲苏
- (10分)如图所示,三棱镜的顶角是30º,出射光线与入射光线夹角也为30º。问:(1)该三棱镜的折射率是多大?(2)光在
- 现代科学研究表明,多种微生物参与了腐乳的发酵,其中起主要作用的是() A.青霉
- 机动灵活,周转速度快,装卸方便,对各种自然条件适应性强的运输方式是 ( ) A.航空 B.公路 C.铁路
- 人的糖蛋白必须经内质网和高尔基体进一步加工合成,通过转基因技术,可以使人的糖蛋白基因得以表达的受体细胞是 A、大肠杆菌
- 在氮源为14N和15N的培养基上生长的大肠杆菌,其DNA分子分别为14N-DNA(相对分子质量为a)和15N-DNA(相
- 为了迎接将于2014年10月在荆州古城举行的湖北省第十四届运动会,荆州市的园林工人们在新建的荆州市体育运动中心的广场上移
- 从编号为1~50的50枚最新研制的某种型号的导弹中随机抽取5枚来进行发射实验,若采用每部分选取的号码间隔一样的系统抽样方
- 身高1.7 m的人在平面镜前1.5 m处,平面镜高1 m,则人在平面镜中的像高 m。人和像的距离是 m。当
- 通常用来衡量一个国家的石油化学工业发展水平的标志是 ( ) A.石油的年产
- 用均匀导线做成的正方形线圈边长为l,正方形的一半放在垂直于纸面向里的匀强磁场中,如图所示,当磁场以的变化率增强时,则A.
- 现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了鉴别四种溶液各是什么,将它们随意编号为A、B、C、D后,按下
- 下列各组植物中,生活环境中和繁殖方式最相似的是 A.墙藓、肾蕨 B.水绵、水稻 C.海带、雪松 D




