含有氢键的物质 知识点题库
(1)下列物质中,哪些形成分子内氢键,哪些形成分子间氢键?(填序号)
①HF ②H2O ③NH3④CH4⑤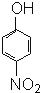 ⑥
⑥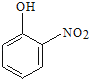 ⑦甲酸
⑦甲酸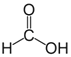 形成分子内氢键的有 ;形成分子间氢键有
形成分子内氢键的有 ;形成分子间氢键有
(2)二聚甲酸解聚反应为:(HCOOH)2→2 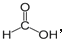 , 该反应需吸收60KJ•mol﹣1的能量,此能量是断开 键所需的能量,所以此键的键能为 kJ•mol﹣1
, 该反应需吸收60KJ•mol﹣1的能量,此能量是断开 键所需的能量,所以此键的键能为 kJ•mol﹣1
(3)根据氢键形成的条件,推测二聚甲酸的结构式为:
下列各组物质,化学键类型相同、晶体类型相同且熔化时破坏作用力类型也相同的( )
A . HCl KCl
B . CO2 SiO2
C . NH4Cl CCl4
D . NaOH Na2O2
根据已学知识,请你回答下列问题:
-
(1) 写出原子序数最小的第Ⅷ族元素原子的原子结构示意图.
-
(2) 写出3p轨道上有2个未成对电子的元素的符号:.
-
(3) 该元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4 , 该元素的名称是.
-
(4) 已知下列化学键的键能:Si﹣O:460kJ/mol,Si﹣Si:175kJ/mol,O=O:498kJ/mol,则反应:Si+O2=SiO2的反应热△H=.
-
(5) 写出二氧化硫和水合氢离子中S原子,O原子分别采用和杂化形式,其空间构型分别为和.
-
(6) 用氢键表示法表示HF水溶液中的所有氢键、、、.
下列物质中分子间能形成氢键的是( )
A . N2
B . HBr
C . H2S
D . NH3
中科院国家纳米科学中心2013年11月22日宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据.这不仅将人类对微观世界的认识向前推进了一大步,也为在分子、原子尺度上的研究提供了更精确的方法.下列说法中正确的是( )
①正是氢键的存在,冰能浮在水面上
②氢键是自然界中最重要、存在最广泛的化学键之一
③由于氢键的存在,沸点:HCl>HBr>HI>HF
④由于氢键的存在,使水与乙醇互溶
⑤由于氢键的存在,使水具有稳定的化学性质.
A . ②⑤
B . ③⑤
C . ②④
D . ①④
下列现象与氢键有关的是( )
①NH3的熔、沸点比VA族其他元素氢化物的高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④尿素的熔、沸点比醋酸的高
⑤液态氟化氢的化学式有时可以写成(HF)n 的形式
⑥H2O比H2S稳定.
A . ①②③④⑤⑥
B . ①②③④⑤
C . ①②③④
D . ①②③
下列物质中分子间能形成氢键的是( )
A . HBr
B . H2S
C . NH3
D . PH3
关于氢键的下列说法正确的是( )
A . 由于氢键的作用,使NH3、H2O、HF的沸点反常,且沸点高低顺序为HF>H2O>NH3
B . 氢键只能存在于分子间,不能存在于分子内
C . 没有氢键,就没有生命
D . 相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多
第二周期除Be、B、N、Ne四种元素外,其他元素的氢化物的沸点为:a.1 317 ℃ b.100 ℃ c.19.5 ℃ d.-162 ℃。则c的化学式为( )
A . LiH
B . CH4
C . H2O
D . HF
通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
A . 分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B . NCl3分子是非极性分子
C . NBr3比NCl3易挥发
D . 在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式为 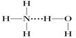
-
(1) 比较NaHCO3与NaAlO2结合氢离子能力的强弱,用一个离子方程式加以说明:。
-
(2) 画出NH3·H2O的结构。 (氢键可用X…H-Y来表示)
-
(3) 常压下,AlF3的熔点(1040℃)比AlCl3的熔点(194℃)高,原因是。
原子序数依次增大的A、B、C、D、E、F、G七种元素。其中A的原子有5种不同运动状态的电子;B的基态原子有3个不同的能级,各能级中的电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;E为它所在周期中原子半径最大的主族元素;F和D位于同一主族,G的原子序数为29。
-
(1) 基态G原子的价电子排布式为。
-
(2) 元素B、C的简单气态氢化物的沸点较高的是 (用化学式表示)。
-
(3) A晶体熔点为2300℃,则其为晶体。
-
(4) GD在加热条件下容易转化为G2D,从原子结构的角度解释原因。
-
(5) G与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸盐,为将生成的两种气体(气体相对分子质量均小于50)完全转化为最高价含氧酸盐,消耗了1molO2和1L2.2mol/LNaOH溶液。则两种气体的分子式及物质的量分别为,生成硫酸铜物质的量为。
已知短周期主族元素X、Y、Z、W和Q的原子序数依次增大,X与Q同主族,其中四种元素可形成化合物M,M的结构简式如图,下列说法错误的是( )
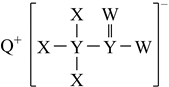
A . X、Z和W可以形成离子化合物
B . 简单离子半径:W<Q
C . W和Q形成的化合物可能含非极性共价键
D . 简单氢化物的沸点:W>Z>Y
下列说法正确的是( )
A . 氢键是一种化学键
B . 氢键使物质具有较高的熔、沸点
C . 能与水分子形成氢键的物质在水中的溶解度增大
D . 水结成冰体积膨胀与氢键无关
硅及其化合物在生产生活中有广泛应用。根据所学知识,回答下列问题:
-
(1) 三甲基卤硅烷【(CH3)3SiX,X为Cl、Br、I】是重要的化工原料。
①氯元素基态原子的价电子排布式为;按照核外电子排布对元素周期表分区,溴元素位于区;基态硅原子中有种运动状态不同的电子。
②Br、I的第一电离能的大小关系:I1(Br)I1(I)(填“大于”“小于”或“等于”)。
③常温下,(CH3)3SiI中Si—I键比(CH3)3SiCl中Si—Cl键易断裂的原因是。
-
(2) (CH3)3SiCl可作为下列有机合成反应的催化剂。
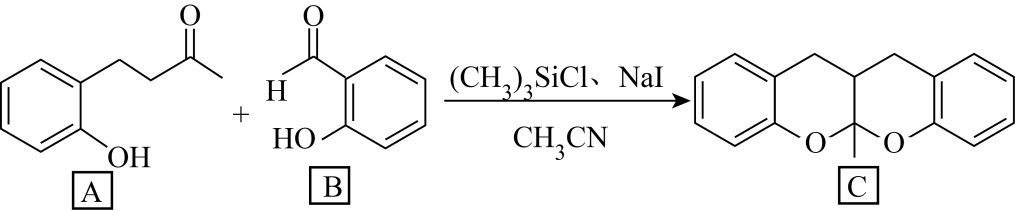
①1个有机物A分子中采取sp2杂化的碳原子有个。
②有机物B的沸点低于对羟基苯甲醛(
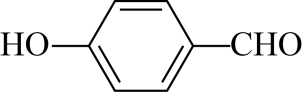 )的沸点,其原因是。
)的沸点,其原因是。③CH3CN中σ键与π键的个数比为。
-
(3) 一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(a、b方向的夹角为120°,c方向垂直于a、b方向,棱长a+b≠c),如图甲所示;晶胞中碳原子的投影位置如图乙所示。
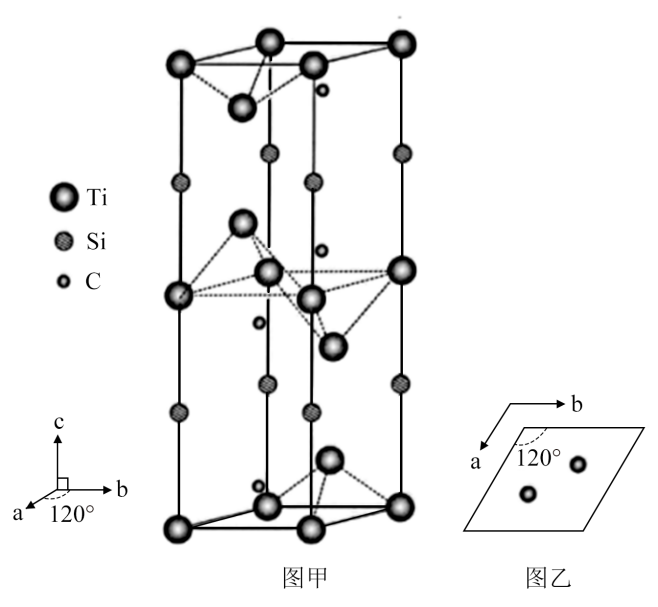
①该钛硅碳新型材料的化学式为。
②已知该新型材料的密度为4.51g•cm-3 , 且a、b的长度均为307pm,阿伏加德罗常数的值用NA表示,则c的长度为pm (列出计算式)。
化合物Z是一种具有广谱抗菌活性的药物,其合成反应如图。下列说法错误的是( )
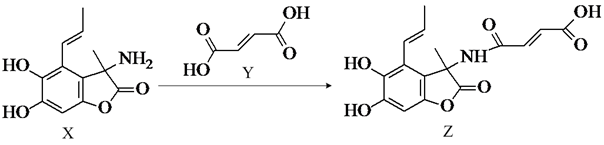
A . X分子间只能形成下列氢键:O-H…O、N-H…N
B . 1molZ最多能与6molNaOH反应
C . Z分子中含2个手性碳原子
D . X、Y、Z三种分子均存在顺反异构体
下 列有关反应N2(g)+ 3H2(g)  2NH3(g)ΔH= -92.4 kJ·mol-1的说法正确的是( )
2NH3(g)ΔH= -92.4 kJ·mol-1的说法正确的是( )
 2NH3(g)ΔH= -92.4 kJ·mol-1的说法正确的是( )
2NH3(g)ΔH= -92.4 kJ·mol-1的说法正确的是( )
A . NH3分子间能形氢键
B . 反应中N2体现了还原性
C . 提高 的值可增大N2的转化率
D . 可以使用酶作该反应的催化剂
的值可增大N2的转化率
D . 可以使用酶作该反应的催化剂
 的值可增大N2的转化率
D . 可以使用酶作该反应的催化剂
的值可增大N2的转化率
D . 可以使用酶作该反应的催化剂
下列“类比”结果正确的是( )
A . 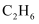 是非极性分子,则
是非极性分子,则 也是非极性分子
B .
也是非极性分子
B .  的分子构型为V形,则二甲醚的分子骨架(
的分子构型为V形,则二甲醚的分子骨架(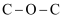 )构型也为V形
C . HF易形成
)构型也为V形
C . HF易形成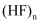 , 则HCl也易形成
, 则HCl也易形成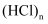 D .
D .  充分水解后再加热分解得到
充分水解后再加热分解得到 , 则也可用类似的方法从
, 则也可用类似的方法从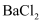 得到
得到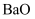
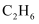 是非极性分子,则
是非极性分子,则 也是非极性分子
B .
也是非极性分子
B .  的分子构型为V形,则二甲醚的分子骨架(
的分子构型为V形,则二甲醚的分子骨架(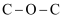 )构型也为V形
C . HF易形成
)构型也为V形
C . HF易形成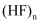 , 则HCl也易形成
, 则HCl也易形成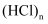 D .
D .  充分水解后再加热分解得到
充分水解后再加热分解得到 , 则也可用类似的方法从
, 则也可用类似的方法从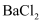 得到
得到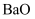
下列事实与氢键无关的是( )
A .  的沸点比
的沸点比 的沸点高
B . NaCl的熔点比CsCl的熔点高
C .
的沸点高
B . NaCl的熔点比CsCl的熔点高
C .  比
比 更易溶于水
D . 邻羟基苯甲醛(
更易溶于水
D . 邻羟基苯甲醛(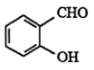 )的沸点比对羟基苯甲醛(
)的沸点比对羟基苯甲醛(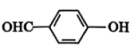 )的低
)的低
 的沸点比
的沸点比 的沸点高
B . NaCl的熔点比CsCl的熔点高
C .
的沸点高
B . NaCl的熔点比CsCl的熔点高
C .  比
比 更易溶于水
D . 邻羟基苯甲醛(
更易溶于水
D . 邻羟基苯甲醛( )的沸点比对羟基苯甲醛(
)的沸点比对羟基苯甲醛( )的低
)的低
随着温度的升高,水从固态融化成液态,再蒸发成气态,最终分解成氢气和氧气,如图所示,这个过程中主要克服的作用力依次是( )

A . 分子间作用力 分子间作用力、氢键 极性共价键
B . 氢键 氢键、分子间作用力 极性共价键
C . 分子间作用力 分子间作用力、氢键 非极性共价键
D . 氢键 氢键、分子间作用力 非极性共价键
最近更新
- 名篇名句默写 (1)《归园田居》(其一)用鸟和鱼来表达自己对园田和自由的向往。这两句诗是
- 下列各选项的分类中,后者包括前者的是() A.化合物,电解质 B.分子,原子
- 已知点A(x1,y1),B(x2,y2)(x1x2≠0)是抛物线y2=2px(p>0)上的两个动点,O是坐标原点,向量,
- 一太阳能电池板,测得它的开路电压为800mV,短路电流为40mA,若将该电池板与一阻值为60Ω的电阻器连成一闭合电路,则
- 在2009年两会召开之际,《国家中长期教育改革和发展规划纲要》面向全社会公开征求意见,希望通过集思广益,改善我国教育现状
- 下列关于运动物体所受合外力做功和动能变化的关系正确的是( )A.如果物体所受合外力为零,则合外力对物体做的功一定为
- 下图为“我国北方及周边地区2012年11月某日某时天气形势示意图”。读图完成问题。2.图中甲、乙天气系统的名称分别是 A
- Radium salts, which have been found to _____ in bones, give
- 滑雪运动员由斜坡高速向下滑行时其速度时间图象如图乙所示,则由图象中AB段曲线可知,运动员在此过程中:A.机械能守恒B.做
- 除去下列物质中少量杂质,所选试剂错误的是( ) 试剂 物质 杂质 试剂 A 炭粉 铁粉 稀盐酸 B 一氧化碳 二氧化碳
- 下列物质溶于水,能发生化学反应的是A.NaCl和KNO3 B.NaOH和BaCl2 C.CaCl2和Fe
- 京九铁路自北向南,跨越多条大江大河,穿过崇山峻岭,沿途地形各异,地质情况复杂, 在这种条件下修建铁路,其支撑条件是(
- 形如 的式子, 定义它的运算规则为 =;若 =0,则 .
- 科学家最新研制了一款微型无人侦察机——“蜂鸟”。为了减轻其质量,该侦察机的材料应具有的特点是 ( )A.硬度
- 所有绝对值小于4的整数的积是____________,和是 .
- 关于胶体的叙述不正确的是 A.淀粉溶液虽为“溶液”,但具有胶体的性质 B.胶体与其他分散系的本质区别是只有胶体有“丁达尔
- 通过比较极性键与非极性键,完成下列表格: 非极性键极性键定义 原子吸引电子能力 共用电子对 成键原子电性 判断依
- 冰壶运动是冬奥会的一个项目。冰壶由花岗岩凿磨而成,质量约为19kg。体积约为8×10-3m3,与冰道接触的底面积约为0.
- 随着生产力和科学技术的进步,对工厂区位影响逐渐减弱的区位因素是 A.市场 B.原料地 C.信息通讯网络
- 阅读下面的材料,根据要求写一篇不少于800字的文章。(60分) 513网上论坛。主题:明星代言。 甲:有明星代言



