晶格能的应用 知识点题库
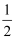 Cl2(g)―→NaCl(s) ΔH1
C . Na(s)―→Na(g) ΔH2
D . Na(g)-e-―→Na+(g) ΔH3
Cl2(g)―→NaCl(s) ΔH1
C . Na(s)―→Na(g) ΔH2
D . Na(g)-e-―→Na+(g) ΔH3
化学键 | Si﹣O | Si﹣Cl | H﹣H | H﹣Cl | Si﹣Si | Si﹣C |
键能/kJ•mol﹣1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
-
(1) 比较下列两组物质的熔点高低(填“>”或“<”)SiC Si;SiCl4 SiO2
-
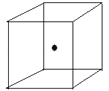
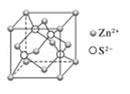
(2) 如图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子.
-
(3) 工业上用高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
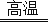 Si(s)+4HCl(g)该反应的反应热△H= kJ/mol.
Si(s)+4HCl(g)该反应的反应热△H= kJ/mol.
物质 | NaF | MgF2 | AlF3 | MgO | CaO | SrO | BaO |
| 923 | 2 957 | 5 492 | 3 791 | 3 401 | E | 1 918 |
由此表中数据不能得出的结论是( )
-
(1) 下列说法中正确的是_________。A . 半径:O2->Na+> Mg2+ B . 含氧酸的酸性:Cl>S>P C . 简单氢化物的稳定性:N>O>F D . 熔点:金刚石>碳化硅>硅单质
-
(2) C、N、O的电负性由大到小的顺序为。Na、Mg、Al的第一电离能由大到小的顺序为。
-
(3) 乙酸分子中σ键与π键的数目比为。HCOOCH3是乙酸的一种同分异构体,但沸点却比乙酸低得多,原因是。
-
(4) 已知AlCl3在178℃升华,熔融时生成二聚体Al2Cl6(结构式如下)。
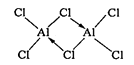
电解法制铝的原料是熔融的Al2O3而不是AlCl3 , 原因是;电解法制镁的原料是熔融的MgCl2而不用MgO,原因是。
 Cl2(g)=NaCl(s); △H2
C . Na+(l)+Cl-(l)=NaCl(s); △H3
D . Na(g)+
Cl2(g)=NaCl(s); △H2
C . Na+(l)+Cl-(l)=NaCl(s); △H3
D . Na(g)+  Cl2(g)=NaCl(s); △H4
Cl2(g)=NaCl(s); △H4
①具有规则几何外形的固体一定是晶体
②NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
③非极性分子中一定含有非极性键
④晶格能由大到小: NaF> NaCl> NaBr>NaI
⑤含有共价键的晶体一定具有高的熔、沸点及硬度
⑥s-s σ键与s-p σ键的电子云形状相同
⑦含有π键的化合物与只含σ键的化合物的化学性质不同
⑧中心原子采取sp3杂化的分子,其立体构形不一定是正四面体
-
(1) 元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。A . 404.4 B . 553.5 C . 589.2 D . 670.8 E . 766.5
-
(2) 基态K原子中,核外电子占据的最高能层的符号是,占据该能层电子的电子云轮廓图形状为。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是。
-
(3) X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为,中心原子的杂化形式为。
-
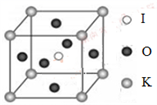
(4) KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为nm,与K紧邻的O个数为。
-
(5) 在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于位置,O处于位置。
 .
.
-
(1) Fe3+价层电子的轨道表达式(电子排布图)为。
-
(2) 硅能形成多种化合物(如SiH4、Si2H4等),SiH4的中心原子的杂化轨道类型为,其分子的立体构型为,键角为;Si2H4分子中含有的σ键和π键的数目之比为。
-
(3) Mg、Al的第一电离能:MgAl(填“>”或“<”)。
-
(4) Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是。
-
(5) Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为;设Ag原子半径为rcm,阿伏加德罗常数的值用NA表示,则Ag晶体的密度为 g·cm-3(写出表达式)。

-
(1) 金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为 ;基态 Mn原子核外有种运动状态不同的电子,M层的电子云有种不同的伸展方向。
-
(2) 第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是
-
(3) NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒(写出一种),K3[Co(NO2)6]中存在的作用力有a.σ键 b.π键 c.配位键 d.离子键 e.范德华力
-
(4) 锰的一种配合物的化学式为 Mn(BH4)2(THF)3 , BH4-的空间构型为
-
(5) FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。

可知,O原子的第一电子亲和能为 kJ•mol-1 , FeO晶格能为kJ•mol-1。
-
(6) 铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为,已知该晶体的密度为ρg•cm-3 , NA是阿伏加德罗常数的值,则晶胞参数为pm
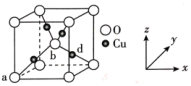
(列出计算式即可)
-
(1) 现有铜锌元素的4种微粒,①锌:[Ar]3d104s2;②锌:[Ar]3d104s1;③铜:[Ar]3d104s1;④铜:[Ar]3d10。失去一个电子需要的最低能量由大到小的顺序是(填字母)。
A ④②①③ B ④②③① C ①②④③ D ①④③②
-
(2) 砷化镉(Cd3As2)是一种验证三维量子霍尔效应的材料。
①砷与卤素可形成多种卤化物,AsBr3、AsCl3、AsF3的熔点由低到高的顺序为。砷酸的酸性弱于硒酸,从分子结构的角度解释原因。
②Cd2+与NH3形成配离子[Cd(NH3)4]2+中,配体的空间构型为,画出配离子的结构式(不考虑立体构型)。
-
(3) 铬(Cr)、钼(Mo)、钨(W)位于同一副族相邻周期,且原子序数依次增大。
①基态铬原子、钼原子的核外电子排布特点相同,则基态钼原子的价层电子排布图为。
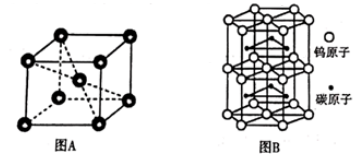
②铬的晶胞结构如图A所示,它的堆积模型为,在该晶胞中铬原子的配位数为。
③钨和碳能形成耐高温、耐磨材料碳化钨,其晶胞结构如图B所示,则碳化钨的化学式为,六棱柱的底边长为a cm,高为b cm,设阿伏加德罗常数的值为NA , 则碳化钨晶体的密度是g·cm-3(列出计算表达式)。
-
(1) 基态Co2+的价电子轨道表示式为。
-
(2) Co2+与CN-结合形成配合物[Co(CN)6]4- , 其中与Co2+结合的C原子的杂化方式是。
-
(3) NH3分子与Co2+结合成配合物[Co(NH3)6]2+ , 与游离的氨分子相比,其键角∠HNH(填“较大”,“较小”或“相同”),解释原因。
-
(4) Li2O熔点为1570℃,CoO的熔点为1935℃,解释后者熔点更高的主要原因是。
-
(5) 图(a)所示石墨晶体按ABAB方式堆积而成,图(b)为石墨的六方晶胞。
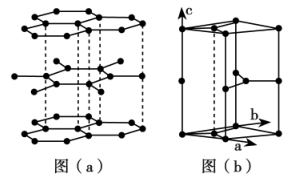
每个晶胞中的碳原子个数为,在下图中画出晶胞沿c轴的投影(用“●”标出碳原子位置即可)。
-
(1) 钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Fe的基态原子价电子排布式为。
②Ti的基态原子共有种不同能级的电子。
-
(2) 制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由小到大的顺序是(用元素符号表示)。
②CCl4和COCl2分子中所有原子均满足8电子构型,CCl4和COCl2分子中σ键的个数比为,COCl2分子的中心原子的杂化方式为。
-
(3) NiO、FeO的晶体结构均与氯化钠的晶体结构相同,从微观角度解释NiO的熔点高于FeO的原因为。
-
(4) Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
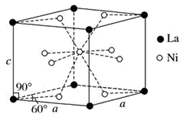
①该晶体的化学式为。
②已知该晶胞的摩尔质量为Mg·mol-1 , 密度为dg·cm-3.设NA为阿伏加德罗常数的值,则该晶胞的体积是cm3(用含M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:a=500pm,c=400pm;标准状况下氢气的密度为9×10-5g·cm-3;储氢能力=
 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为。(NA可近似取6×1023 ,
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为。(NA可近似取6×1023 , 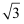 =1.7)
=1.7)
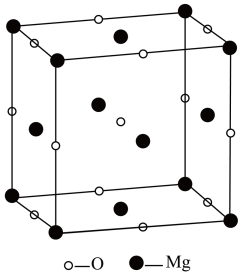
 距离相等且最近的
距离相等且最近的 共有8个
C . 一个晶胞中含有4个MgO
D . 晶体的熔点:CaO>MgO
共有8个
C . 一个晶胞中含有4个MgO
D . 晶体的熔点:CaO>MgO
- 阅读下面这首宋诗,完成(1)~(2)题。春 日 吴锡畴① 韶光大半去匆匆,几许幽情递不通。 燕未成家寒食雨,人如中酒落花
- 如图1,在中,,,,另有一等腰梯形()的底边与重合,两腰分别落在AB、AC上,且G、F分别是AB、AC的中点.1.直接写
- “某物体由静止开始在t时间内运动了S的路程”,仅凭这段描述,你只能得到( )
- 下图是二战后日本经济发展总量柱状图,导致这一状况的原因是( ) ①美国的扶植 ②战后政治民主化改革
- 如图所示,三条平行等距的虚线表示电场中的三个等势面,电势值分别为10V、20V、30V,实线是一带负电的粒子(不计重力)
- 墨子说:“尽也农夫之所以早出暮入,强乎耕稼树艺,多聚菽粟,而不敢怠倦者,何也?曰:彼以为强必富,不强必贫;强必饱,不强必
- 在氮化硅中添加氧化铝,用氧原子取代一部分氮,用铝原子取代一部分硅,通过常压烧结即成为新一代无机非金属材料,叫氧氮化硅铝,
- In spite of repeated wrongs done to him, he looks _____ to p
- 在“研究平抛运动”实验中,某同学只记录了小球运动途中的A、B、C三点的位置,取A点为坐标原点,则各点的位置坐标如图所示,
- 当前世界交通运输的发展趋势是 ( ) ①提高运
- 下列由左到右的变形哪 是因式分解,哪 不是(是的打“∨”,不是的打“×”): a3-b3=(a-b)(a2+ab+b2
- (12分)如图所示,A、B为两块平行金属薄板,A板带正电、B板带负电。两板之间存在着匀强电场,两板间距为d、电势差为U,
- All her life, my mother wanted busy children. It was very im
- 下列反应中,既属于离子反应,又属于有颜色变化的氧化还原反应的是( ) A.FeCl3溶液和KSCN溶
- 根据相关知识回答下列问题: (1)实验开始时,关闭K1,开启K2和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。过一会儿
- 下列加点的成语使用不正确的一项是( ) A、这些第三代移民,在物质方面已经西化,但在精神方面,祖国母亲赋予他们的文化底蕴
- I saw him______ the game on the computer yesterday evening.
- 正常情况下,以下物质属于人体内环境组成成分的是 ( ) ①血红蛋白 ②葡萄糖 ③无机盐
- 对下列曲线图相关解释,正确的是() A. 甲图所示植物的光合作用和呼吸作用的最适温度相同 B.
- 右图所示为蒋介石的一封信件,来源于国民政府军委会战时新闻检查局档案。由此可见,当时 A.蒋介石反对抗日民族统一战线



