画元素的原子结构示意图 知识点
画元素的原子结构示意图 知识点题库
-
(1) 画出砷的原子结构示意图.
-
(2) 工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫.写出发生反应的化学方程式.该反应需要在加压下进行,原因是.
-
(3) 已知:As(s)+
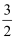 H2(g)+2O2(g)=H3AsO4(s)△H1
H2(g)+2O2(g)=H3AsO4(s)△H1H2(g)+
 O2(g)=H2O(l)△H2
O2(g)=H2O(l)△H22As(s)+
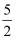 O2(g)=As2O5(s)△H3
O2(g)=As2O5(s)△H3则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的△H=.
-
(4)
298K时,将20mL 3x mol•L﹣1 Na3AsO3、20mL 3x mol•L﹣1 I2和20mL NaOH溶液混合,发生反应:AsO33﹣(aq)+I2(aq)+2OH﹣⇌AsO43﹣(aq)+2I﹣(aq)+H2O(l).溶液中c(AsO43﹣)与反应时间(t)的关系如图所示.
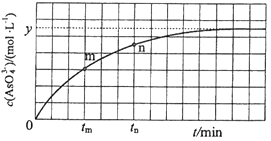
①下列可判断反应达到平衡的是(填标号).
a.溶液的pH不再变化
b.v(I﹣)=2v(AsO33﹣)
c.c (AsO43﹣)/c (AsO33﹣)不再变化
d.c(I﹣)=y mol•L﹣1
②tm时,v正 v逆(填“大于”“小于”或“等于”).
③tm时v逆tn时v逆(填“大于”“小于”或“等于”),理由是.
④若平衡时溶液的pH=14,则该反应的平衡常数K为.
请回答与这两种物质中元素有关的一些问题。
-
(1) 基态铁原子的核外电子排布式为;基态铜原子的电子占据的最高能层符号为 。
-
(2) 氧元素的第一电离能小于氮元素,其原因是 。
-
(3) SO42-、H2O、NH4+三种微粒中,空间构型为正四面体的是;NH4+中氮原子的杂化轨道类型是。
-
(4) 写出与SO42-互为等电子体的分子的化学式 (写一种)。
-
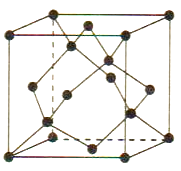
(5) Cu与Au的合金可形成面心立方最密堆积的晶体,在该晶胞中Cu 原子处于面心,该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图) 相似,该晶体储氢后的化学式为,若该晶体的密度为ρg.cm-3 , 则晶胞中Cu原子与Au原子中心的最短距离d=cm (NA表示阿伏加德罗常数的值)。
-
(1) 现代化学中,常利用上的特征谱线来鉴定元素。Ga的外围电子排布式为:,基态Ga原子核外有种运动状态不同的电子。
-
(2) 锗、砷、硒、溴的第一电离能由大到小的顺序为(用元素符号表示);其中锗的化合物四氯化锗可用作光导纤维掺杂剂,其熔点为-49.5℃,沸点为83.1℃,则其晶体类型为,中心原子的杂化类型为;砷酸的酸性弱于硒酸,从分子结构的角度解释原因。
-
(3) 铁能形成[Fe(Bipy)2Cl2]ClO4等多种配合物(Bipy结构如下图A)。
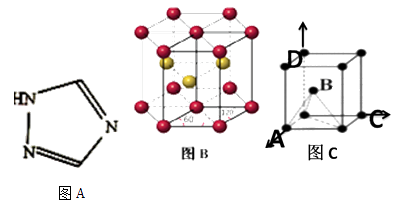
①该配合物中中心原子的化合价为;与中心原子形成配位键的原子是。
②与ClO4-互为等电子体的一种非极性分子是(举1例)。
③1 mol Bipy中所含σ键mol。
-
(4) 钛(Ti)被誉为“21世纪金属”,Ti晶体的堆积方式是六方最密堆积如图B所示,晶胞可用图C表示。设金属Ti的原子半径为a cm,空间利用率为。设晶胞中A点原子的坐标为(1,0,0),C点原子的坐标为(0,1,0),D点原子的坐标为(0,0,1),则B点原子的坐标为。
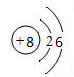 C .
C . 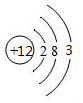 D .
D . 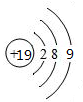
-
(1) 现有下列十种物质:① H2O、② 空气、③ Mg、④ H2SO4、⑤ CaO、⑥ CuSO4、⑦ 碘酒、⑧ Ca(OH)2、⑨ 酒精、⑩ NaHCO3 , 其中属于混合物的是(填序号,下同),属于氧化物的是,属于酸的是,属于碱的是,属于盐的是。
-
(2) 用化学用语填空:
氯原子的结构示意图;Na2O2中氧元素的化合价为;5个磷酸根离子;
-
(3) NH4+的摩尔质量为。
-
(1) A,B,C,D 的元素符号分别为、、、。
-
(2) B2−的电子式为,D 原子的结构示意图为,B与C形成的简单化合物的电子式为。
 D . 标准状况下密度为1.25g/L的气态烃的球棍模型:
D . 标准状况下密度为1.25g/L的气态烃的球棍模型: 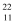 Na
B . 氯原子的结构示意图:
Na
B . 氯原子的结构示意图:  C . NaCN的电子式:
C . NaCN的电子式: 

![]()
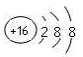 B .
B . 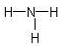 D . 2311Na+
D . 2311Na+
|
元素编号 |
元素性质与原子(或分子)结构 |
|
T |
最外层电子数是次外层电子数的3倍 |
|
X |
常温下单质分子为双原子分子, 分子中含有3对共用电子对 |
|
Y |
M层比K层少1个电子 |
|
Z |
第三周期元素的金属离子中半径最小 |
-
(1) 写出元素T的原子结构示意图:。
-
(2) 元素Y与元素Z相比,金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是(填字母)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质与水反应剧烈
d.Y最高价氧化物对应的水化物的碱性比Z的强
-
(3) T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式:。
-
(4) 元素T和氢元素以原子个数比为1∶1化合形成化合物Q,元素X与氢元素以原子个数比1∶2化合形成常用于火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式: 。
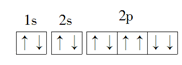 B . Na+的结构示意图:
B . Na+的结构示意图: |
X |
L层电子数是K层电子数的3倍 |
|
Y |
核外电子层数等于原子序数 |
|
Z |
L层电子数是K层和M层电子数之和 |
|
W |
最外层电子数是次外层电子数的2.5倍 |
-
(1) 写出W的原子结构示意图:。
-
(2) 元素X与元素Z相比,非金属性较强的是(填元素名称),写出一个能表示X、Z非金属性强弱关系的化学方程式:。
-
(3) X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为。
-
(4) 元素X和元素Y以原子个数之比1∶1化合形成化合物Q,元素W和元素Y化合形成化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒且在自然界中稳定存在的物质,M的结构式为,写出该反应的化学方程式。
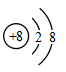 、
、 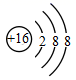 、
、 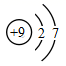 B .
B . 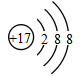 C .
C . 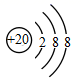 D .
D . 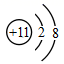


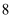 的
的 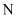 原子:
原子: 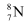 B .
B . 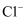 的结构示意图:
的结构示意图: 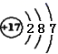 C .
C . 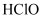 的电子式:
的电子式: |
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
1 |
① |
|||||||
|
2 |
② |
③ |
④ |
|||||
|
3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
||
|
4 |
-
(1) 请画出元素⑨阴离子的结构示意图:。
-
(2) ②⑥⑦的原子半径由大到小的顺序为(填元素符号)。
-
(3) ①-⑨号元素中元素的最高价氧化物对应的水化物中酸性最强的是,碱性最强的是,③ 、⑧两种元素的最简单氢化物的熔点较高的是(均用化学式表示)。
-
(4) ③⑤两种元素的原子按1:1组成的常见化合物的电子式为;元素⑤的最高价氧化物对应水化物中含有的化学键类型为。
-
(5) 欲比较③和⑧两种元素的非金属性强弱,可以作为验证的证据是(填字母)。
A 比较这两种元素单质的沸点
B 比较这两种元素单质与氢气化合的难易
C 比较这两种元素的最高价氧化物对应水化物的酸性
-
(6) ⑨单质与水反应的离子方程式为。
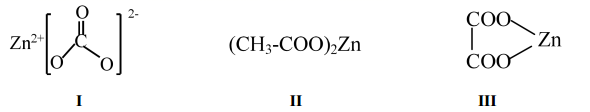
回答下列问题:
-
(1) Zn为30号元素,它在元素周期表中的位置是。
-
(2) 原料Ⅰ中阴离子空间结构为,其等电子体为(写出1种即可)。
-
(3) 原料Ⅱ、Ⅲ阴离子对应的酸沸点较高的是(写结构简式),原因是。
-
(4) 关于以上几种锌盐说法正确的是____。A . 化合物Ⅱ中电负性最大的元素是O B . 化合物Ⅱ中所有C原子的杂化形式均为sp3 C . 化合物Ⅲ中只存在离子键和极性共价键 D . 化合物Ⅰ阴离子中σ键和π键数目比为2:1
-
(5) ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,下图为这两种晶体的局部结构。
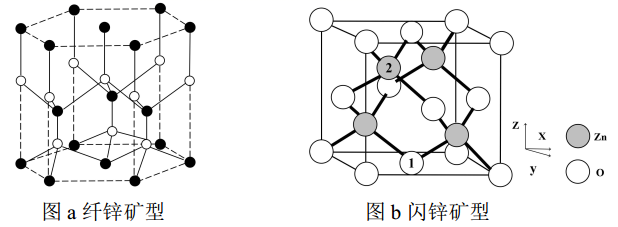
①图a不是纤锌矿型ZnO的晶胞单元,原因是。
②图b闪锌矿型属于立方晶胞,原子1的坐标为
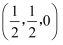 , 则原子2的坐标为。
, 则原子2的坐标为。③图
 的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为,其晶胞参数为a nm,阿伏加德罗常数的值为NA , 则晶体密度为g/cm3(列出计算式)。
的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为,其晶胞参数为a nm,阿伏加德罗常数的值为NA , 则晶体密度为g/cm3(列出计算式)。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ① | |||||||
二 | ② | ③ | ④ | ⑤ | ||||
三 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
四 | ⑩ | |||||||
-
(1) 表中元素⑧的原子结构示意图为,①~⑩元素中,最不活泼的元素是(填元素名称)。
-
(2) ①~⑩元素中,金属性最强的元素是(填元素符号),原子半径最小的元素是(填元素符号);最高价氧化物对应的水化物酸性最强的是(填化学式)。
-
(3) 表中④⑧⑨元素的氢化物的稳定性由强到弱的顺序为(填化学式);写出元素②的氢化物的电子式。
-
(4) 表中元素③与元素⑦形成的物质是(填化学式),写出该物质与⑥的最高价氧化物对应的水化物反应的化学方程式;写出该物质与盐酸反应的离子方程式。
 和
和 B .
B .  和
和 C .
C . 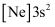 和
和 D .
D .  和
和
- 常温下,下列各组物质中,Y既能与X反应又能与Z反应的是 X Y Z ① NaOH溶液 Al(OH)3 稀硫酸 ② KOH
- (2013北京市海淀区模拟)一般来说,正常人从距地面1.5m高处跳下,落地时速度较小,经过腿部的缓冲,这个速度对人是安
- 在用显微镜观察人的口腔上皮细胞的实验中,下列说法正确的是() A.制作临时装片时要在载玻片的中央滴一滴清水 B.盖盖玻片
- 人口、资源、环境等要素与一个国家发展息息相关。确保国家的资源安全,倡导发展低碳经济和低碳生活是各国的共识。根据下列材料,
- 某反应的微观示意图如下(一种小球代表一种元素的原子),下列说法错误的是()。A.该反应中共有三种元素 B.图中反应物都是
- 如图,连接四边形ABCD各边中点,得到四边形EFGH,只要添加条件,就能保证四边形EFGH是菱形.
- Several years ago, a friend of mine andher husband were inv
- 金融界网站2011年9月21日讯:在9月21日银行间外汇市场上,l美元兑人民币6.3772元,而前一交易日为l 美元兑
- 有一歌词是“红日照遍了东方,自由之神在纵情歌唱,看吧,千山万壑铜墙铁壁,抗日的烽火,燃烧在太行山上。气焰千万丈,听吧,母
- 郭嵩焘在担任英国大使时写信给李鸿章说:“中国之人患,在于士大大没有见识。”他这里所说的“见识”,在李鸿章看来,应该是(
- 周末商场搞促销活动,其中一顾客想购买一件衣服、一双鞋和一套化妆品,这三件物品的原价和优惠方式如下表所示:欲购买的商品原价
- “大树底下好乘凉”是因为植物的蒸腾作用能增湿降温。这说明 A.植物生长需要光合作用 B.生物能适应环境 C.
- They looked forward with hope _____ from you, but you never
- 如图,抛物线y=x2-x+a与x轴交于点A,B,与y轴交于点C,其顶点在直线y=-2x上.1.求a的值;2.求A,B的坐
- 如图,已知是△的外接圆的直径,=13 cm, ,则的长等于( )A.5 cm B.6 cm
- 下表为两个地区的人口指标。据此回答15~16题: 地区 出生率 死亡率 A 1.
- 大蒜中含有的一种有效成分“硫化丙烯”(C3H6S),具有一定的杀菌食疗价值。下列 有关C3H6S的说法正确的是
- 浓盐酸与次氯酸钙能发生反应Ca(ClO)2+4HCl(浓)===CaCl2+2Cl2↑+2H2O,用贮存很久的漂白粉与浓
- 已知物体A受三个力F1=12 N,F2=10 N,F3=6 N,如图3-5-4所示.求A受的合力. 图3-5-4
- 下图表示蛙的发育过程,正确的发育顺序是 A.②→③→④→⑤→① B.④→②→③→⑤→① C.③→②→④→⑤→



