物质结构与性质 知识点题库
固体A的化学式为NH5 , 它的所有原子的最外层都符合相应稀有气体原子的最外层电子结构,则下列有关说法中,不正确的是( )
A . 1mol NH5中含有5NA个N﹣H键(NA表示阿伏加德罗常数)
B . NH5中既有共价键又有离子键,它属于离子化合物
C . NH5的电子式为: 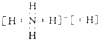 D . 它与H2O反应的化学方程式为:NH5+H2O═NH3•H2O+H2↑
D . 它与H2O反应的化学方程式为:NH5+H2O═NH3•H2O+H2↑
根据信息及要求填空.(写出元素名称)
-
(1) B原子3p能级上有一个未成对电子,常温下B单质呈气态,B是元素.
-
(2) C原子L层上的电子数等于次外层上的电子数、电子层数,C是元素.
-
(3) D原子L层上有二个轨道充满电子,D是元素.
-
(4) L原子核外电子占有9个轨道,而且有一个未成对电子,L是元素.
下列关于晶体的说法正确的组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、H2O、H2S晶体的熔点依次降低
④离子化合物中只有离子键没有共价键,分子晶体中肯定没有离子键
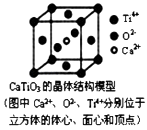
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2﹣相紧邻
⑥金刚石硬度很大是因为金刚石的分子间作用力很强
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠溶于水时离子键被破坏.
A . ①②③⑥
B . ①②④
C . ③⑤⑦
D . ③⑤⑧
下列说法正确的是( )
A . 金属与非金属元素形成的化合物一定是离子化合物
B . 干冰气化过程中只需克服分子间作用力
C . HF的热稳定性很好,是因为HF分子间存在氢键
D . 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构
下列化合物分子中含2个手性碳原子的是( )
A . 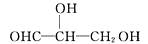 B .
B . 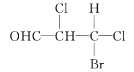 C .
C . 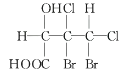 D .
D . 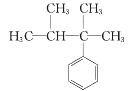
 C .
C .  D .
D . 
下列原子的电子跃迁能释放光能形成发射光谱的是( )
A . 1s22s22p63s2―→1s22s22p63p2
B . 1s22s22p33s1―→1s22s22p4
C . 1s22s2―→1s22s12p1
D . 1s22s22p 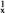 ―→1s22s22p
―→1s22s22p 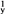
日本福岛核电站泄漏的核燃料衰变产物有放射性元素 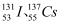 等,其中
等,其中 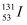 可以用来治疗甲状腺癌,但是如果没有癌症,它也可能诱发甲状腺癌。下列有关说法中错误的是( )
可以用来治疗甲状腺癌,但是如果没有癌症,它也可能诱发甲状腺癌。下列有关说法中错误的是( )
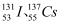 等,其中
等,其中 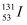 可以用来治疗甲状腺癌,但是如果没有癌症,它也可能诱发甲状腺癌。下列有关说法中错误的是( )
可以用来治疗甲状腺癌,但是如果没有癌症,它也可能诱发甲状腺癌。下列有关说法中错误的是( )
A . 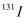 的原子核所含中子数是78
B . 核能的利用证实了原子的可分性
C .
的原子核所含中子数是78
B . 核能的利用证实了原子的可分性
C .  原子和放射性碘原子
原子和放射性碘原子 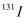 互为同位素
D .
互为同位素
D .  原子和碘
原子和碘 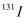 原子的质子数不同
原子的质子数不同
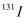 的原子核所含中子数是78
B . 核能的利用证实了原子的可分性
C .
的原子核所含中子数是78
B . 核能的利用证实了原子的可分性
C .  原子和放射性碘原子
原子和放射性碘原子 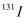 互为同位素
D .
互为同位素
D .  原子和碘
原子和碘 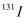 原子的质子数不同
原子的质子数不同
短周期主族元素X、Y、Z的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z的核电荷数比Y多4。下列说法正确的是( )
A . 原子半径的大小顺序:Z>Y>X
B . Y分别与Z、X形成的化合物中化学键类型相同
C . 单质Z能在X的最高价氧化物中燃烧
D . Y、X的简单气态氢化物的热稳定性:Y<X
下列物质中所含的化学键只有离子键的是( )
A . KCl
B . NaOH
C . HCl
D . SO3
H2和I2在一定条件下发生反应:H2(g)+I2(g)  2HI(g) ΔH=-akJ·mol-1。已知:
2HI(g) ΔH=-akJ·mol-1。已知:
 2HI(g) ΔH=-akJ·mol-1。已知:
2HI(g) ΔH=-akJ·mol-1。已知: 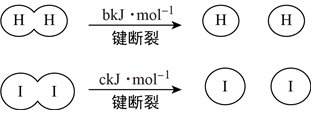 (a、b、c均大于零)
(a、b、c均大于零)
下列说法错误的是( )
A . 该反应中反应物的总能量高于生成物的总能量
B . 断开1 mol H—H键和1 mol I—I键所需能量大于断开2 mol H—I键所需能量
C . 断开2 mol H—I键所需能量约为(a+b+c) kJ
D . 向密闭容器中加入2 mol H2和2 mol I2 , 充分反应后放出的热量小于2akJ
 是常规核裂变产物之一,可以通过测定大气或水中
是常规核裂变产物之一,可以通过测定大气或水中  的含量变化来检测核电站是否发生放射性物质泄漏。下列有关
的含量变化来检测核电站是否发生放射性物质泄漏。下列有关  的叙述中错误的是( )
的叙述中错误的是( )
A .  的化学性质与
的化学性质与 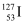 相同
B .
相同
B .  的质子数为53
C .
的质子数为53
C .  的原子核外电子数为78
D .
的原子核外电子数为78
D .  的原子核内中子数多于质子数
的原子核内中子数多于质子数
 的化学性质与
的化学性质与 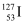 相同
B .
相同
B .  的质子数为53
C .
的质子数为53
C .  的原子核外电子数为78
D .
的原子核外电子数为78
D .  的原子核内中子数多于质子数
的原子核内中子数多于质子数
下列各离子或原子的电子排布式错误的是( )
A . Ca2+:1s22s22p63s23p6
B . O2-:1s22s22p4
C . K: 1s22s22p63s23p64s1
D . Fe3+:1s22s22p63s23p63d5
有关晶体的结构如图所示,下列说法中错误的是( )
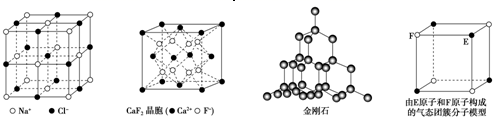
A . 在NaCl 晶体中,距Na 最近的Cl 形成正八面体
B . 在  晶体中,每个晶胞平均占有4 个Ca2+
C . 在金刚石晶体中,碳原子与碳碳键个数的比为1:2
D . 该气态团簇分子的分子式为EF或FE
晶体中,每个晶胞平均占有4 个Ca2+
C . 在金刚石晶体中,碳原子与碳碳键个数的比为1:2
D . 该气态团簇分子的分子式为EF或FE
 晶体中,每个晶胞平均占有4 个Ca2+
C . 在金刚石晶体中,碳原子与碳碳键个数的比为1:2
D . 该气态团簇分子的分子式为EF或FE
晶体中,每个晶胞平均占有4 个Ca2+
C . 在金刚石晶体中,碳原子与碳碳键个数的比为1:2
D . 该气态团簇分子的分子式为EF或FE
表中元素①~⑧均为短周期元素:
| 元素 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/ | 0.066 | 0.160 | 0.152 | 0.077 | 0.099 | 0.186 | 0.070 | 0.082 |
| 最外层电子数 | 6 | 2 | 3 | |||||
| 常见化合价 | +1 | -4,+4 | -1,+7 | -3、+5 | ||||
| 焰色实验 | 黄色 |
下列说法错误的是( )
A . ③单质能在①或⑦的单质中燃烧
B . ②和⑥元素原子的失电子能力强弱可通过单质与水反应比较
C . ⑤分别与⑦、⑧形成的最简单分子的空间构型相同
D . 第一电离能大小顺序: 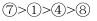
碳、氮和铬的相关化合物在药物化学及催化化学等领域应用广泛。请回答下列问题:
-
(1) 基态铬原子价电子排布式为,未成对电子数为。
-
(2) 铬的一种含氧酸——铬酸(H2CrO4),结构和硫酸类似。其阴离子CrO
 的立体构型为,铬酸是一种二元强酸,原因是。
的立体构型为,铬酸是一种二元强酸,原因是。
-
(3) 含铬的化合物吡啶甲酸铭是一种用于二型糖尿病的保健药,其结构如图所示。
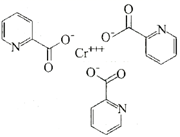
①该化合物中H、C、N、O的电负性由大到小的顺序为,N原子的杂化轨道类型为。
②该化合物中含有的化学键类型有(填字母)。
a.离子键 b.极性键 c.非极性键 d.配位键 e.氢键
-
(4) 铬的某种氧化物晶胞如图所示(灰球代表铬原子,黑球代表氧原子)。
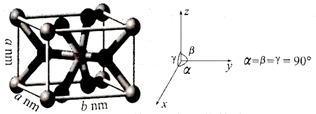
该氧化物的化学式为,铬原子的配位数是;该晶体的密度为g·cm-3(用NA表示阿伏加德罗常数的值,列出计算式即)。
已知C3N4晶体具有比金刚石还大的硬度,且构成该晶体的微粒间只以单键结合。关于C3N4晶体的说法错误的是( )
A . 该晶体属于共价晶体,其化学键比金刚石中的C-C键更牢固
B . 该晶体中碳原子和氮原子的最外层都满足8电子结构
C . 该晶体中每个碳原子连接4个氮原子,每个氮原子连接3个碳原子
D . 该晶体与金刚石结构相似,都是原子间以非极性共价键形成空间网状结构
GaAs晶体被业内称为“半导体贵族" ,2001年7月31日,我国科学家宣布掌握其生产技术,中国成为继日本和德国之后第三个拥有此项技术的国家。它的熔点很高,硬度很大,其原子间以共价键(配位键)相连,密度为ρg·cm-3 , Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1 , 原子半径分别为rGapm和rAspm,阿伏加德罗常数的值为NA , 其晶胞结构如图所示。下列说法错误的是( )
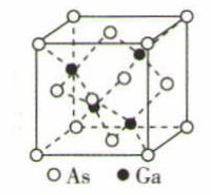
A . 该晶体为离子晶体
B . 在该晶体中Ga和As的配位数均为4
C . 所有原子均满足8电子稳定结构
D . 原子的体积占晶胞体积的百分比为 ×100%
×100%
 ×100%
×100%
下列物质中不含共价键的是( )
A . 水
B . 甲烷
C . 二氧化碳
D . 单质氦
下列粒子的中心原子的杂化轨道类型和粒子的空间结构错误的是( )
A .  中P原子为sp3杂化,分子空间结构为三角锥形
B .
中P原子为sp3杂化,分子空间结构为三角锥形
B .  中O原子为sp杂化,分子空间结构为直线形
C .
中O原子为sp杂化,分子空间结构为直线形
C . 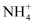 中N原子为sp3杂化,分子空间结构为正四面体形
D .
中N原子为sp3杂化,分子空间结构为正四面体形
D .  中S原子为sp2杂化,分子空间结构为V形
中S原子为sp2杂化,分子空间结构为V形
 中P原子为sp3杂化,分子空间结构为三角锥形
B .
中P原子为sp3杂化,分子空间结构为三角锥形
B .  中O原子为sp杂化,分子空间结构为直线形
C .
中O原子为sp杂化,分子空间结构为直线形
C . 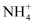 中N原子为sp3杂化,分子空间结构为正四面体形
D .
中N原子为sp3杂化,分子空间结构为正四面体形
D .  中S原子为sp2杂化,分子空间结构为V形
中S原子为sp2杂化,分子空间结构为V形
锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等三十多种对人体有益的微量元素。
-
(1) 基态Ge原子的价电子排布图为。
-
(2) Ni(CO)4常温下为无色液体,沸点42.1℃,熔点−19.3℃,难溶于水,易溶于有机溶剂。推测Ni(CO)4是分子(“极性”或“非性极”)。
-
(3) Co2+可与
 形成配离子[Co(NO3)4]2− , 该配离子中各元素的第一电离能由小到大的顺序为(用元素符号表示),
形成配离子[Co(NO3)4]2− , 该配离子中各元素的第一电离能由小到大的顺序为(用元素符号表示), 中N的杂化方式为。
中N的杂化方式为。
-
(4) 氨气中H−N−H键的键角为107.3°,[Zn(NH3)6]2+离子中H−N−H键的键角107.3°(填“大于”“小于”或“等于”),原因是:。
-
(5) 硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,A点原子的坐标为(0,0,0),B点原子的坐标为(
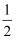 , 1,
, 1,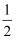 ),则C点原子的坐标为;已知晶胞边长为apm,阿伏加德罗常数的值为NA , 该晶胞密度ρ为g·cm-3(只列出计算式)。
),则C点原子的坐标为;已知晶胞边长为apm,阿伏加德罗常数的值为NA , 该晶胞密度ρ为g·cm-3(只列出计算式)。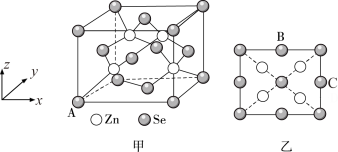
最近更新
- 下列各句中,没有语病的一句是 A.中国足球早就因为糟糕的战绩和球员低下的素质而屡遭诟病,近期爆出的“世界杯赌球风波”则又
- KMnO4溶液常用做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中某些少量还原性物质还
- -_______me you won't breathe a word of this to anyone. - N
- 珠蛋白是血红蛋白的组成成分。如果将来自非洲爪蟾红细胞的珠蛋白mRNA,以及放射性标记的氨基酸,注射到非洲爪蟾的卵细胞中,
- 风景区不少摊贩出售景区内捕杀和采挖的动植物资源,如此会造成()。 A.环境污染 B.对文物古迹的破坏 C.对正常社会秩序
- “凡年满六周岁的儿童,不分性别、民族、种族,应当入学接受规定年限的义务教育”,这是我国哪部法律的规定( )A、《中华人民
- 小沛用如图所示装置测量空气中氧气含量,集气瓶容积为700mL,集气瓶内水的体积为100mL,实验开始前量筒200mL,实
- 如果U={1,2,3,4,5},M={1,2,3},N=,那么(∁)∩N等于() A. B.{5}
- 历史地图中蕴含着丰富的历史信息。右图反映的中国古代政治制度有 A.分封制 B.行省制 C.郡县制
- 下列各风向示意图中,表示南半球近地面的是
- (8分)现有①CaF2 ②金刚石 ③ 冰④干冰 ⑤Na2SO4 ⑥碘片 ⑦ 二氧化硅七种物质,按下列要求回答(填序
- 在△ABC中,已知D是AB边上一点,若,且,则( ) A. B.
- 下列图示与对应的叙述不相符的是() A. 如图表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
- 2011年新华网电:距离8月2日最后期限日的前一天,美国国会众议院8月1日最终高票通过了提高美国债务上限法案。国会参议院
- 如果全球变暖,南极冰川全部融化,我国将被淹没的地区是 ( ) A.东北平原
- 近年来,中国民乐在欧洲的主流音乐厅多次上演,为欧洲听众带去了充满中国韵味的音乐享受,受到了较高的评价。这表明 A.
- 豌豆种子的形状是由一对等位基因R和r控制的,下表是有关豌豆种子形状的三组杂交试验结果。据表回答问题。组合序号 杂交组 合
- 读我国某地潜水位埋深与气象要素相关模式图,回答当潜水位埋深小于15米时,该地区A.空气相对湿度大于70%
- 读图,回答问题。海拔高于600米的区域面积约为
- 在“用油膜法估测分子大小”实验中,油酸酒精溶液的浓度为1000mL溶液里有纯油酸0.6mL,用注射器测得1mL上述溶液