离子浓度大小的比较 知识点题库
 )=c(K+)=c(Ba2+)
D . 0.2mol•L﹣1某一元弱酸HA溶液和0.1mol•L﹣1NaOH溶液等体积混合后的溶液:2c(OH﹣)+c(A﹣)=2c(H+)+c(HA)
)=c(K+)=c(Ba2+)
D . 0.2mol•L﹣1某一元弱酸HA溶液和0.1mol•L﹣1NaOH溶液等体积混合后的溶液:2c(OH﹣)+c(A﹣)=2c(H+)+c(HA)
-
(1) 常温下,浓度均为0.1mol/L的下列五种钠盐溶液的pH如表;
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
上述盐溶液中的阴离子,结合氢离子能力最强的是;根据表中数据,浓度均为0.01mol/L的下列四种酸的溶液分别稀释100倍,pH变化最大的是(填序号).
A.HCN B.HClO C.CH3COOH D.H2CO3
-
(2) 有①100mL0.1mol/L碳酸氢钠 ②100mL0.1mol/L碳酸钠两种溶液,溶液中水电离出的氢离子个数:①②(填“>”“=”“<”下同);溶液中阴离子的物质的量浓度之和:①②.
-
(3) 实验室中常用氢氧化钠来进行洗气和提纯.
①当150mL1mol/L的氢氧化钠溶液吸收标况下2.24L二氧化碳时,所得溶液中各离子浓度由大到小的顺序为:常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有.
②几种离子开始沉淀时的pH如表:
离子
Fe2+
Cu2+
Mg2+
pH
7.6
5.2
10.4
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,(填离子符号)先沉淀,Ksp[Fe(OH)3]Ksp[Mg(OH)2](填“>”“=”或“<”),要使0.2mol/L硫酸铜溶液中铜离子沉淀较为完全(使铜离子浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为.( Ksp[Cu(OH)2]=2×10﹣20 )
-
(1) 已知部分弱酸的电离常数如下表:
弱酸
HCOOH
HCN
H2CO3
电离常数(25℃)
Ka = 1.77×10 -4
Ka=4.3×10-10
Ka1=5.0×10-7
Ka2=5.6×10-11
①0.1 moI/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)c(HCO3 -)(填“>”、“<”或“=”)。
②常温下,pH相同的三种溶液
A.HCOONa B.NaCN C.Na2CO3 ,
其物质的量浓度由大到小的顺序是(填编号)。
③已知25℃时,HCOOH( aq) +OH -( aq)=HCOO-(aq) +H2O(1) △H=-a kJ/mol
H+(aq) +OH-(aq) =H2O(1) △H=-b kJ/mol
甲酸电离的热化学方程式为。
④将少量CO2通入NaCN溶液,反应的离子方程式是。
⑤室温下,—定浓度的HCOONa溶液pH =9,用离子方程式表示溶液呈碱性的原因是:,溶液中
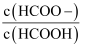 =。
=。 -
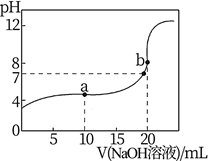
(2) 室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.100mol/L 的某氨水溶液,滴定曲线如图所示。
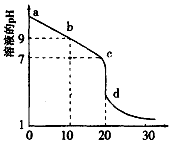
①d点所示的溶液中离子浓度由大到小的顺序依次为。
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=(用溶液中的其它离子浓度表示)。
③pH =10的氨水与pH =4的NH4Cl溶液中,由水电离出的c(H+)之比为。
-
(3) 已知Ksp(BaCO3) =2.6×10-9 , Ksp( BaSO4)=1.1×10-10.
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为mol/L。
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中
 =(保留三位有效数字)。
=(保留三位有效数字)。
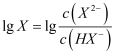 或
或  。下列叙述不正确的是( )
。下列叙述不正确的是( ) 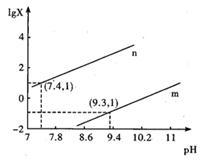
 与pH的变化关系
B . Ka1(H2X)的数量级为10-7
C . 当溶液呈中性时,C(HX-)>C(X2-)>C(H2X)
D . 25℃时,NaHX溶液中:C(OH-)>C(H+)
与pH的变化关系
B . Ka1(H2X)的数量级为10-7
C . 当溶液呈中性时,C(HX-)>C(X2-)>C(H2X)
D . 25℃时,NaHX溶液中:C(OH-)>C(H+)
| 物质 | HCOOH | CH3COOH | NH3·H2O |
| 电离平衡常数K | 1.77×10−4 | 1.75×10−5 | 1.76×10−5 |
下列说法错误的是( )
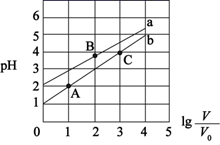
 的电离程度大于其水解程度
C . NaH2PO2溶液中:c(Na+)+c(H+)=c(H2PO
的电离程度大于其水解程度
C . NaH2PO2溶液中:c(Na+)+c(H+)=c(H2PO  )+c(OH-)
D . 图中A,B,C点溶液中水的电离程度由大到小的顺序是:B>C>A
)+c(OH-)
D . 图中A,B,C点溶液中水的电离程度由大到小的顺序是:B>C>A
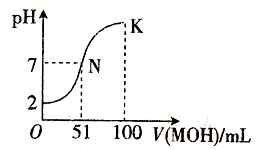
 溶液滴加到
溶液滴加到 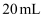 等浓度的某一元酸(HA)溶液中,测得混合溶液的pH与微粒浓度变化关系如图所示[已知:
等浓度的某一元酸(HA)溶液中,测得混合溶液的pH与微粒浓度变化关系如图所示[已知: 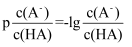 ]。下列说法错误的是( )
]。下列说法错误的是( ) 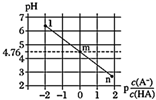
 溶液体积小于
溶液体积小于 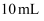 B .
B .  的数量级为
的数量级为  C . l点所示溶液中:
C . l点所示溶液中: 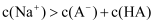 D . n、m、l三点,n点水的电离程度最大
D . n、m、l三点,n点水的电离程度最大
|
化学式 |
CH3COOH |
H2SO3 |
HClO |
H2CO3 |
H2C2O4 |
|
电离平衡常数 |
K =1.8×10-5 |
K1=1.2×10-2 K2=6.6 ×10-8 |
K =3.0×10-8 |
K1=4.4×10-7 K2=4.7×10-11 |
K1=5.4×10-2 K2=5.4×10-5 |
-
(1) Na2C2O4水解的离子方程式为。
-
(2) ①常温下,用0.200 mol/L NaOH溶液滴定20.00 mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:
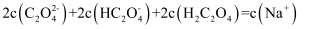
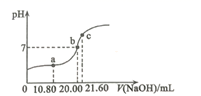
该草酸溶液的物质的量浓度为。
②c点所示溶液中,c(Na+)、c(H+)、c(OH-)、c(
 )、c(
)、c(  )各离子的浓度由大到小的顺序为。
)各离子的浓度由大到小的顺序为。 -
(3) 以下反应的离子方程式书写正确的是。
A 次氯酸钠溶液吸收少量二氧化硫:ClO-+SO2+H2O=HClO+

B 漂白液生效的原理:ClO-+CO2+H2O=HClO+

C Na2CO3溶液吸收少量SO2:2
 +SO2+H2O=
+SO2+H2O=  +2
+2 
-
(4) 已知100℃时,水离子积为1×10-12 , 将此温度下pH=1的H2SO4溶液b L与pH=11的NaOH溶液a L混合,若所得混合液pH=2,则a:b=。
-
(5) 常温下,将SO2通入氨水中,当溶液中的
 =50/33时,此时使溶液的pH为。
=50/33时,此时使溶液的pH为。
-
(1) 某温度(t℃)时,测得0.01 mol∙L-1的NaOH溶液的pH=11,则该温度下水的kW=。在此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液Vb L混合。若所得混合液的pH=10,且a=12,b=2,则:Va ︰Vb=。
-
(2) 室温时,向100mL0. 1 mol∙L-1NH4HSO4溶液中滴加0.1 mol∙L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:试分析图中a、b、c、d四个点,水的电离程度最大的是:在b点,溶液中阳离子浓度由大到小的排列顺序是。
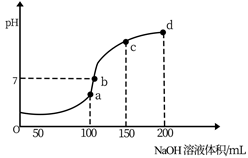
-
(3) 煤燃烧排放的烟气含有SO2和NO,采用碱性的 NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为
 。反应10min后溶液中离子浓度的分析结果如下表。
。反应10min后溶液中离子浓度的分析结果如下表。
离子




Cl-
c/(mol∙L-1)
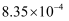
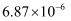
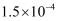
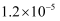
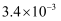
①写出NaClO2溶液脱硝过程中主要反应的离子方程式。
②如果采用Ca(ClO)2替代 NaClO2 , 其脱硫效果会更好。试从化学平衡原理分析,Ca(ClO)2相比 NaClO2具有的优点是。
 C . a点所示的溶液中
C . a点所示的溶液中 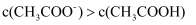 D . b点所示的溶液中
D . b点所示的溶液中 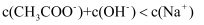
-
(1)
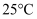 时,物质的量浓度均为
时,物质的量浓度均为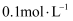 的几种盐溶液的
的几种盐溶液的 如下表所示。
如下表所示。序号
Ⅰ
Ⅱ
Ⅲ
溶液
 溶液
溶液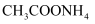 溶液
溶液 溶液
溶液
5
7
8.4
①溶液Ⅰ显酸性的原因是(用离子方程式表示)。
②溶液Ⅱ中,
 (填“>”“<”或“=”)
(填“>”“<”或“=”)  。
。③写出溶液Ⅲ中阴离子浓度由大到小的关系:。
-
(2) 几种离子开始沉淀时的
 如下表所示。
如下表所示。离子




7.6
5.2
10.4
①当向含相同浓度
 的溶液中滴加氢氧化钠溶液时,(填离子符号)最先沉淀。
的溶液中滴加氢氧化钠溶液时,(填离子符号)最先沉淀。②
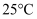 时,要使
时,要使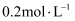 硫酸铜溶液中铜离子浓度降至原来的千分之一,则应向溶液里加入氢氧化钠溶液,使溶液
硫酸铜溶液中铜离子浓度降至原来的千分之一,则应向溶液里加入氢氧化钠溶液,使溶液 为。
为。
-
(3) 已知:
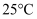 时,
时,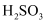 的电离常数
的电离常数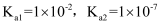 , 则该温度下
, 则该温度下 的水解平衡常数
的水解平衡常数 ,若向
,若向 溶液中加入少量的
溶液中加入少量的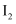 , 则溶液中
, 则溶液中 将(填“增大”“减小”或“不变”)。
将(填“增大”“减小”或“不变”)。
-
(4) 已知常温下
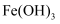 和
和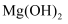 的
的 分别为
分别为 , 浓度均为
, 浓度均为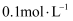 的
的 、
、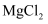 的混合溶液中.要使
的混合溶液中.要使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而
)而 不沉淀,应该调节溶液
不沉淀,应该调节溶液 的范围是,调节
的范围是,调节 应选用的试剂是.(填化学式)。
应选用的试剂是.(填化学式)。
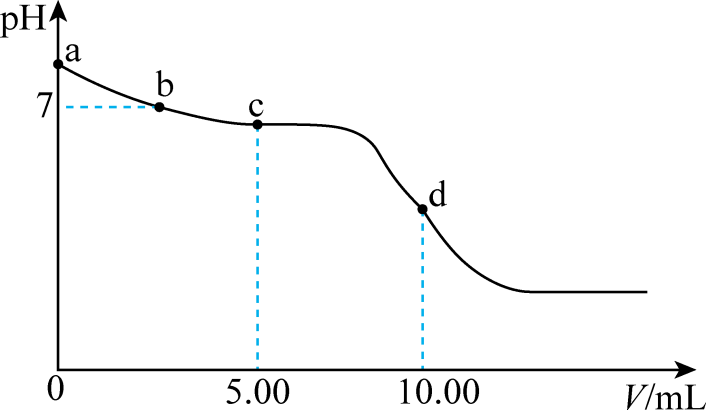
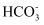 水解程度大于电离程度
B . b点,c(Na+)=c(
水解程度大于电离程度
B . b点,c(Na+)=c(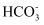 )+c(
)+c( )+c(Cl−)
C . c点,溶液中H+的主要来自
)+c(Cl−)
C . c点,溶液中H+的主要来自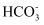 的电离
D . d点,c(Na+)= c(Cl−)=0.0500mol/L
的电离
D . d点,c(Na+)= c(Cl−)=0.0500mol/L

 溶液中逐渐加入
溶液中逐渐加入 固体(忽略加入时引起的溶液体积变化),所得溶液中含Y元素的三种微粒的分布系数(浓度分数)
固体(忽略加入时引起的溶液体积变化),所得溶液中含Y元素的三种微粒的分布系数(浓度分数)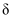 随溶液pH变化的关系如图所示,下列说法正确的是 ( )
随溶液pH变化的关系如图所示,下列说法正确的是 ( )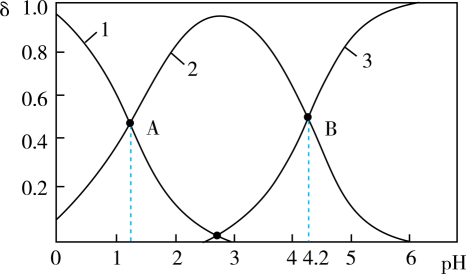
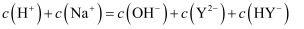 B .
B . 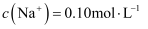 时,溶液中的
时,溶液中的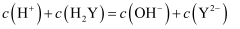 C . 由图可知,
C . 由图可知, 为二元弱酸,如果将物质的量浓度均为0.20
为二元弱酸,如果将物质的量浓度均为0.20 的
的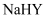 和
和 溶液等体积混合,所得溶液的
溶液等体积混合,所得溶液的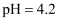 D . 已知25℃时,
D . 已知25℃时,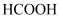 的
的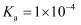 。若把少量
。若把少量 加入
加入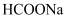 溶液中,发生的离子反应可表示为:
溶液中,发生的离子反应可表示为: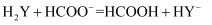
- X、Y、Z、W四块金属板分别用导线两两相连浸入稀硫酸中构成原电池。X、Y相连时,X为负极;Z、W相连时,外电路电流方向是
- 阅读下面的文章,回答1~4题。 美丽的五指山 ①五指山是海南的第一高山,是海南岛的象征,也是我国名山之一,被国际旅游组织
- 25℃时,下列四种溶液中,由水电离生成的氢离子浓度之比是 ( ) ①pH=
- 读下面“南半球某地海平面等压线分布图”,图中A、B、C、D四处 所绘箭头能正确表示当地风向的是 A.A B.B
- 同属于欧洲近代的思想解放运动,启蒙运动有别于文艺复兴,主要表现在 A.发展人文主义 B.批评天主教会
- 阅读下面的短文和问题,根据短文内容,完成对该问题的回答。答语要书写工整,字迹清楚,结构正确,不多于八个单词。
- 某同学在学习“细胞工程”时,列表比较了动植物细胞工程的有关内容,你认为有几处不正确?( )植物细胞工程 动物细胞工
- 7、检测还原糖、蛋白质、油脂、淀粉的试剂分别是:( ) A.本尼迪特试剂、苏丹Ⅲ、碘-碘化钾溶液、双缩脲试剂
- 认为人是环境的产物而忘记了环境是由人来改变的观点是 A. 唯物主义观点 B. 形而上学观点 C. 唯心主义观点 D. 形
- 受地势影响,亚洲河流( )A.呈放射状流向周边的海洋 B.呈环状围绕着青藏高原C.呈放
- Let’sask him ________ his best photos here tomorrow. A.bring
- 下列各句中加点的成语使用恰当的一句是( ) A.战士们奋战了一天一夜,吃不上饭,喝不上水,但是他们忘乎所以,继续
- 俄国二月革命和十月革命的相同背景是 A、列宁提出了明确的社会主义革命任务 B、两个政权并立 C、沙皇实行专制统治
- Mr Ascot, headmaster of the school, refused to accept ______
- 蛋白质的结构多种多样,在细胞中承担的功能也是多种多样的。下列不属于动植物体内蛋白质功能的是
- 一物体放置在倾角为的斜面上,斜面固定于加速上升的电梯中,加速度为,如图所示.在物体始终相对于斜面静止的条件下,下列说法中
- 最近科学家发现,水在﹣157℃超低温、正常压力或真空条件下仍呈液态,比蜂蜜还粘稠。下列关于这种“高密度液态水”的说法正确
- 下列说法正确的是( )A. 葡萄糖、果糖和蔗糖都能发生水解反应 B.糖类、油脂、蛋白质都是由C、H、O三种元
- 决定19世纪音乐发展呈现出多样性和民族性的主要原因是( ) A.19世纪欧洲各国资本主义的进一步发展 B.封建主义和
- 在某省人民代表大会上,人民代表在审议政府财政预算报告时,就某些问题质询财政厅厅长,要求他做出答复。同时,在审议人民法院的



