化学反应速率与化学平衡的综合应用 知识点题库
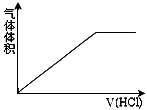 表示Na2CO3溶液中滴入稀盐酸
B .
表示Na2CO3溶液中滴入稀盐酸
B . 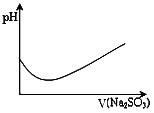 表示溴水中滴入Na2SO3溶液
C .
表示溴水中滴入Na2SO3溶液
C . 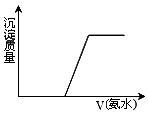 表示AgNO3溶液中滴入氨水
D .
表示AgNO3溶液中滴入氨水
D . 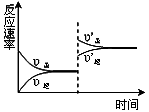 表示一定条件下2SO2+O2⇌2SO3△H<0达平衡后,升高温度
表示一定条件下2SO2+O2⇌2SO3△H<0达平衡后,升高温度
-
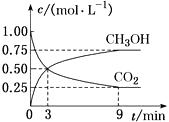
(1) CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1mol CO2和3mol H2 , 一定条件下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。①从3min到9min,v(H2)=mol·L-1·min-1。
②该反应的平衡常数为。
③下列说法正确的的是(填字母)。
A.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
B.平衡时CO2的转化率为75%
C.平衡时混合气体中CH3OH(g)的体积分数是30%
D.该条件下,第9min时v逆(CH3OH)大于第3min时v正(CH3OH)。
-
(2) 工业中,CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)反应B:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如左下图所示。
①由图可知温度升高CO的产率上升,其主要原因可能是。
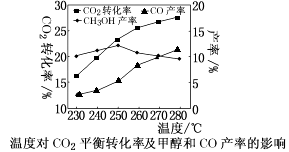
②由图可知获取CH3OH最适宜的温度是。下列措施有利于提高CO2转化为CH3OH的平衡转化率的有(填字母)。
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
-
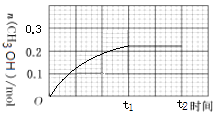
(3) 250℃下CH3OH物质的量随时间的变化曲线如右上图所示。画出280℃下0~t2时刻CH3OH物质的量随时间的变化曲线。
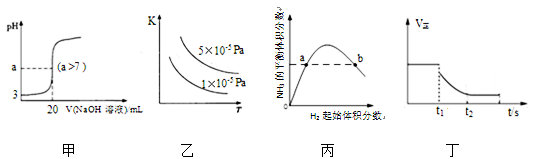
 2SO3(g) △H<0的平衡常数K与温度和压强的关系
C . 图丙表示一定条件下的合成氨反应,N2的起始量恒定时,NH3的平衡体积分数随H2起始体积分数的变化,图中a点N2的转化率等于b点
D . 图丁表示反应 2SO2+O2
2SO3(g) △H<0的平衡常数K与温度和压强的关系
C . 图丙表示一定条件下的合成氨反应,N2的起始量恒定时,NH3的平衡体积分数随H2起始体积分数的变化,图中a点N2的转化率等于b点
D . 图丁表示反应 2SO2+O2  2SO3 , t1 时刻降低温度符合图示变化
2SO3 , t1 时刻降低温度符合图示变化
 HCOOH(g) △H,测得,n(H2)/mol在不同温度随时间的变化如下表:
HCOOH(g) △H,测得,n(H2)/mol在不同温度随时间的变化如下表: | 实验编号 | 时间/min | 60 | 90 | 120 | 150 | 180 |
| Ⅰ | T1/K | 1.50mol | 1.32 mol | 1.28 mol | 1.26 mol | 1.26 mol |
| Ⅱ | T2/K | 1.45mol | 1.20 mol | 1.10 mol | 1.10 mol | 1.10 mol |
-
(1) 实验I中0~60min内用HCOOH表示的该反应的平均反应速率为。
-
(2) 实验II反应开始时体系压强为P0 , 第90min时体系压强为P1 , 则P1:P0=。
-
(3) T2温度下反应的平衡常数为。
-
(4) 比较实验温度T1T2(填“>”或“<”),该反应的△H0(填“>”、“=”或“<”)。
-
(5) 下列说法正确的是_______(填编号)。A . 当CO2、H2和HCOOH的物质的量浓度之比为1:1:1时,该反应达到平衡 B . 容器中气体密度不再改变,不能判断该反应是否达到平衡 C . 将HCOOH液化后分离既能提高转化率又能加快反应速率 D . 选用更高效的催化剂可提高生产效率
-
(1) Ⅰ.干法脱除:在催化剂存在下,COS和H2可发生两个平行反应:
i. COS(g)+H2(g)
 H2S(g)+CO(g)△H1=-17kJ/mol
H2S(g)+CO(g)△H1=-17kJ/molii. COS(g)+4H2(g)
 H2S(g)+CH4(g)+H2O(g) △H2
H2S(g)+CH4(g)+H2O(g) △H2已知:CH4(g)+H2O(g)
 CO(g)+3H2(g)△H=+206kJ/mol,则△H2=。
CO(g)+3H2(g)△H=+206kJ/mol,则△H2=。 -
(2) T1℃时,向10L恒容密闭容器中充人1molCOS和4molH2 , 发生反应i和ii。5min时达到平衡,测得体系压强减少了20%,CO的体积分数为10%且其平衡分压为P1。
①0-5min内,v(COS)=。
②反应i的平衡常数K=。
③若在起始温度为T1℃的绝热容器中重复上述实验,H2的平衡分压P2P1(填“>”“=”或“<”),理由为。
-
(3) Ⅱ.湿法脱除:原理为COS+4OH-=S2-+CO32-+2H2O。温度为293K时,将COS以固定流速匀速通入一定浓度的NaOH溶液中,测得体系内c(S2-)随时间(t)的变化如图所示:
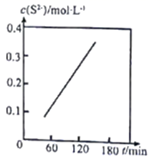
由图可知,增大NaOH溶液的初始浓度,COS的吸收速率(填“增大”“减小”或“不变”),判断依据为。
-
(4) 在上述反应体系中同时加入少量溴水,也能吸收COS并得到澄清溶液,发生反应的化学方程式为。
 是一种重要的化工原料,主要用于生产三氧化硫、亚硫酸盐等,生产
是一种重要的化工原料,主要用于生产三氧化硫、亚硫酸盐等,生产  的反应为
的反应为 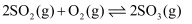
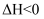 。实验室用浓硫酸和
。实验室用浓硫酸和  固体反应制取少量
固体反应制取少量  。
。  排放到大气中会形成酸雨。下列有关生产
排放到大气中会形成酸雨。下列有关生产 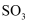 反应的说法正确的是( )
反应的说法正确的是( )
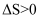 B . 反应中每消耗
B . 反应中每消耗 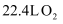 转移的电子的物质的量为
转移的电子的物质的量为 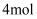 C . 升温、加压和使用催化剂能增大
C . 升温、加压和使用催化剂能增大 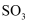 的生成速率
D . 当
的生成速率
D . 当 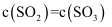 时,说明该反应处于平衡状态
时,说明该反应处于平衡状态
I. 
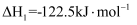
Ⅱ. 
回答下列问题:
-
(1) 反应
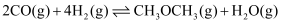 的△H=。
的△H=。
-
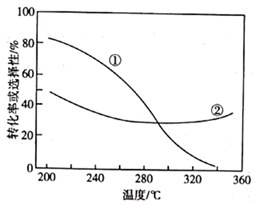
(2) 在压强、CO2和H2的起始投料一定的条件下,发生反应Ⅰ、Ⅱ,实验测得 CO2平衡转化率和平衡时 CH3OCH3的选择性随温度的变化如图所示。
已知:
 的选择性=
的选择性=  ×100%。其中表示平衡时
×100%。其中表示平衡时  的选择性的是曲线(填"①"或"②");温度高于 300℃时,曲线②随温度升高而升高的原因是;为同时提高 CO2的平衡转化率和平衡时
的选择性的是曲线(填"①"或"②");温度高于 300℃时,曲线②随温度升高而升高的原因是;为同时提高 CO2的平衡转化率和平衡时  的选择性,应选择的反应条件为(填标号)。
的选择性,应选择的反应条件为(填标号)。a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
-
(3) 也可以利用甲醇脱水制备二甲醚:
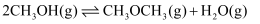 。已知:
。已知: 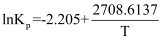 ,其中 Kp为以分压表示的平衡常数,T 为热力学温度。
,其中 Kp为以分压表示的平衡常数,T 为热力学温度。
①为提高 CH3OCH3的平衡产率,可以采取的措施有(任写一条)。
②473 K时,在密闭容器中加入一定量 CH3OH(g),采用合适的催化剂进行反应,达到平衡时体系中 CH3OCH3(g)的物质的量分数为(填标号)。
a.<
 b.
b.  c.
c. 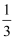 ~
~  d. >
d. > 
-
(4) 对于反应
 ,反应速率v=v正-v逆=k正p(CO2)·p(H2)-k逆p(CO)·p(H2O),其中k正、k逆分别为正、逆反应速率常数,p为气体的分压(分压=总压×物质的量分数)。
,反应速率v=v正-v逆=k正p(CO2)·p(H2)-k逆p(CO)·p(H2O),其中k正、k逆分别为正、逆反应速率常数,p为气体的分压(分压=总压×物质的量分数)。
①降低温度,k正-k逆(填"增大"、"减小"或"不变");
②在TK、101kPa下,按照
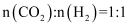 投料,CO2转化率为50%时,
投料,CO2转化率为50%时,  ,用气体分压表示的平衡常数 Kp=。
,用气体分压表示的平衡常数 Kp=。
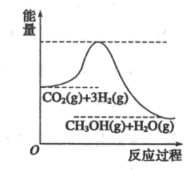
 N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法错误的是( )
N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法错误的是( )
-
(1) 该反应为(填“放热”或“吸热”)反应。
-
(2) 恒容容器中,对于以上反应,能加快反应速率的是。
a.升高温度 b.充入氮气 C.加入合适的催化剂 d.降低压强
-
(3) 在体积为2L的密闭容器中,充入1molCO2和3molH2 , 测得CO2的物质的量随时间变化如表所示。
t/min
0
2
5
10
15
n(CO2)/mol
1
0.75
0.5
0.25
0.25
从反应开始到5min末,用H2浓度变化表示的平均反应速率v(H2)=;反应达到平衡状态,此时H2的转化率为。
-
(4) 在相同温度、容积不变的条件下,不能说明该反应已达平衡状态的是。
a.CO2、H2、CH3OH、H2O的浓度均不再变化
b.体系压强不变
c.n(CO2):n(H2):n(CH3OH):n(H2O)=1:1:1:1
d.H2的消耗速率与CH3OH的消耗速率之比为3:1
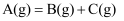 ,若反应物的浓度由
,若反应物的浓度由 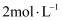 降到
降到 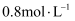 需要
需要 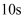 ,那么反应物浓度再由
,那么反应物浓度再由 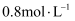 降到
降到 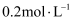 所需要的时间为( )
所需要的时间为( )
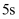 B . 小于
B . 小于 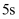 C . 大于
C . 大于 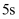 D . 无法判断
D . 无法判断
 C2H5OH(g), 下图为乙烯的平衡转化率与温度(T)、压强(p) 的关系[ 起始n(C2H4)∶n(H2O)=1∶1]。下列有关叙述正确的是( )
C2H5OH(g), 下图为乙烯的平衡转化率与温度(T)、压强(p) 的关系[ 起始n(C2H4)∶n(H2O)=1∶1]。下列有关叙述正确的是( ) 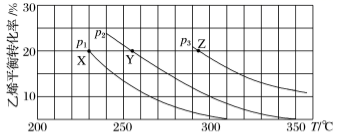
 B . X、Y、Z 对应的反应速率:v(X)>v(Y)>v(Z)
C . X、Y、Z 对应的平衡常数数值:KX<KY<KZ
D . 增大压强、升高温度均可提高乙烯的平衡转化率
B . X、Y、Z 对应的反应速率:v(X)>v(Y)>v(Z)
C . X、Y、Z 对应的平衡常数数值:KX<KY<KZ
D . 增大压强、升高温度均可提高乙烯的平衡转化率
 在9月22日召开的联合国大会上表示:“中国将争取在2060年前实现碳中和”。所谓“碳中和”,通俗地说,日常活动可能制造的二氧化碳排放量,通过植树、节能减排等方法来中和抵消。
在9月22日召开的联合国大会上表示:“中国将争取在2060年前实现碳中和”。所谓“碳中和”,通俗地说,日常活动可能制造的二氧化碳排放量,通过植树、节能减排等方法来中和抵消。
-
(1) CO2甲烷化反应是由法国化学家PaulSabatier提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程如图1:
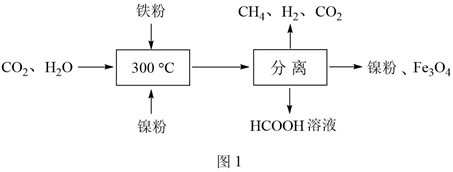
①上述过程中,加入铁粉的作用是。
②HCOOH是CO2转化为CH4的中间体:CO2
 HCOOH
HCOOH  CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是。
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是。 -
(2) 一定条件下,Pd-Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为,反应过程中碳元素的化合价为-2价的中间体是。
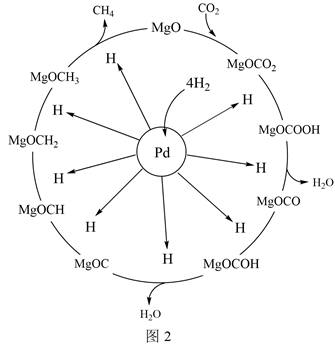
-
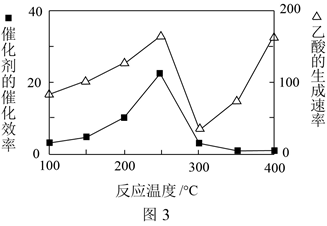
(3) CO2和CH4是两种重要的温室气体,通过化学反应可以将它们转化为其他物质。以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如图3所示,250~300℃时,温度升高而乙酸的生成速率降低的原因是。
②为了提高该反应中CH4的转化率,可以采取的措施是。
已知: ![]() (g)=
(g)= ![]() (g)+H2(g) ΔH1=100.3kJ·mol-1①
(g)+H2(g) ΔH1=100.3kJ·mol-1①
H2(g)+I2(g)=2HI(g) ΔH2=-11.0kJ·mol-1②
对于反应: 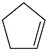 (g)+I2(g)=
(g)+I2(g)= ![]() (g)+2HI(g) ΔH3③
(g)+2HI(g) ΔH3③
-
(1) 关于反应③的判断(填“低温自发”、“高温自发”或者“任意条件均自发”),理由为。
-
(2) 某温度下,等物质的量的碘和环戊烯(
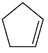 )在恒容容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,该反应的平衡常数Kp=Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有(填标号)。
)在恒容容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,该反应的平衡常数Kp=Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有(填标号)。 A.通入惰性气体
B.再充入碘和环戊烯各2mol
C.提高温度
D.增加环戊烯浓度
E.增加碘浓度
-
(3) 环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是___(填标号)。
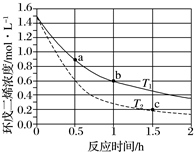 A . T1>T2 B . a点的反应速率小于c点的反应速率 C . a点的正反应速率大于b点的逆反应速率 D . b点时二聚体的浓度为0.45mol·L-1
A . T1>T2 B . a点的反应速率小于c点的反应速率 C . a点的正反应速率大于b点的逆反应速率 D . b点时二聚体的浓度为0.45mol·L-1 -
(4) 环戊二烯可用于制备二茂铁(Fe(C5H5)2结构简式为
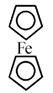 ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制各原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。该电解池的总反应式为,电解制备需要在无水条件下进行,原因为。
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制各原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。该电解池的总反应式为,电解制备需要在无水条件下进行,原因为。 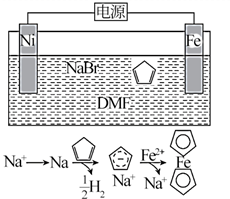
 HCHO(g)+H2(g)
HCHO(g)+H2(g) 
 。Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
。Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下: 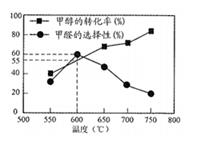
历程ⅰ: 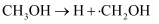
历程ⅱ: 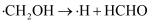
历程ⅲ: 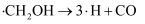
历程ⅳ: 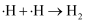
如图所示为在体积2L的恒容容器中,投入1molCH3OH,在碳酸钠催化剂作用下,经过
5min反应,测得甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的CH3OH中生成HCHO的百分比),下列有关说法正确的是( )
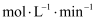 B . 700℃时,反应历程ⅱ的速率小于反应历程ⅲ的速率
C . 脱氢法制甲醛中,在高温高压条件下更有利于提高平衡产率
D . 反应历程ⅰ的活化能大于CH3OH(g)
B . 700℃时,反应历程ⅱ的速率小于反应历程ⅲ的速率
C . 脱氢法制甲醛中,在高温高压条件下更有利于提高平衡产率
D . 反应历程ⅰ的活化能大于CH3OH(g)  HCHO(g)+H2(g)的活化能
HCHO(g)+H2(g)的活化能
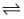 cC(g)+dD(s) △H=-QkJ/mol,反应过程中,当其它条件不变时,C在混合物中的含量与温度(T)的关系如图1所示,反应速率(v)与压强(p)的关系如图2所示。据图分析,以下说法正确的是( )
cC(g)+dD(s) △H=-QkJ/mol,反应过程中,当其它条件不变时,C在混合物中的含量与温度(T)的关系如图1所示,反应速率(v)与压强(p)的关系如图2所示。据图分析,以下说法正确的是( )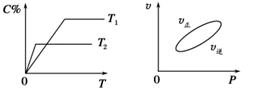
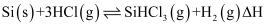 是工业上制备高纯硅的重要中间过程。一定压强下,起始投入原料
是工业上制备高纯硅的重要中间过程。一定压强下,起始投入原料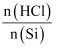 的值和温度与
的值和温度与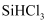 的平衡产率的变化关系如图所示。下列说法不正确的是( )
的平衡产率的变化关系如图所示。下列说法不正确的是( )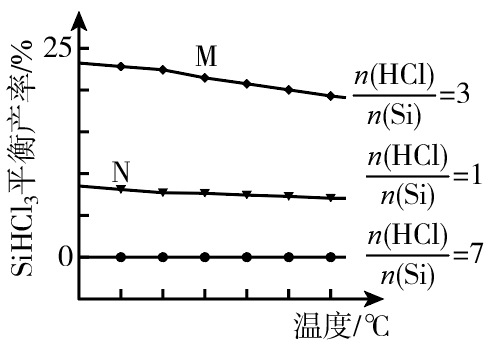
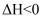 B . M、N点
B . M、N点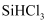 的分压:
的分压: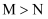 C .
C . 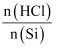 的值越大
的值越大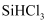 平衡产率越高
D . M、N点的逆反应速率:
平衡产率越高
D . M、N点的逆反应速率:
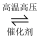 2NH3 , 开始时加入4 mol H2、4molN2和1molNH3 , 在5min末测得NH3的物质的量为2mol。下列说法正确的是( )
2NH3 , 开始时加入4 mol H2、4molN2和1molNH3 , 在5min末测得NH3的物质的量为2mol。下列说法正确的是( )
-
(1) (一)制备苯乙烯(原理如反应I所示):
Ⅰ.
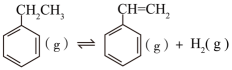 △H=+124kJ·mol-1
△H=+124kJ·mol-1部分化学键的键能如下表所示:
化学键
C-H
C-C
C=C
H-H
键能/ KJ/mol
412
348
X
436
根据反应I的能量变化,计算X=。
-
(2) 工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气。请用化学平衡理论解释通入水蒸气的原因:。
-
(3) 已知吉布斯自由能△G=△H-T△S ,当△G < 0时反应可自发进行。由此判断反应I在(填“高温”或“低温”)更易自发进行。
-
(4) (二)制备α-氯乙基苯(原理如反应Ⅱ所示):
Ⅱ.
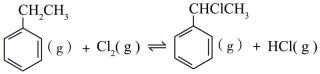 △H2>0
△H2>0T℃时,向10 L恒容密闭容器中充入2mol乙苯(g)和2 mol Cl2(g)发生反应Ⅱ,乙苯(或Cl2)、 α-氯乙基苯(或HCl)的物质的量浓度(c)随时间(t)变化的曲线如图所示:
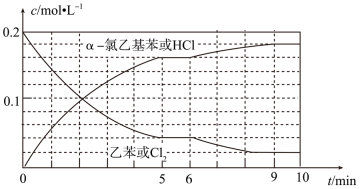
①0—2 min内,以HCl表示的该反应速率v(HCl)=。
②6 min时,改变的外界条件为,该条件下的平衡常数K的数值=。
③10 min时,保持其他条件不变,再向容器中充入1 mol乙苯、1 mol Cl2、1 molα-氯乙基苯和1mol HCl,则此时该反应v正v逆(填“>”、“<”或“=” );若12 min时反应再次达到平衡,则在0-12 min内,Cl2的转化率α=。(计算结果保留三位有效数字)
-
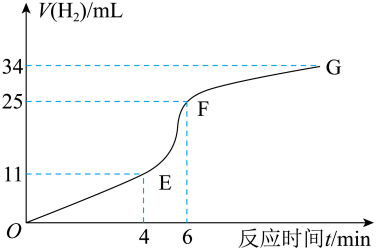
(1) Ⅰ.用纯净的锌粒与稀盐酸反应制取氢气,请回答:
实验过程如图所示,分析判断段化学反应速率最快(答“O~E”、“E~F”或“F~G”)。
-
(2) 将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生
 的速率逐渐加快,其原因是。
的速率逐渐加快,其原因是。
-
(3) Ⅱ.一定温度下,在体积为0.5L的恒容密闭容器中,
 和之间发生反应:
和之间发生反应: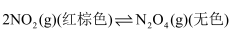 , 反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
, 反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题: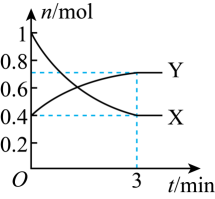
曲线(填“X”或“Y”)表示
 的物质的量随时间的变化曲线。
的物质的量随时间的变化曲线。 -
(4) 在
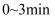 内,用
内,用 表示的反应速率为。
表示的反应速率为。
-
(5) 若在一绝热(不与外界发生热交换)容器中加入一定量
 , 反应一段时间后,混合气体温度升高,说明
, 反应一段时间后,混合气体温度升高,说明 的能量比
的能量比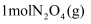 的能量(填“高”或“低)。
的能量(填“高”或“低)。
-
(6) 下列叙述能说明该反应已达到化学平衡状态的是____(填标号)。A . 容器内压强不再发生变化 B . 混合气体的密度不变 C . 混合气体的平均相对分子质量不变 D .
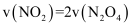 E . 相同时间内消耗nmol的Y的同时消耗2nmol的X
E . 相同时间内消耗nmol的Y的同时消耗2nmol的X
-
(7) 氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极为极(填“正”或“负”)。

- 在中,已知是边上一点,若,则( ) A. B.
- 二次函数的图象如图所示,对称轴是直线,则下列四个结论错误的是 A. B. C. D.
- While building a tunnel through the mountain, ___________. A
- 有一段时期,明斯克生产的一粒纽扣在当地售价是1卢布,在700公里外的莫斯科售价也是1卢布,而在万里之外的海参崴售价仍是1
- 下列说法正确的是 (
- 一个动物精原细胞进行减数分裂时可形成4个四分体,则精细胞的染色体、染色单体、DNA分子数分别是() A.4、0、4B.2
- 阅读下面一段文字,按要求作文。 田野里、山坡上、道路旁、花园中,我们经常能够看到一朵朵鲜艳的花,不管脚下的土地是否肥沃,
- 硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]是分析化学中重要的试剂,常用于代替硫酸亚铁。 已知:硫酸亚铁铵在
- 有关金属晶体的说法不正确的是:() A.金属Cu的晶体的配位数为12 B.金属键是金属阳离子与自由电子间的相互作用 C.
- 阅读下列短文,完成小题。(一) 美景,总在半梦半醒①在故乡的夜晚,一本书,一杯自制的五味子果汁,就会给我带来踏实的睡眠。
- 若某种限制性核酸内切酶的识别序列是CCTAGG,它在A和G之间切断DNA。下图表示用该酶处理某基因后产生的片段。下列有关
- 9.在人体内环境中可以发生的生理过程是( ) A.食物中的淀粉经消化分解成葡萄糖 B.合成生长
- 在今天如何对待包括儒家学说在内的传统文化,按照唯物辩证法的观点应该( )①以全面肯定的态度保护和弘扬传统文化②以辩证否
- 2016年福建省计划选聘大学生村官800名,选聘对象为本省生源的普通高等院校全日制应届大学本科、硕士研究生毕业生。大学生
- --- Is Bob still working in your school? --- I’m afraid
- 某无色透明溶液中,由水电离出来的c(H+)=1×10-13 mol·L-1,在该溶液中一定能够大量共存的离子组是()A
- 单项选择。 —What_______ heavy rain it was! —Yes, but I love ____
- 国家结构形式要解决的问题是 ( ) A.国家政权掌握在谁的手里的问题 B.国家政权如何组织的问题 C.国家的领土如
- 在化学学习中使用数轴的表示方法可收到直观形象的效果,,下列表述中错误的是( ) A.分散质微粒的大小
- 在一容积可变的密闭容器中,aA(气) bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是



