化学平衡中反应条件的控制 知识点题库
 B(g)+2C(g)
B(g)+2C(g)
-
(1) 元素Z在周期表中位于第族.我国首创以W组成的金属﹣海水﹣空气电池作为能源的新型海水标志灯,它以海水为电解质溶液,靠空气中的氧气使W组成的金属不断氧化而产生电流.只要把灯放入海水中数分钟,就会发出耀眼的白光.
则该电源负极反应为.
-
(2) YO2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VO,有关反应的离子方程式为,由此可知YO2和VO还原性较强的是(写化学式).
-
(3) V的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变如表中反应条件x,该平衡体系中随x递增y递增的是(选填序号).
选项
a
b
c
d
x
温度
温度
加入H2的物质的量
加入甲的物质的量
y
混合气体的平均相对分子质量
平衡常数K
混合气体的密度
达平衡时的甲的转化率
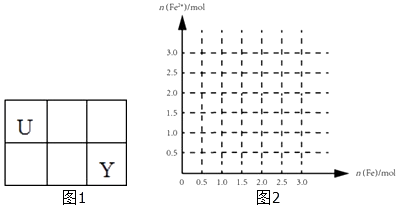
③向含4molV 的最高价含氧酸的稀溶液中,逐渐加入Fe粉至过量.假设生成的气体只有一种,请在图2坐标系中画出n(Fe2+)随n(Fe)变化的示意图.
-
(4) 相同温度下,等体积、物质的量浓度都为0.1mol/L的KZ和CH3COOK溶液的两种溶液中,离子总数相比较 .A . 前者多 B . 一样多 C . 后者多 D . 无法判断.
X | Y | |
A | 减小压强 | A的转化率 |
B | 升高温度 | 混合气体平均分子量 |
C | 升高温度 | A的浓度 |
D | 增加压强 | B的转化率 |
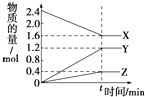
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
 表示混合气体的平均相对分子质量)( )
表示混合气体的平均相对分子质量)( )
 B .
B . 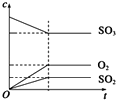 C .
C . 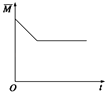 D .
D . 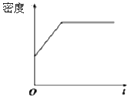
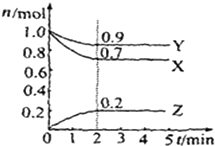
-
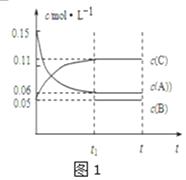
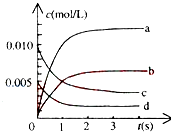
(1) 该反应的化学方程式为.
-
(2) 反应开始至2min,用X表示的平均反应速率为 mol•L﹣1•mi﹣1;
平衡时,Y的转化率为,
平衡时,Z的浓度为 mol•L﹣1 .
-
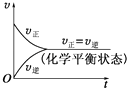
(3) 下列叙述能说明上述反应达到平衡状态的是(填选项、多选)
A.X,Y,Z的物质的量之比为3:1:
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗3mol X,同时生成2mol Z
D.混合气体的总质量不随时间的变化而变化
E.混合气体的总物质的量不随时间的变化而变化.
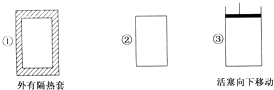
-
(1) a、b应满足的关系是.
-
(2) a的取值范围是.
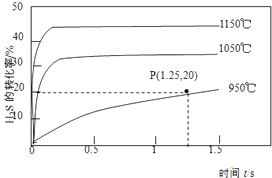
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①图中表示NO2变化的曲线是,用O2表示从0~2s内该反应的平均速率v=.
②能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变.
 bB(g)+cC(g)达到平衡后,保持温度不变,将容器体积增加一倍,最终测得A的物质的量的浓度为原来的55%,则( )
bB(g)+cC(g)达到平衡后,保持温度不变,将容器体积增加一倍,最终测得A的物质的量的浓度为原来的55%,则( )
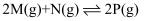 ,其化学平衡常数
,其化学平衡常数 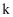 和温度
和温度 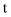 的关系如下表所示:
的关系如下表所示: | | 700 | 800 | 830 | 1000 | 1200 |
| | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
回答下列问题:
-
(1) 该反应的平衡常数表达式
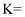 ,该反应的正反应为(填“放热”或“吸热”)反应。
,该反应的正反应为(填“放热”或“吸热”)反应。
-
(2) ①某温度下,平衡浓度符合等式
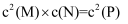 ,试判断此时的温度为
,试判断此时的温度为 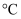 。
。 ②保持此温度不变,在容积为
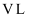 的恒容密闭容器中,充入
的恒容密闭容器中,充入 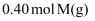 和
和 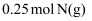 ,反应达到平衡后,测得
,反应达到平衡后,测得 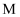 的物质的量占总物质的量的
的物质的量占总物质的量的 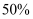 ,此时
,此时 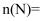
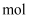 。
。 -
(3) 现将
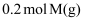 和
和 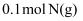 通入某密闭容器中,测得
通入某密闭容器中,测得 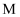 的平衡转化率变化如图所示。
的平衡转化率变化如图所示。 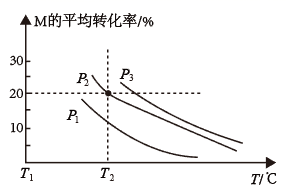
①下列判断正确的是(填标号)。
A.
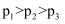 B.
B.  C.
C. 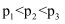 D.
D. 
②
 点的平衡常数
点的平衡常数  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
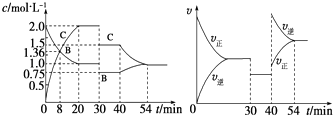
 的污染:
的污染: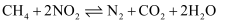 。在温度为T℃时,向5L恒容密闭容器中通入等物质的量的
。在温度为T℃时,向5L恒容密闭容器中通入等物质的量的 和
和 进行反应,反应过程中测定的部分数据见下表:
进行反应,反应过程中测定的部分数据见下表:
| 0 | 5 | 10 | 15 | 20 |
| 2 | 1.6 | 1.45 | ||
| 2 | 1.0 | |||
| 0 | 0.55 |
下列说法错误的是( )
 的物质的量浓度为
的物质的量浓度为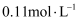 B . 在该温度条件下,反应在15~20min内处于化学平衡状态
C . 在0~10min内,用
B . 在该温度条件下,反应在15~20min内处于化学平衡状态
C . 在0~10min内,用 表示的平均反应速率为
表示的平均反应速率为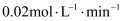 D . 通过调控反应条件,可以使
D . 通过调控反应条件,可以使 完全转化为
完全转化为 除去
除去
- 古诗文名句默写。(10分,(1)至(8)选做6小题,(9)(10)题必做。) (1)过尽千帆皆不是,____ ▲
- 方程的两个根是等腰三角形的底和腰,则这个三角形的周长为( )A.12B.15C.12或15D.17或11
- 下图漫画“是值班,不是加班”的做法说明()①维护了企业和用人单位的利益,是正确的 ②不利于构建和谐稳定的劳动关系 ③损害
- (6分)如图是“探究物质的熔化规律”的实验装置。实验时先将固体物质和温度计分别放入试管内,再放入大烧杯的水中,观察固体的
- 太阳能量来源于太阳内部的________。
- 已知是三角形所在平面内一点,满足,现将一粒黄豆随机撒在三角形内,则黄豆落在三角形内的概率是( ) A.
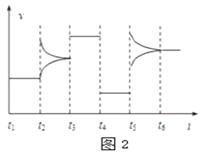
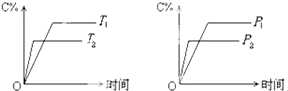
- 下列各图中,表示正反应是吸热反应的图是
- 作为澳大利亚中国文化年的重要视觉艺术展览项目,“心灵的景象——中国当代水墨人物画展”在澳大利亚拉开帷幕,渲染澳大利亚“中
- In today’s Internet age, online games can be a change from t
- 2009年是中华人民共和国成立60周年。在新中国一步一步走向繁荣富强的六十载伟大光荣的历史进程中,中国对世界和平发展大局
- 目前,科学家拟合成一种“二重构造”的球形分子,即把足球型的C60分子融进Si60的分子中,外面的硅原子与里面的碳原子以共
- 下表是元素周期表的一部分,针对表中的a~g元素,回答下列问题:(1)d元素位于金属与非金属的分界线处,常用作
- 已知函数f(x)=|2x﹣1|. (Ⅰ)求不等式f(x)<2的解集; (Ⅱ)若函数g(x)=f(x)+f(x﹣1)的最小
- (本小题满分12分)已知函数,. (I)证明:当时,函数在其定义域内为单调函数;(II)若函数的图象在点(1,)处的切线
- 金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是 ( ) A.硬度很大、熔点很高
- —If you keep on breaking the rules, you will be fired. —
- 如图10,某同学在做“探究平面镜成像的特点”实验时,将一块玻璃板竖直架在一把直尺的上面,取两段相同的蜡烛A和B,将A和B
- 极地狐与大耳狐的耳朵大小明显不同,造成这一差异的环境因素是( )A.温度B.水分C.光照D.空气
- 下列表述不正确的是 ( ) A.磷脂是所有细胞必不可少的脂质 B.淀粉和纤维素都是由许多葡萄糖连接而
- 如图,如果我们要上网搜索右图的历史信息,应键入的“关键词”是A.早期殖民扩张 B.手工工场 C.工业革命 D