焓变和熵变 知识点题库
某反应2AB(g)⇌C(g)+3D(g)在高温时能自发进行,其逆反应在低温下能自发进行,则该反应的正反应的△H、△S应为( )
A . △H>0,△S>0
B . △H<0,△S<0
C . △H<0,△S>0
D . △H>0,△S<0
下列叙述不正确的是( )
A . 铁生锈、白磷燃烧均为自发放热过程
B . 冰融化过程其熵值增大
C . 高温高压下可以使石墨转化为金刚石是自发的化学反应
D . 同一物质固态时熵值最小
下列体系的熵变大于零的是( )
A . 水蒸气冷凝成水
B . CaCO3(s)=CaO(s)+CO2(g)
C . 乙烯聚合成聚乙稀
D . N2O4(g)=2NO2(g)
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+ 2H2(g) ![]() CH3OH(g) △H
CH3OH(g) △H
-
(1) 已知CO(g)、H2(g)的标准燃烧热分别为-283.0kJ•mol-1 , -285.8kJ•mol-1
且CH3OH(g)+3/2O2(g)
 CO2(g)+2H2O(l) △H=-761 kJ•mol-1;
CO2(g)+2H2O(l) △H=-761 kJ•mol-1;则CO(g)+ 2H2(g)
 CH3OH(g)的△H= 。
CH3OH(g)的△H= 。 -
(2) 反应的ΔS0(填“>”、“<”或“=”)。在(填“较高”或“较低”)温度下该反应自发进行。
-
(3) 若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行上述反应,下列事实能说明此反应已达到平衡状态的是 。A . 容器内气体密度保持不变 B . 混合气体的平均相对分子质量不变 C . 生成CH3OH的速率与生成H2的速率相等 D . CO的体积分数保持不变
-
(4) 图1中能正确反映平衡常数K随温度变化关系的曲线为(用a或b表示)。
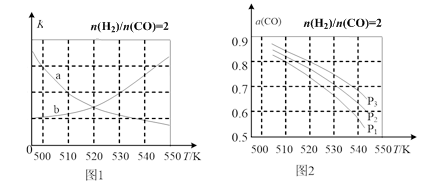
-
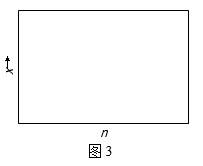
(5) 投料比n(H2)/n(CO)=2时,体系中CO的平衡转化率(α)温度和压强的关系如图2所示。α(CO)值随温度升高而(填“增大”或“减小”)其原因是;图2中的压强由大到小为(用P1 , P2 , P3表示)。
-
(6) 520K时, 投料比n(H2)/n(CO)=2(总物质的量为3mol),维持反应过程中压强p3不变,达到平衡时测得容器体积为0.1L,则平衡常数K=。
若H2和CO的物质的量之比为n∶1(维持反应过程中压强p3不变),相应平衡体系中CH3OH的物质的量分数为x , 请在图3中绘制x随n变化的示意图 。
某化学反应的△H=–122 kJ·mol-1 , △S=+231 J·mol-1·K-1 , 则在下列哪种情况下可自发进( )
A . 在任何温度下都能自发进行
B . 在任何温度下都不能自发进行
C . 仅在高温下自发进行
D . 仅在低温下自发进行
下列有关说法错误的是( )
A . 同一物质的固、液、气三种状态的熵值相同
B . 自发进行的化学反应的方向,应由焓判据和熵判据的复合判据来判断
C . 反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0
D . 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0
-
(1) 高温下,C(s)+H2O(g)
 CO(g)+H2(g) ΔH>0,反应的化学平衡常数表达式K= ,该反应随温度升高,K值(填增大、减小或不变),该反应在高温下自发进行的原因是。
CO(g)+H2(g) ΔH>0,反应的化学平衡常数表达式K= ,该反应随温度升高,K值(填增大、减小或不变),该反应在高温下自发进行的原因是。
-
(2) 向重铬酸钾溶液中加入氢氧化钠固体,溶液的颜色变化为,原因是(请从平衡的角度用化学用语及必要的文字说明)。
-
(3) 密闭容器中充入N2O4达化学平衡,压缩体积达新平衡,整个过程的现象为。
-
(4) 多元弱酸的逐级电离平衡常数为K1、K2、K3……,则K1、K2、K3的大小关系为。
图表示某反应的能量变化,对于该图的理解,你认为一定正确的是:( )
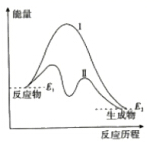
A . 曲线Ⅰ和曲线Ⅱ分别表示两个化学反应的能量变化
B . 曲线Ⅱ可表示反应2KClO3  2KCl+3O2↑的能量变化
C . 该反应不需要加热条件就一定能发生
D . 该反应的ΔH=E2-E1
2KCl+3O2↑的能量变化
C . 该反应不需要加热条件就一定能发生
D . 该反应的ΔH=E2-E1
 2KCl+3O2↑的能量变化
C . 该反应不需要加热条件就一定能发生
D . 该反应的ΔH=E2-E1
2KCl+3O2↑的能量变化
C . 该反应不需要加热条件就一定能发生
D . 该反应的ΔH=E2-E1
下列说法正确的是( )
A . 凡是放热反应都是自发的,因为吸热反应都是非自发的
B . 自发反应的熵一定增大,非自发反应的熵一定减小
C . 常温下,反应C(s)+CO2(g)  2CO(g)不能自发进行,则该反应的ΔH>0
D . 反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
2CO(g)不能自发进行,则该反应的ΔH>0
D . 反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
 2CO(g)不能自发进行,则该反应的ΔH>0
D . 反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
2CO(g)不能自发进行,则该反应的ΔH>0
D . 反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
下列说法正确的是( )
A . 自发反应一定能快速进行,不自发的反应一定不能发生
B . 体系能量降低和混乱度增大都有促使反应自发进行的倾向
C . Br2+H2O⇌HBr+HBrO的平衡常数表达式为K=  D . 弱电解质的电离平衡常数和其对应盐的水解平衡常数互为倒数
D . 弱电解质的电离平衡常数和其对应盐的水解平衡常数互为倒数
 D . 弱电解质的电离平衡常数和其对应盐的水解平衡常数互为倒数
D . 弱电解质的电离平衡常数和其对应盐的水解平衡常数互为倒数
下列说法正确的是(NA表示阿伏加德罗常数)( )
A . 反应TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)ΔH>0能自发进行,其原因是ΔS>0
B . 对反应使用催化剂虽然不能改变转化率,但能够改变反应的焓变
C . 除去MgCl2溶液中的少量FeCl3 , 加入足量氢氧化钠,充分反应后,过滤
D . 1molCl2溶于水后,溶液中Cl2、HClO、ClO-、Cl-四种粒子总数为2NA
Cl2可用于生产漂白粉等化工产品。Cl2的制备方法有:
方法ⅠNaClO+2HCl(浓)=NaCl+Cl2↑+H2O;
方法Ⅱ4HCl(g)+O2(g)=2H2O(g)+2Cl2(g)ΔH=akJ·mol−1
上述两种方法涉及的反应在一定条件下均能自发进行。一定条件下,在密闭容器中利用方法Ⅱ制备Cl2 , 下列有关说法正确的是( )
A . 升高温度,可以提高HCl的平衡转化率
B . 提高  ,该反应的平衡常数增大
C . 若断开1molH-Cl键的同时有1molH-O键断开,则表明该反应达到平衡状态
D . 该反应的平衡常数表达式K=
,该反应的平衡常数增大
C . 若断开1molH-Cl键的同时有1molH-O键断开,则表明该反应达到平衡状态
D . 该反应的平衡常数表达式K= 
 ,该反应的平衡常数增大
C . 若断开1molH-Cl键的同时有1molH-O键断开,则表明该反应达到平衡状态
D . 该反应的平衡常数表达式K=
,该反应的平衡常数增大
C . 若断开1molH-Cl键的同时有1molH-O键断开,则表明该反应达到平衡状态
D . 该反应的平衡常数表达式K= 
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O 转变为H2。其过程如下:
mCeO2  (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+xCO2 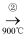 mCeO2+xH2+xCO
mCeO2+xH2+xCO
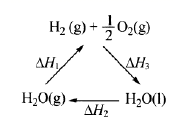
下列说法错误的是( )
A . 该过程中CeO2是催化剂
B . 该过程实现了太阳能向化学能的转化
C . 上图中∆H1 = ∆H2 + ∆H3
D . 从H2O(l)变成H2O(g)是熵增的过程
将一定量的硫化氢气体加入一密闭容器中,发生反应2H2S(g)=S2(g)+2H2(g),该反应的平衡常数的负对数(-lgK)随温度(T)的变化如图所示。下列说法错误的是( )
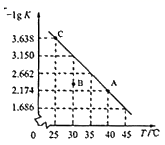
A . C点对应状态的平衡常数为10-3.638
B . 该反应的ΔH>0
C . A,C点的反应速率VA>Vc
D . 30℃时,B点对应状态v正>v逆
我国科学家提出用  替换可燃冰(
替换可燃冰( 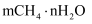 )中
)中  的设想,替换过程如图所示,下列说法正确的是( )
的设想,替换过程如图所示,下列说法正确的是( )
 替换可燃冰(
替换可燃冰( 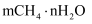 )中
)中  的设想,替换过程如图所示,下列说法正确的是( )
的设想,替换过程如图所示,下列说法正确的是( ) 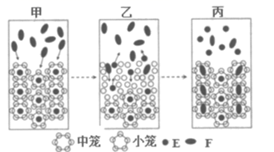
A . E代表  ,F代表
,F代表  B . 乙到丙的过程熵变大于零
C . 甲到乙的过程中释放能量
D . 笼状结构中水分子间主要靠氢键“结合”
B . 乙到丙的过程熵变大于零
C . 甲到乙的过程中释放能量
D . 笼状结构中水分子间主要靠氢键“结合”
 ,F代表
,F代表  B . 乙到丙的过程熵变大于零
C . 甲到乙的过程中释放能量
D . 笼状结构中水分子间主要靠氢键“结合”
B . 乙到丙的过程熵变大于零
C . 甲到乙的过程中释放能量
D . 笼状结构中水分子间主要靠氢键“结合”
下列说法错误的是( )
A . NH4NO3溶于水吸热,说明其溶于水不是自发过程
B . 水凝结成冰的过程中,体系的混乱度变化△S<0
C . 某化学反应自发进行的方向,与反应的△H和△S都有关
D . 发生离子反应的条件之一是生成气体,此过程是一个△S>0的过程
下列说法错误的是( )
A . 1 mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)]
B . 合成氨反应,加入合适的催化剂能降低反应的活化能,从而改变反应的焓变
C . CaCO3(s)  CaO(s)+CO2(g) ΔH>0 能否自发进行与温度有关
D . 常温下,反应C(s) +CO2(g) =2CO(g)不能自发进行,则该反应的ΔH>0
CaO(s)+CO2(g) ΔH>0 能否自发进行与温度有关
D . 常温下,反应C(s) +CO2(g) =2CO(g)不能自发进行,则该反应的ΔH>0
 CaO(s)+CO2(g) ΔH>0 能否自发进行与温度有关
D . 常温下,反应C(s) +CO2(g) =2CO(g)不能自发进行,则该反应的ΔH>0
CaO(s)+CO2(g) ΔH>0 能否自发进行与温度有关
D . 常温下,反应C(s) +CO2(g) =2CO(g)不能自发进行,则该反应的ΔH>0
相同温度和压强下,关于物质熵的大小比较,合理的是( )
A . 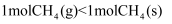 B .
B . 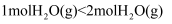 C .
C . 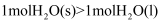 D . 1mol干冰
D . 1mol干冰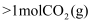
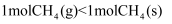 B .
B . 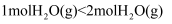 C .
C . 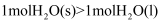 D . 1mol干冰
D . 1mol干冰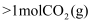
下列说法错误的是( )
A . 反应(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)的熵值增加
B . 同一种物质气态时熵值最大,液态时次之,固态时熵值最小
C . NH4NO3溶于水吸热,所以其溶解于水不是自发过程
D . 由于合成氨反应ΔH<0,ΔS<0,所以该反应低温下能自发进行
在体积均为1.0 L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2 , 在不同温度下反应CO2(g)+C(s) 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )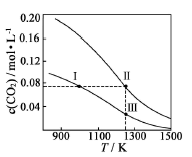
A . 反应CO2(g)+C(s) 2CO(g)△S>0、△H<0
B . 体系的总压强p总:P总(状态Ⅱ)>2P总(状态Ⅰ)
C . 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D . 逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ)
2CO(g)△S>0、△H<0
B . 体系的总压强p总:P总(状态Ⅱ)>2P总(状态Ⅰ)
C . 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D . 逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ)
 2CO(g)△S>0、△H<0
B . 体系的总压强p总:P总(状态Ⅱ)>2P总(状态Ⅰ)
C . 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D . 逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ)
2CO(g)△S>0、△H<0
B . 体系的总压强p总:P总(状态Ⅱ)>2P总(状态Ⅰ)
C . 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D . 逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ)
最近更新
- 下图是“世界主要石油运输路线图”,读图完成问题。【小题1】目前世界上石油储量最大、产量最高,输出量最多的地区是( )A
- 在热气球下方开口处燃烧液化气,使热气球内部气体温度升高,热气球开始离地,徐徐升空。分析这一过程,下列表述正确的是
- 某英文杂志正在举办以Fancy yourself as aninterviewer为主题的征文活动,请你以“A Famo
- (4分)摆长分别为的四个单摆如图所示,且>=>,先让它们静止不动,之后使c开始摆动,设c球质量比其他摆球质量大很多,当其
- 读写综合;根据信息卡回答问题. Personal Data Name:David
- 在促进政府解决物价、住房、医疗、教育和就业等民生问题上,人大代表应该 A.行使提案权,依法提出有关问题的议案 B.
- 未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是( ) ①天然
- 大年三十,中共中央政治局常委、国务院总理温家宝在辽宁农村考察时指出,我国新型合作医疗制度要本着自愿参加、多方筹资、因地制
- 阅读下面的文言文,完成后面题。 赵韩王普①为相。太祖即位之初,数出微行,或过功臣之家,不可测。一日大雪,向夜,叩赵普门。
- 函数f(x)=x3+ax-2在区间(1,+∞)内是增函数,则实数a的取值范围是()A.[3,+∞)
- 著名学者胡绳说:“近代中国在20世纪初处于一个社会大变革时期,中国民主主义革命由旧民主主义革命向新民主主义革命的转折,这
- 如图,已知二次函数y=x2+bx+c的图像的对称轴为过点(1,0)且与y轴平行的直线,点A、B均在图像上,且直线AB与x
- 阅读下面的文字,完成后面题宋词中的帘,品种繁多,状态各异,就前者言,有珠帘、绣帘、画帘、翠帘等等;就后者言,有卷帘、开帘
- 如图所示,水平桌面上斜放着一个平面镜,桌面上有一个小球向右滚去。要使平面镜中小球的像沿竖直方向下落,则镜面与桌面间的夹
- 判断题,正确的填“T”,错误的填“F”。 ( )1.地球的自转造成了四季交替
- 某男性与一正常女性婚配, 生育了一个白化病兼色盲的儿子。右图为此男性的一个精原细胞示意图(白化病基因a、色盲基因b)。这
- 老鼠对人有害,人们可以将其灭绝。 ( )
- 一个圆锥的底面半径为3㎝,它的侧面积为15π㎝2,那么这个圆锥的高线长为----( ▲ )A.4㎝ B.5㎝
- 问题解决——测量电阻: 小雨想要知道未知电阻Rx的阻值,现有—个电压恒定的电源(电压值未知)、—个单刀双掷开关、一个量程
- 古语云:“贪如火,不扑则燎原;欲如水,不遏则滔天。”从哲学上看,这警示我们 A .要注意量的积累,防微杜渐 B.要抓住时



