有效碰撞理论 知识点题库
①化学反应的实质是活化分子有合适取向时的有效碰撞
②普通分子间的碰撞有时也能发生化学反应
③活化分子比普通分子具有较高的能量
④化学反应的实质是原子的重新组合
⑤化学反应的实质是旧化学键的断裂和新化学键的形成过程
⑥活化分子间的碰撞一定能发生化学反应.
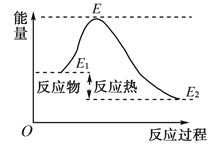
B . 活化分子具有比普通分子更高的能量
C . 反应物的分子的每次碰撞都能发生化学反应
D . 反应物分子间的有效碰撞是发生化学反应的充要条件
B . 活化分子具有比普通分子更高的能量
C . 反应物的分子的每次碰撞都能发生化学反应
D . 反应物分子间的有效碰撞是发生化学反应的充要条件
①活化分子间的碰撞一定能发生化学反应
②普通分子有时也能发生有效碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应实质是活化分子有合适取向时的有效碰撞
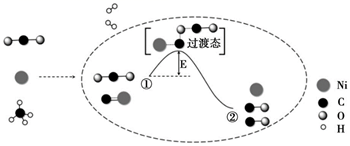
下列说法错误的是( )
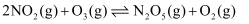 ,该反应一定条件下可自发进行。若反应在恒容密闭容器中进行,下列由该反应作出的判断(有关图像)错误的是( )
,该反应一定条件下可自发进行。若反应在恒容密闭容器中进行,下列由该反应作出的判断(有关图像)错误的是( )
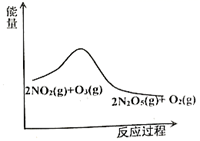 B .
B . 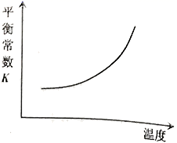 C .
C . 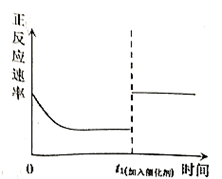 D .
D . 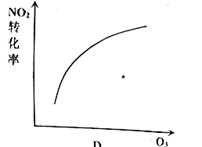
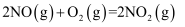 分两步进行:Ⅰ.
分两步进行:Ⅰ.  ,Ⅱ.
,Ⅱ. 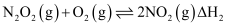 ,其反应过程能量变化如图1所示。在其它条件相同时,分别在
,其反应过程能量变化如图1所示。在其它条件相同时,分别在 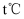 和
和 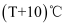 测得c(NO)随时间(t)的变化关系如图2 所示。下列说法错误的是( )
测得c(NO)随时间(t)的变化关系如图2 所示。下列说法错误的是( ) 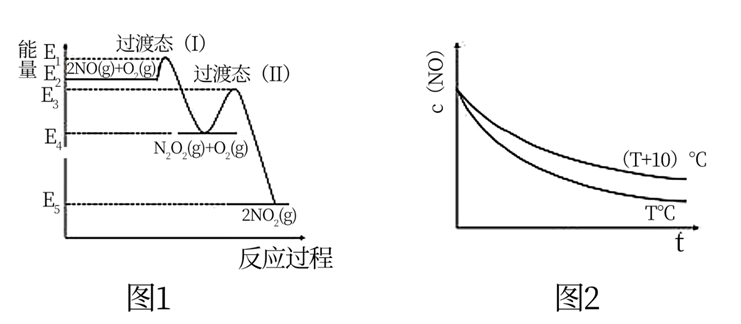
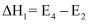 B . 反应Ⅱ是总反应的决速步骤
C . 升高温度总反应速率一定增大
D . 反应中只有部分分子发生有效碰撞
B . 反应Ⅱ是总反应的决速步骤
C . 升高温度总反应速率一定增大
D . 反应中只有部分分子发生有效碰撞
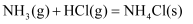 在室温下可自发进行,则该反应的
在室温下可自发进行,则该反应的 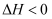 D . 反应
D . 反应  的熵变
的熵变 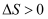
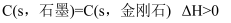 ,则石墨比金刚石稳定
C . 在一恒容密闭容器中发生反应
,则石墨比金刚石稳定
C . 在一恒容密闭容器中发生反应 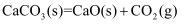 ,仅增加
,仅增加 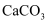 的质量,反应速率加快
D . 对于反应
的质量,反应速率加快
D . 对于反应 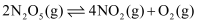 ,反应达到平衡后,保持其他条件不变,增大压强,化学平衡常数增大
,反应达到平衡后,保持其他条件不变,增大压强,化学平衡常数增大
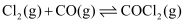 的速率方程
的速率方程  [
[ 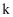 为速率常数,只受温度影响]该反应可认为经过以下反应历程:
为速率常数,只受温度影响]该反应可认为经过以下反应历程: 第一步: 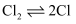 快速平衡
快速平衡
第二步: 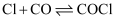 快速平衡
快速平衡
第三步: 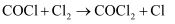 慢反应
慢反应
下列说法正确的是( )
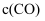 、
、  分别增大相同的倍数,对总反应速率的影响程度相同
C . 该总反应的速率主要取决于第三步反应
D . 压缩容器体积,会使体系中活化分子百分数增加
分别增大相同的倍数,对总反应速率的影响程度相同
C . 该总反应的速率主要取决于第三步反应
D . 压缩容器体积,会使体系中活化分子百分数增加
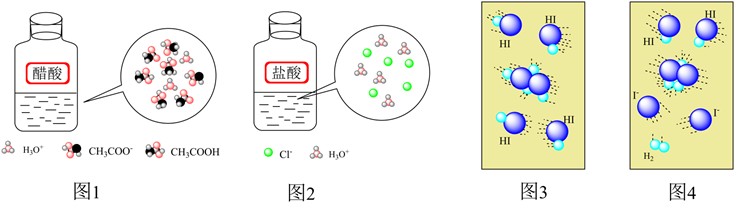
 在水中电离示意图
B . 图2为HCl在水中电离示意图
C . 图3为HI分解反应中分子碰撞时能量不足示意图
D . 图4为HI分解反应中分子发生有效碰撞时示意图
在水中电离示意图
B . 图2为HCl在水中电离示意图
C . 图3为HI分解反应中分子碰撞时能量不足示意图
D . 图4为HI分解反应中分子发生有效碰撞时示意图
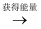 活化分子
活化分子  产物分子
D . 基元反应发生的先决条件是反应物的分子必须发生碰撞
产物分子
D . 基元反应发生的先决条件是反应物的分子必须发生碰撞
-
(1) 已知某反应体系中主要涉及如下反应:
Ⅰ.
 ;
;Ⅱ.
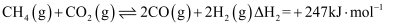 。
。①反应Ⅰ和反应Ⅱ中,在热力学上趋势更大的是(填“Ⅰ”或“Ⅱ”)。
②反应Ⅰ的一种溶剂化催化反应历程如图所示(其中TS表示过渡态)。
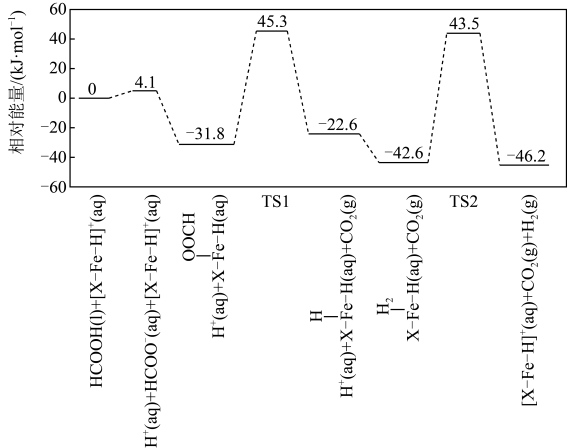
历程中生成(填“TS1”或“TS2”)的反应步骤为总反应的决速步,反应过程的催化剂为。
③反应Ⅱ的催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应而降低积碳量,设计如下反应:
Ⅲ.
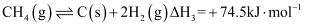 ;
;Ⅳ.
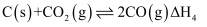 。
。反应Ⅳ的
 为。其他条件相同时,催化剂表面积碳量与温度的关系如图所示,
为。其他条件相同时,催化剂表面积碳量与温度的关系如图所示, 之后,温度升高积碳量减小的主要原因为。
之后,温度升高积碳量减小的主要原因为。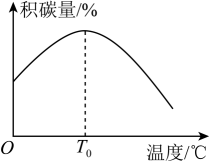
-
(2) 甲烷部分催化氧化剂制备乙炔是目前研究的热点之一、反应原理为:
 。
。①该反应在(填“较高”或“较低”)温度下能自发进行。
②一定温度下,将1 mol
 充入10 L的固定容积容器中发生上述反应,实验测得反应前容器内压强为
充入10 L的固定容积容器中发生上述反应,实验测得反应前容器内压强为 , 容器内各气体分压与时间的关系如图所示。
, 容器内各气体分压与时间的关系如图所示。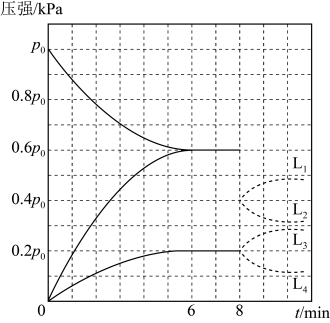
6~8 min时,
 的浓度为
的浓度为 , 反应的平衡常数
, 反应的平衡常数 ;若8 min时改变的条件是缩小容器容积到5 L,其中
;若8 min时改变的条件是缩小容器容积到5 L,其中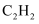 分压与时间关系可用图中曲线(填“
分压与时间关系可用图中曲线(填“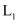 ”“
”“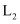 ”“
”“ ”或“
”或“ ”)表示。
”)表示。
- 某溶液中含有HCO、SO与CO、CH3COO-等4种阴离子。向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变
- 取一植物形态、大小、生长发育状况相同的四张叶片按下图进行实验,烧杯中的液体可以保证叶片所需的水与矿质元素的正常供应,气体
- 下列有关我国自然资源地区差异的叙述中,正确的是 A.在东部,北方的平原比南方多,但水热条件比南方差 B.西北地区的垂直地
- NA表示阿伏加德罗常数的值,下列叙述中正确的是A.1 L 1 mol·L-1醋酸溶液中离子总数为2NAB.标准状况下,2
- 已知角的终边经过点. (1)求的值; (2)求的值.
- (配方法)
- 下列句子标点符号的使用,正确的一句是 A、两个分厂的近200台设备、设施的迁出;100多台新进设备、设施的迁入安装,几乎
- 已知:(a﹣b)2=9;(a+b)2=25,则a2+b2=.
- (14分)如图所示,光滑水平面上放置质量均为M=2kg的甲、乙两辆小车,两车之间通过一感应开关相连(当滑块滑过感应开关时
- 下列实验现象的描述正确的是 A.氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾 B.铁丝在氯气中燃烧,产生棕褐色的
- 我国水旱灾害比较频繁的主要原因是 A.地势高低不同 B.夏季风进退
- 在我国的收入分配中,要兼顾效率与公平,唯有效率与公平统一的社会主义才是改革的基本方向。下列措施有利于实现效率与公平统一的
- 有人用“有心栽花花不开,无心插柳柳成荫”来形容洋务运动,这一运动没能挽救腐朽的清王朝,但在客观上为中国的近代化开辟了道
- 阅读下面两则材料,回答问题。(7分) 今年3月25日,在中国人的强烈反对声中,佳士得拍卖行仍将圆明园非法流失的兔首、鼠首
- —______ doyou go to the cinema?—On Sundayevening.A. How ofte
- 唐朝思想家刘禹锡提出天与人“交相胜,还相用”,这一观点 A.是正确的,表明人与自然的相互作用 B.是错误的,
- 三江源地区地处青藏高原腹地,是长江、黄河、澜沧江的发源地,长江水量的25%、黄河水量的49%、澜沧江水量的15%都来自这
- 为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液
- 修改下面的一个病句 尽管你的礼品多么微薄,但在农民心上,却象千斤重的砝码。
- 喷瓜有雄株、雌株和两性植株.G基因决定雄株.g基因决定两性植株。基因决定雌株。G对g、对g是显性。如:Gg是雄株,g是两



