活化分子 知识点题库
改变以下反应的条件,能提高反应物活化分子百分数的是①温度 ②浓度 ③压强 ④正催化剂( )
A . ①④
B . ②③
C . ①②
D . ③④
下列说法正确的是( )
A . 活化分子间的碰撞一定是有效碰撞
B . 活化分子具有的能量是活化能
C . 活化分子的总数越多,反应速率越快
D . 单位时间内有效碰撞次数越多,反应速率越快
下列说法正确的是( )
A . 热化学方程式中,如没有注明温度和压强,表示反应热是在标准状况下测得的数据
B . 升高温度和增加反应物的浓度,都使反应物活化分子数和活化分子百分数同时增加
C . 化学反应速率可通过实验测定,比如可以测量在一定温度和压强下释放出的气体的体积,或者可以用比色的方法测定溶液颜色的深浅进行换算
D . 物质发生化学变化不一定伴随着能量变化
一定条件下的可逆反应:2SO2(g)+O2(g)  2SO3(g),若改变下列条件,可提高反应物中的活化分子百分数的是( )
2SO3(g),若改变下列条件,可提高反应物中的活化分子百分数的是( )
 2SO3(g),若改变下列条件,可提高反应物中的活化分子百分数的是( )
2SO3(g),若改变下列条件,可提高反应物中的活化分子百分数的是( )
A . 升高温度
B . 降低温度
C . 增大压强
D . 增大反应物浓度
如图所示是25℃时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
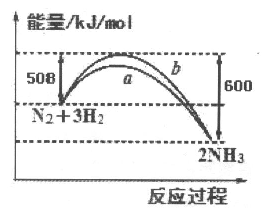
A . 该反应为放热反应
B . b曲线是表示加入了催化剂时的能量变化曲线
C . 加入催化剂,增加了反应的热效应
D . 反应开始通入1 mol N2和3 mol H2 , 反应后放出的热量一定为92kJ
升高温度能加快反应速率的主要原因是( )
A . 活化分子能量明显增加
B . 增加了活化分子的百分数
C . 降低了反应所需的能量
D . 改变了反应物的本身性质
改变下列一个条件,通过提高活化分子的百分率来改变反应速率的是( )
A . 增加固体反应物表面积
B . 加压
C . 加大反应物浓度
D . 加催化剂
甲醛(HCHO)是一种重要的化工产品,工业上可用甲醇脱氢法制备,相关反应方程式为:CH3OH(g)  HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
 HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
-
(1) 反应过程中需要向体系中通入空气,通过以下反应提供上述反应所需要的热量:H2(g)+
 O2(g)=H2O(g) △H=-bkJ/mol
O2(g)=H2O(g) △H=-bkJ/mol 要使反应温度维持在650℃,则进料时,甲醇和空气的体积比应为(已知空气中氧气的体积分数为20%,b>a)。
-
(2) Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
历程i:CH30H→・H+・CH2OH(・H叫做氢自由基,实际上就是H原子,有很高的反应活性,
“・”代表有一个单电子可以参与配对成键)
历程ii:・CH2OH→・H+HCHO
历程iii:・CH2OH→3•H+CO
历程iv:自由基发生碰撞形成新化学键而湮灭
如图1所示为在体积为2L的恒容容器中,投入1molCH3OH(g),在碳酸钠催化剂作用下开始反应,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)与温度的关系(副反应仅考虑CH3OH
 CO+2H2):
CO+2H2):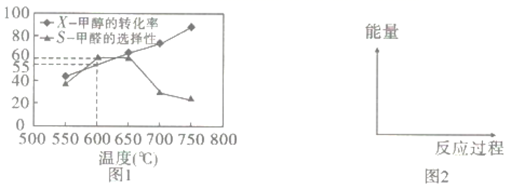
①请在图2所给坐标中,画出历程iv的反应过程一能量变化示意图。
②下列说法合理的是。
a.升高温度,甲醇转化率提高,平衡常数变大
b.当体系气体密度保持不变时,达到平衡状态
c.及时分离产品有利于提高甲醇生成甲醛的转化率
③600℃时,前20min甲醇的平均反应速率为,此时生成甲醛的反应的Qp=(Qp的表达式与平衡常数Kp相同,p为物质的分压,分压=总压×物质的量分数,体系初始压强为P0)
④650℃以后,甲醛的选择性降低,而甲醇的转化率升高的可能原因是。
-
(3) 氧化剂可处理甲醛污染,结合以下图像分析夏季(水温约20℃)应急处理甲醛污染的水源最好应选择的试剂为。

最近,中国科学院大连化物所“CO2催化转化为CO的研究”获得新进展。如图是使用不同催化剂(NiPc和CoPc)时转化过程中的能量变化,下列说法不合理的是( )
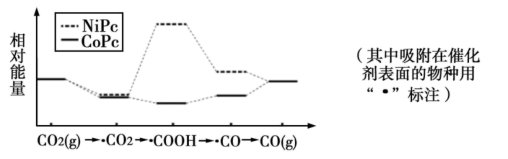
A . •CO2经还原反应得到•COOH
B . 该研究成果将有利于缓解温室效应,并解决能源转化问题
C . 相同基团的物种分别吸附在NiPc和CoPc表面,其能量可能不同
D . 催化剂可以改变CO2转化为CO反应的焓变
工业上研究高效处理煤燃烧释放出来的SO2 , 有利于减小环境污染。在T℃时,利用CO处理SO2的反应为:2CO(g)+SO2(g)  2CO2(g)+S(l) △H=akJ/mol;
2CO2(g)+S(l) △H=akJ/mol;
 2CO2(g)+S(l) △H=akJ/mol;
2CO2(g)+S(l) △H=akJ/mol;
-
(1) 已知T℃时:C(s)+
 O2(g)=CO(g) △H1=-110.5kJ/mol
O2(g)=CO(g) △H1=-110.5kJ/mol S(l)+O2(g)=SO2(g) △H2=-290.0kJ/mol
C(s)+O2(g)=CO2(g) △H3=-390.0kJ/mol
则T℃时,a=。
-
(2) 在T℃下,将1.4molCO和1molSO2通入2L恒容容器中发生上述反应,反应体系气体总物质的量随时间变化如图;在0~10min,反应的平均速率v(CO)=,SO2的平衡转化率
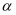 (SO2)=%;在T℃时该反应的平衡常数Kc=L/mol。
(SO2)=%;在T℃时该反应的平衡常数Kc=L/mol。 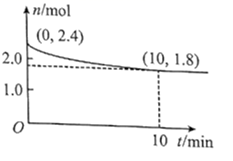
-
(3) 实验测得:v正=v(CO)消耗=k正c(CO)•c(SO2),v逆=v(CO2)消耗=k逆
 ,k正、k逆为只受温度影响的速率常数。若将(2)中容器内的温度升高(假设各物质的状态不发生变化),
,k正、k逆为只受温度影响的速率常数。若将(2)中容器内的温度升高(假设各物质的状态不发生变化),  的值将(填“增大”、“减小”或“不变”)。
的值将(填“增大”、“减小”或“不变”)。
-
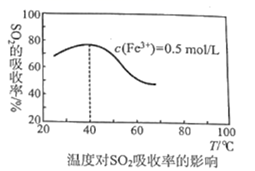
(4) 某科研团队研究用Fe2(SO4)3(aq)处理SO2:Fe3+溶液吸收SO2发生的离子反应方程式为;其他外界条件不变下,在相同时间内温度对SO2吸收率的影响结果如图,在40℃前,SO2的吸收率随温度变化的可能原因是;在40℃后,SO2的吸收率发生的变化是温度升高该反应逆向移动的结果,导致反应逆向移动的原因:一是该反应为放热反应,二是。
氮及其化合物的转化过程如图所示。下列分析合理的是( )
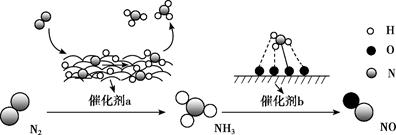
A . 催化剂a表面发生了极性共价键的断裂和形成
B . N2与H2反应生成NH3的原子利用率为100%
C . 在催化剂b表面形成氮氧键时,不涉及电子转移
D . 催化剂a、b能提高反应的平衡转化率
在恒容条件下,能使NO2(g)+CO(g)  CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:( )
CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:( )
 CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:( )
CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增大的措施是:( )
A . 增大NO2或CO的浓度
B . 减小CO2或NO的浓度
C . 通入Ne使气体的压强增大
D . 升高反应的温度
碰撞理论是一种较直观的反应速率理论,下列有关碰撞理论叙述正确的是( )
A . 分子发生碰撞就一定发生反应
B . 发生有效碰撞的分子具有最高的能量
C . 有效碰撞是活化分子在一定方向上的碰撞
D . 活化分子的平均能量称之活化能
有气体参加的反应中,能使反应物中活化分子数和活化分子百分数都增大的方法是( )
①增大反应物浓度 ②增大压强 ③升高温度 ④加入催化剂
A . ①②③
B . ②③④
C . ①③④
D . ③④
在气体反应中,使反应物中活化分子数增多,且活化分子百分数增大的方法是( )
①增大反应物浓度②升高温度③增大压强④移去生成物⑤加入合适的催化剂
A . ①③⑤
B . ②⑤
C . ②③⑤
D . ①③④
下列说法正确的是( )
A . 对于有气体参与的反应,增大压强,活化分子数增多,化学反应速率增大
B . 对放热反应而言,升高温度,活化分子百分数减少,反应速率减小
C . 活化分子间发生的碰撞为有效碰撞
D . 使用催化剂,活化分子百分数增多,化学反应速率增大
一定温度下, 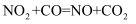 ,反应过程对应的能量变化如图,下列说法正确的是( )
,反应过程对应的能量变化如图,下列说法正确的是( )
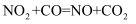 ,反应过程对应的能量变化如图,下列说法正确的是( )
,反应过程对应的能量变化如图,下列说法正确的是( ) 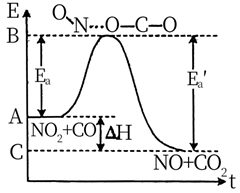
A . 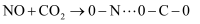 的
的 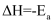 B .
B .  是正反应的活化能,是活化络合物的平均能量与反应物的平均能量的差值
C . 温度升高,活化分子数增多,活化分子百分数不变,有效碰撞次数增多,反应速率增大
D . 加入催化剂可以减小
是正反应的活化能,是活化络合物的平均能量与反应物的平均能量的差值
C . 温度升高,活化分子数增多,活化分子百分数不变,有效碰撞次数增多,反应速率增大
D . 加入催化剂可以减小  ,反应速率加快,
,反应速率加快, 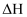 减小
减小
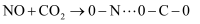 的
的 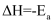 B .
B .  是正反应的活化能,是活化络合物的平均能量与反应物的平均能量的差值
C . 温度升高,活化分子数增多,活化分子百分数不变,有效碰撞次数增多,反应速率增大
D . 加入催化剂可以减小
是正反应的活化能,是活化络合物的平均能量与反应物的平均能量的差值
C . 温度升高,活化分子数增多,活化分子百分数不变,有效碰撞次数增多,反应速率增大
D . 加入催化剂可以减小  ,反应速率加快,
,反应速率加快, 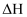 减小
减小
下列关于化学反应速率及化学平衡的说法,正确的是 ( )
A . 升高温度能增大单位体积内活化分子数目,加快反应速率
B . 增大反应物浓度,可增大活化分子的百分数,因而反应速率加快
C . 化学反应条件改变,已处于化学平衡的可逆反应一定发生平衡移动
D . 催化剂可以提高化学反应的选择性,进而提高反应物的平衡转化率
在化学反应中,其他条件不同,仅改变下列其中一个条件,能提高活化分子百分数的是( )
A . 增大反应物浓度
B . 增大气体反应压强
C . 加入高效催化剂
D . 增大固气反应接触面积
“人工固氮”对农业生产至关重要。在常温、常压和光照条件下,N2在某种催化剂表面与水反应的热化学方程式为2N2(g) + 6H2O(l) = 4NH3(g) + 3O2(g) ∆H,反应过程中的能量变化如图所示。下列有关说法正确的是( )
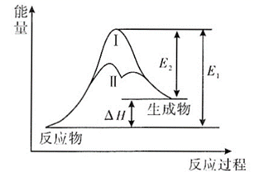
A . 该反应的焓变∆H<0
B . 升高温度,活化分子数目增多
C . 反应Ⅰ的活化能大,活化分子数目多
D . 反应Ⅱ的转化率比反应Ⅰ的转化率高
最近更新
- 某班一次数学测试成绩的茎叶图(茎上数代表十位,叶上数代表个位)如图1所示. (1)以10为组距,在图2给定的坐标系中画出
- The secretaryhas a lot of things to ______ in the office si
- 15.阅读下面的文字,完成小题。杂交水稻之父1982年的一个秋日,马尼拉洛斯巴洛斯镇国际水稻研究所的学术报告厅里,正在举
- I look on it as a good opportunityto _______ fresh skills a
- 欧盟国家人们可以统一使用的货币是 A. 欧元 B. 英镑 C. 美元 D. 法郎
- 下列营养物质中,不能为人体提供能量,但对维持正常生命活动却很重要的一组是() A.蛋白质、无机盐、水
- 2007年6月26日,世界最长的跨海大桥________正式贯通。此桥北起嘉兴市海盐,跨越杭州湾海域,止于宁波市慈溪,全
- 二氧化碳已逐渐成为一种备受关注的物质。 (1)下图所示的三个实验中,实验1说明二氧化碳具有的性质是 ;实
- 一物体在水平面内沿半径R=20 cm的圆形轨道做匀速圆周运动,线速度v=0.2 m/s,那么,它的向心加速度为_____
- 某人在静水中游泳,速度为4千米/时,他在水流速度为4千米/时的河中游泳.(1)若他垂直游向河对岸,则他实际沿什么方向前进
- 读地球上的五带图判断,吉林省位于五带中的 A.热带 B.北温带
- 一个阻值为2 Ω的线圈在匀强磁场中转动,产生的交变电动势为e=10sin20πtV,当该线圈与一阻值为8 Ω的电阻组成闭
- 如果你用手掌托在耳廓后边,就会感到传来的声音变得更大了,这说明耳廓的功能是 A.收集声波 B.传递声波
- 一元二次方程的根是( ) A.x1=1,x2=6 B.x1=2,x2=3 C.x1=1,x2=-6
- 图一是苏维埃政府发给农民的耕田证书,图二是晋察冀根据地农民拥护当时中共的土地政策而举行游行的一幅照片,图三是解放区开展土
- 基因型为AaXBXb的雌果蝇与基因型为AaXBY的雄果蝇交配后,后代将产生几种基因型 A.6
- 能正确表示下列反应的化学方程式是() A.黄铁矿煅烧:2FeS2+5O22FeO+4SO2 B.石英与石灰石共熔:SiO
- 关于半导体,以下说法错误的是: A.计算机的集成电路是用半导体材料做成的。B
- 下列关于回归直线的命题,正确的个数是() ①回归直线通过散点图的中心(x,y) ②回归直线必经过散点图的多个点 ③
- 一年一度的高考来临时,保健品市场常出现很多脑保健品,有些产品是通过给大脑持续补充磷脂酰胆碱,有效合成记忆传递因子——乙酰



