化学反应速率和化学平衡 知识点题库
 B . 图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
B . 图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小 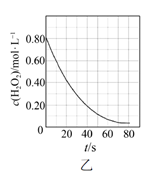 C . 图丙是室温下用0.1000 mol·L−1NaOH溶液滴定20.00 mL 0.1000 mol·L−1某一元酸HX的滴定曲线,说明HX是一元强酸
C . 图丙是室温下用0.1000 mol·L−1NaOH溶液滴定20.00 mL 0.1000 mol·L−1某一元酸HX的滴定曲线,说明HX是一元强酸 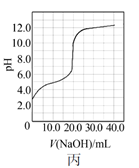 D . 图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO42−)的关系曲线,说明溶液中c(SO42−)越大c(Ba2+)越小
D . 图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO42−)的关系曲线,说明溶液中c(SO42−)越大c(Ba2+)越小 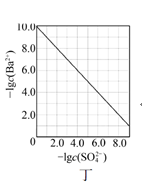
 4NO2(g)+O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中,正确的是( )
4NO2(g)+O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中,正确的是( ) 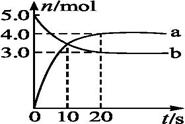
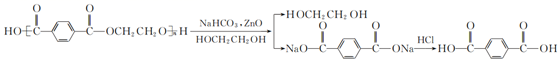
实验步骤如下:
步骤1:在题图1所示装置的四颈烧瓶内依次加入洗净的矿泉水瓶碎片、氧化锌、碳酸氢钠和乙二醇,缓慢搅拌,油浴加热至180 ℃,反应0.5 h。
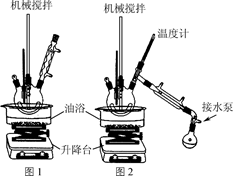
步骤2:降下油浴,冷却至160 ℃,将搅拌回流装置改为图2所示的搅拌蒸馏装置,水泵减压,油浴加热蒸馏。
步骤3:蒸馏完毕,向四颈烧瓶内加入沸水,搅拌。维持温度在60 ℃左右,抽滤。
步骤4:将滤液转移至烧杯中加热煮沸后,趁热边搅拌边加入盐酸酸化至pH为1~2。用砂芯漏斗抽滤,洗涤滤饼数次直至洗涤滤液pH=6,将滤饼摊开置于微波炉中微波干燥。
请回答下列问题:
-
(1) 步骤1中将矿泉水瓶剪成碎片的目的是。
-
(2) 步骤2中减压蒸馏的目的是,蒸馏出的物质是。
-
(3) 抽滤结束后停止抽滤正确的操作方法是。若滤液有色,可采取的措施是。
-
(4) 该实验中,不采用水浴加热的原因是。
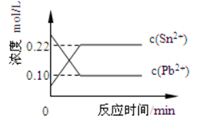
下列判断正确的是( )
-
(1) 已知:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2=-49.0kJ•mol-1
CH3OH(g)+H2O(g) ΔH2=-49.0kJ•mol-1 CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH3=-41.1kJ•mol-1
CO2(g)+H2(g) ΔH3=-41.1kJ•mol-1H2还原 CO反应合成甲醇的热化学方程式为:CO(g)+2H2(g)
 CH3OH(g) ΔH1 , 则ΔH1=kJ•mol-1 , 该反应自发进行的条件为
CH3OH(g) ΔH1 , 则ΔH1=kJ•mol-1 , 该反应自发进行的条件为A.高温
B.低温
C.任何温度条件下
-
(2) 恒温恒压下,在容积可变的密闭容器中加入 1molCO和2.2mol H2 , 发生反应CO(g)+2H2(g)
 CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1P2 , 判断的理由是。
CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1P2 , 判断的理由是。 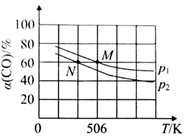
-
(3) 若反应 CO(g)+2H2(g)
 CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示: 时间/min
0
5
10
15
H2
4
2
CO
2
1
CH3OH(g)
0
0.7
①下列各项能作为判断该反应达到平衡标志的是(填字母);
A.容器内压强保持不变
B.2v正(H2)=v逆(CH3OH)
C.混合气体的相对分子质量保持不变
D.混合气体的密度保持不变
②若起始压强为P0 kPa,则在该温度下反应的平衡常数Kp=(kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③反应速率若用单位时间内分压的变化表示,则10min内H2的反应速率v(H2)=kPa•min-1。
-
(1) 将amol NO和bmol O2发生反应,要使反应达到平衡后反应物的物质的量和生成物的物质的量相等,则
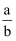 的取值范围是。
的取值范围是。 a.0<
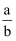 <
< 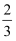 b.
b. 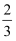 <
< 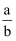 <1 c.
<1 c. 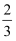 <
< 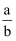 <4 d.1<
<4 d.1< 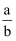 <
< 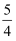
-
(2) 某温度时,按物质的量比2:1充入NO和O2开始反应,n(NO)随时间的变化如表:
时间(s)
0
1
2
3
4
5
n(NO)(mol)
0.020
0.010
0.008
0.007
0.007
0.007
写出该反应的平衡常数表达式:K=。0~1s内以O2浓度变化表示的正反应速率0~5s内以NO浓度变化表示的正反应速率(选填“小于”、“大于”、“等于”、“无法确定”)。
-
(3) 能说明该反应已达到平衡状态的是。
a.气体颜色不再变化 b.容器内压强保持不变 c.v逆(NO)=2v正(O2) d.容器内密度保持不变
-
(4) 已知:K300℃>K350℃ , 能使该反应的反应速率增大且平衡向正反应方向移动的是。
a.及时分离出NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
 PCl3(g)+Cl2(g),反应达到平衡时,PCl5在混合气体中的体积分数为m%,若在相同的温度和相同的容器中,起始时加入2molPCl5 , 反应达到平衡时,PCl5在混合气体中的体积分数为n%,则m和n的关系正确的是( )
PCl3(g)+Cl2(g),反应达到平衡时,PCl5在混合气体中的体积分数为m%,若在相同的温度和相同的容器中,起始时加入2molPCl5 , 反应达到平衡时,PCl5在混合气体中的体积分数为n%,则m和n的关系正确的是( )
 2C + 4D 反应中,表示反应速率最快的是( )
2C + 4D 反应中,表示反应速率最快的是( )
 2C(g)+D(g)已达平衡状态的是( )
2C(g)+D(g)已达平衡状态的是( )
 2Z(g),达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
2Z(g),达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
 2NH3 (g) △H<0,下列说法正确的是( )
2NH3 (g) △H<0,下列说法正确的是( )
| 编号 | 实验目的 | 实验过程 |
| A | | |
| B | 探究温度对化学平衡移动的影响 | 将少量95%的乙醇和氯化钻晶体 |
| C | 验证淀粉水解产物有无还原性 | 淀粉与稀硫酸共热,再加人新制的氢氧化铜悬浊液并加热,观察实验现象 |
| D | 探充浓度对反应速率的影响 | 向2支盛有5mL不同浓度 |
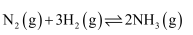
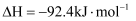 ,他因此获得了1918年诺贝尔化学奖.
,他因此获得了1918年诺贝尔化学奖. 在密闭容器中,使2mol  和6 mol
和6 mol  混合发生下列反应:
混合发生下列反应:
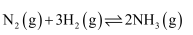 (正反应为放热反应)
(正反应为放热反应)
-
(1)
 和
和  的转化率之比为.
的转化率之比为.
-
(2) 当达到平衡时,充入氩气,并保持体积不变,平衡将(填“正向”“逆向”或“不”)移动.
-
(3) 恒温下,压缩容器体积,混合气体的平均相对分子质量,密度.(填“变大”“变小”或“不变”)
-
(4) 若容器恒容、绝热,降温使容器内温度迅速下降至原来的1/2,平衡将(填“向左程动”“向右移动”或“不移动”),达到新平衡后,容器内温度(填“大于”“小于”或“等于”)原来的1/2.
-
(1) Ⅰ.决定化学反应速率的主要因素是_______。A . 浓度 B . 温度 C . 催化剂 D . 反应物的性质
-
(2)
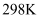 时,
时,  与
与  反应的能量变化曲线如图。下列叙述正确的是_______。
反应的能量变化曲线如图。下列叙述正确的是_______。 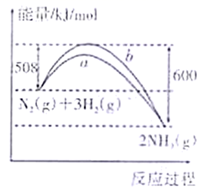 A . 该反应的
A . 该反应的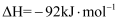 B . 加入催化剂,能提高
B . 加入催化剂,能提高  的转化率
C . 形成
的转化率
C . 形成 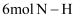 键,吸收
键,吸收 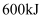 能量
D .
能量
D .  曲线是加入催化剂时的能量变化曲线
曲线是加入催化剂时的能量变化曲线
-
(3) 向纯水中加入下列物质,能抑制水的电离,并使溶液中的
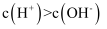 的是_______。
A .
的是_______。
A .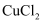 B .
B . 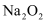 C .
C .  D .
D . 
-
(4) 下图装置中,能形成原电池的是_______。A .
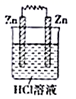 B .
B . 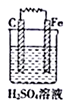 C .
C . 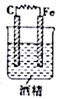 D .
D . 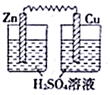
-
(5) 在一密闭容器中,反应
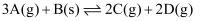
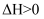 达到平衡后,改变以下条件,下列说法正确的是_______。
A . 增大压强,正、逆反应速率同等程度增大,平衡不移动 B . 增加
达到平衡后,改变以下条件,下列说法正确的是_______。
A . 增大压强,正、逆反应速率同等程度增大,平衡不移动 B . 增加 的用量,正、逆反应速率不变,平衡不移动
C . 增加
的用量,正、逆反应速率不变,平衡不移动
C . 增加  的浓度,平衡向正方向移动,平衡常数增大
D . 升高温度,正反应速率增大,逆反应速率减小,平衡向正方向移动
的浓度,平衡向正方向移动,平衡常数增大
D . 升高温度,正反应速率增大,逆反应速率减小,平衡向正方向移动
-
(6) Ⅱ.
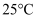 时,用
时,用 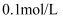 盐酸滴定
盐酸滴定 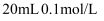 氨水的图像如图所示。回答以下问题。
氨水的图像如图所示。回答以下问题。 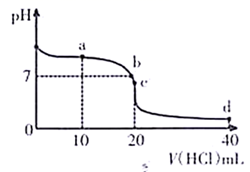
在图像的
 、
、  、
、  、
、  四点中,表示盐酸与氨水恰好反应的是点,此时溶液呈(填“酸”、“碱”或“中”)性。
四点中,表示盐酸与氨水恰好反应的是点,此时溶液呈(填“酸”、“碱”或“中”)性。 -
(7)
 点时,溶液中微粒浓度关系:
点时,溶液中微粒浓度关系: 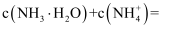 (用离子浓度符号填空)。
(用离子浓度符号填空)。
-
(8)
 点时,溶液中
点时,溶液中 
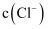 (填“
(填“ 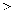 ”、“
”、“  ”或“
”或“ 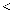 ”),理由是。
”),理由是。
-
(9)
 点时,溶液中粒子浓度关系:
点时,溶液中粒子浓度关系:  (用离子浓度符号填空)。
(用离子浓度符号填空)。
-
(10)
 、
、  、
、  、
、  点均成立的离子浓度等式为。
点均成立的离子浓度等式为。
 , 达到平衡后,缩小容器的体积可使体系颜色变深
B . 向
, 达到平衡后,缩小容器的体积可使体系颜色变深
B . 向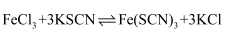 平衡体系中加入少量
平衡体系中加入少量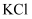 固体,平衡逆向移动,溶液红色颜色变浅
C . 重铬酸钾溶液中滴加
固体,平衡逆向移动,溶液红色颜色变浅
C . 重铬酸钾溶液中滴加 溶液,溶液由橙色变黄色【重铬酸钾溶液中存在:
溶液,溶液由橙色变黄色【重铬酸钾溶液中存在: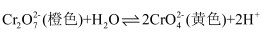 】
D .
】
D . 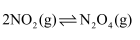 平衡体系,压缩容器的体积,平衡正向移动,最终体系颜色变浅
平衡体系,压缩容器的体积,平衡正向移动,最终体系颜色变浅
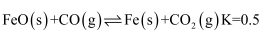 , 一段时间后达到平衡。下列说法不正确的是( )
, 一段时间后达到平衡。下列说法不正确的是( )
 减小,则
减小,则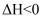 B . 加入一定量CO(g),平衡正向移动,
B . 加入一定量CO(g),平衡正向移动, 的体积分数增大
C . 改变浓度使
的体积分数增大
C . 改变浓度使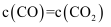 , 平衡将逆向移动
D . 若减小容器体积,平衡不移动
, 平衡将逆向移动
D . 若减小容器体积,平衡不移动
-
(1) 已知H2(g)和CH3OH(g)的燃烧热分别是285.8kJ·mol-1和763.9kJ·mol-1 , H2O(1)的汽化热是40.8kJ·mol-1 , 则反应CO2(g)+3H2(g)→CH3OH(g)+H2O(g)的ΔH=。该反应在(填“高温”“低温”或“任何温度”)下可自发进行。
-
(2) CO2催化加氢制CH3OH的一种反应机理历程如下图所示(吸附在催化剂表面的物质用*标注,如CO2*表示CO2吸附在催化剂表面)
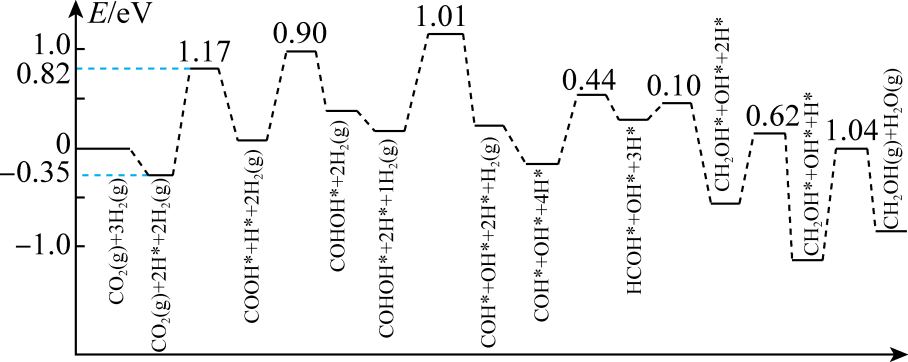
该反应历程中决速步反应的化学方程式为。
-
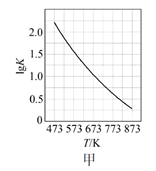
(3) 已知化学反应速率方程k正、k逆是正逆反应v正=k正·c(CO2)·c3(H2),v逆=k逆·c(CH3OH)·c(H2O)的速率常数,只受温度影响。如图表示速率常数的对数lgk与温度的倒数
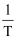 之间的关系,k正、k逆对应的曲线分别是、。
之间的关系,k正、k逆对应的曲线分别是、。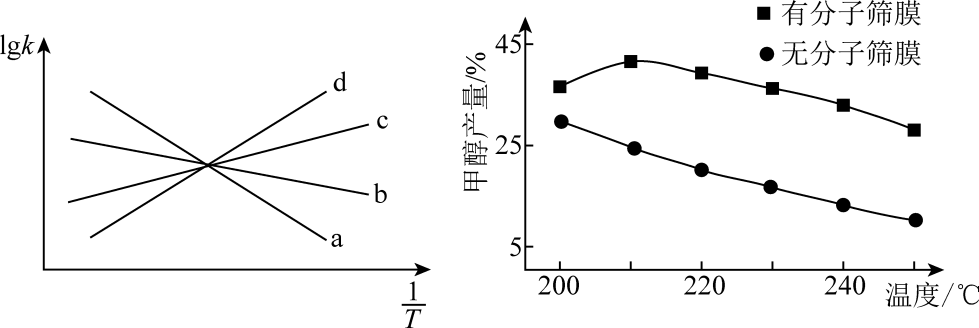
-
(4) CO2和H2起始物质的量之比为1:3时,该反应在有、无分子筛膜时甲醇的平衡产率随温度的变化如图所示(分子筛膜能选择性分离出H2O)。有分子筛膜时,温度为210℃时甲醇平衡产率最高的原因是。
-
(5) 一定条件下,向2L恒容密闭容器中充入2 molCO2和6molH2 , 发生反应CO2(g)+3H2(g) → CH3OH(g)+H2O(g)。已知容器内起始压强为320kPa,反应达平衡时容器内压强为200kPa,平衡时CH3OH(g)的分压为kPa,该温度下反应的标准平衡常数Kθ=。(该反应标准平衡常数的表达式为Kθ=
 , 其中p为分压,分压=总压×物质的量分数,pθ=100kPa)
, 其中p为分压,分压=总压×物质的量分数,pθ=100kPa)
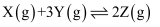 , 一定条件下,将
, 一定条件下,将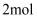 X和
X和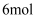
 通入
通入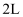 的恒容密闭容器中,反应到
的恒容密闭容器中,反应到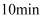 时,测得Y的物质的量为
时,测得Y的物质的量为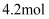 , 当反应达到平衡时测得放出
, 当反应达到平衡时测得放出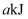 热量,下列说法正确的是( )
热量,下列说法正确的是( )
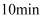 时,Y的反应速率为
时,Y的反应速率为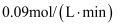 B . 前
B . 前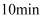 内,X的转化率为
内,X的转化率为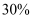 C . 当有
C . 当有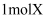 参与反应时,放出的热量为
参与反应时,放出的热量为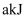 D . 达到化学平衡状态时,
D . 达到化学平衡状态时,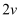 正
正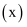

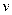 逆
逆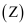 , 且Z的浓度不再变化
, 且Z的浓度不再变化
- 读中心点为南极的示意图。完成下面试题。若阴影部分表示黑夜,甲地时间为 A.8时 B.9时 C.15时 D.16时
- 2.下列各句中,没有语病的一句是( ) A.那时候的青年学生,对梁启超先生怀着无限的景仰,原因是因为他的学术文
- 下列有关实验或做法合理有效的是 A.配制FeSO4溶液可加Zn 粉防止溶液氧化变质 B.0.01mol/LKMnO4和0
- We __________3,000 English words by the end of last year. A.
- 一 对表现正常的夫妇,他们的基因型是Bb.预计他们生育一个白化病的孩子基因是 A.BB B.Bb C.B
- 下列叙述中,属于生物因素对生物影响的是
- 2009年是孔子诞辰2560年,2009年9月28日上午,在曲阜举行祭孔大典,数百名海外华人、华侨和侨界领袖一齐前来参与
- 以40 m/s的初速度竖直向上抛出一个物体,经过t秒后,物体的重力势能是动能的3倍,g=10 m/s2,则t的大小为(
- 文明的发祥总是和河流密切相关。西亚的中心地带荒凉而干旱,这片漫无边际的沙漠,如今看来毫无生气,可它却拥有多个“世界之最”
- 右下图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是 A.左池电极反应式:X4++ 2e-=X2
- 下列为某一遗传病的家系图,已知Ⅰ1为携带者。可以准确判断的是()A.该病为常染色体隐性遗传 B.Ⅱ4是携带者 C.Ⅱ6是
- 已知数列的前项和为,(). (1)证明数列是等比数列,求出数列的通项公式; (2)设,求数列的前项和; (3)数列中是否
- 依次填入下列各句横线处的词语,最恰当的一组是( ) (1)报载孙中山的孙女孙穗芳女士近年多次 北京大学,为推动孙中山研究
- 方程表示的曲线为 ( ) A.一条直线和一个圆
- 过正方形ABCD的顶点A作线段AA1⊥平面ABCD,且AA1=AB,则平面ABA1与平面CDA1所成的二面角的度数是(
- 长江三角洲地区城市化滞后于工业化的社会发展进程,如今出现急剧变化,城市间快速交通网络呈现出全面接轨态势,农民向城市迁移,
- 某溶液中加入铝粉能产生氢气,在该溶液中一定能大量共存的离子组是() A.K+、NH4+、Cl﹣、SO42﹣ B.Cu
- 下列各项中翻译不恰当的一项是:( ) A.先是,庭中通南北为一。 在这以前,庭院南北相通成为一体。 B.吾儿,久不见若影
- 有机物A的结构简式为:从A出发,可以发生所示的一系列反应,其中K的分子式为C12H14O4,L和K互为同分异构体,F的产
- 把下面的长句变成几个较短的句子。 从严密的综合科学体系讲,最基础的是研究物质运动基本规律的物理和指导我们推理、演算的数学
 具有漂白性
具有漂白性 溶于水配成粉红色溶液,然后用酒精灯加热,观察实验现象
溶于水配成粉红色溶液,然后用酒精灯加热,观察实验现象 溶液的试管中同时加入
溶液的试管中同时加入 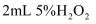 溶液,观察实验现象
溶液,观察实验现象


