化学反应速率和化学平衡 知识点题库
-
(1) I.CO还原NO的脱硝反应:
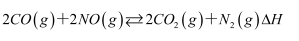
已知:
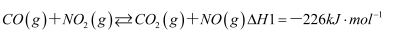

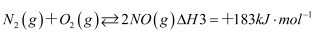
脱硝反应△H=,该反应向正反应方向自发进行的倾向很大,其原因是,有利于提高NO平衡转化率的条件是(写出两条)。
-
(2) 以Mn3O4为脱硝反应的催化剂,研究者提出如下反应历程,将历程补充完整。
第一步:;
第二步:3MnO2+2CO=Mn3O4+2CO2
-
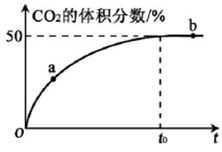
(3) 在恒温恒容的密闭容器中,充入等物质的量的CO和NO混合气体,加入Mn3O4发生脱硝反应,t0时达到平衡,测得反应过程中CO2的体积分数与时间的关系如右图所示。
①比较大小:a处V正b处V逆(填“>”、“<”或“=”)
②NO的平衡转化率为。
-
(4) II.T℃时,在刚性反应器中发生如下反应:
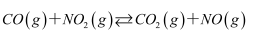 ,化学反应速率
,化学反应速率 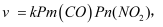 k为化学反应速率常数。研究表明,该温度下反应物的分压与化学反应速率的关系如下表所示:
k为化学反应速率常数。研究表明,该温度下反应物的分压与化学反应速率的关系如下表所示: 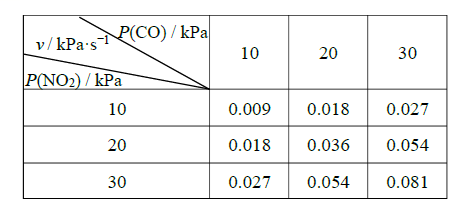
若反应初始时P(CO)=P(NO2)=akPa,反应t min时达到平衡,测得体系中P(NO)=bkPa,则此时v=
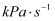 (用含有a和b的代数式表示,下同),该反应的化学平衡常数Kp=(Kp是以分压表示的平衡常数)。
(用含有a和b的代数式表示,下同),该反应的化学平衡常数Kp=(Kp是以分压表示的平衡常数)。
 2NH3 , 其反应速率与时间的关系如图所示。下列说法错误的是( )
2NH3 , 其反应速率与时间的关系如图所示。下列说法错误的是( ) 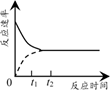
A.催化剂 B.温度 C.光照 D.固体表面积
-
(1) 夏天的食品容易霉变,冬天就不容易发生该现象;
-
(2) 熔化的氯酸钾放出气泡很慢,撒入少量二氧化锰很快产生气体;
-
(3) 工业上常将固体燃料粉碎,以提高燃烧效率 ;
-
(4) 集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸 。
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸
④加 CH3COONa固体 ⑤加NaCl溶液 ⑥滴入几滴CuSO4溶液
⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 1mol·L-1盐酸
 B .
B . 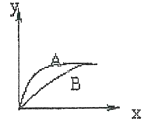 C .
C . 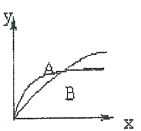 D .
D . 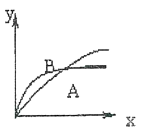
资料1:乙醇分子有两个末端,一端是憎水(易溶于油)的—C2H5;一端是亲水(易溶于水)的—OH。
资料2:破坏蛋白质分子中形成蜷曲和螺旋的各种力,使长链舒展、松弛,可导致蛋白质变性。
资料3:水分子可以松弛蛋白质外部亲水基团之间的吸引力,而-OH不能;—C2H5可以破坏蛋白质内部憎水基团之间的吸引力。
-
(1) 乙醇的结构及性质
①1mol乙醇分子中的极性共价键有mol。
②从结构角度解释乙醇的沸点比乙烷高的原因 。
-
(2) 乙醇的用途
①医用酒精(75%)制备过程与制酒的过程类似,不能饮用,但可接触人体医用。
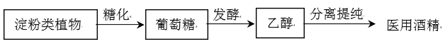
结合题中资料,下列说法正确的是(填字母)。
a.糖化、发酵的过程均含有化学变化
b.获得医用酒精常采用的分离提纯方法是蒸馏
c.浓度99%的酒精消毒杀菌效果一定大于75%的酒精
②乙醇是一种很好的溶剂,在油脂的皂化反应中,加入乙醇可加快反应速率,其原因是 。
-
(3) 乙醇的工业制取
乙醇的工业制取方法很多,由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙
醇的工艺流程。
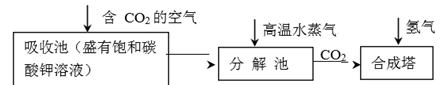
该流程中能循环使用的物质是。
 ,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
-
(1)
 的捕集:
的捕集: ①
 属于分子(填“极性”或“非极性”),其晶体(干冰)属于晶体。
属于分子(填“极性”或“非极性”),其晶体(干冰)属于晶体。②用饱和
 溶液做吸收剂可“捕集”
溶液做吸收剂可“捕集”  。若所得溶液
。若所得溶液 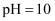 ,溶液中
,溶液中 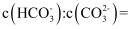 ;(室温下,
;(室温下, 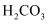 的
的 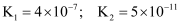 )若吸收剂失效,可利用
)若吸收剂失效,可利用  溶液使其再生,写出该反应的离子方程式。
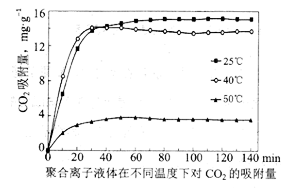
溶液使其再生,写出该反应的离子方程式。③聚合离子液体是目前广泛研究的
 吸附剂。结合下图分析聚合离子液体吸附
吸附剂。结合下图分析聚合离子液体吸附  的有利条件是。
的有利条件是。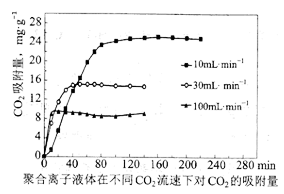
-
(2) 生产尿素:工业上以
 、
、  为原料生产尿素
为原料生产尿素 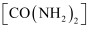 ,该反应分为二步进行:
,该反应分为二步进行: 第一步:
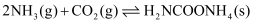
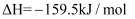
第二步:
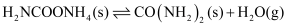
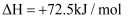
写出上述合成尿素的热化学方程式。
-
(3) 合成乙酸:中国科学家首次以
 、
、  和
和  为原料高效合成乙酸,其反应路径如图所示:
为原料高效合成乙酸,其反应路径如图所示: 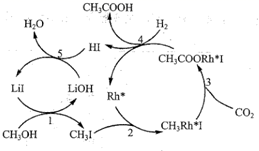
①原料中的
 可通过电解法由
可通过电解法由  制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成  的电极反应式:。
的电极反应式:。②根据图示 , 写出总反应的化学方程式:。
 2NO2(g) △H<0达平衡后,若分别采取下列措施;①增大压强 ② 减小NO2的浓度 ③增大O2浓度、④升高温度 ⑤加入催化剂,能使平衡向正向移动的是( )
2NO2(g) △H<0达平衡后,若分别采取下列措施;①增大压强 ② 减小NO2的浓度 ③增大O2浓度、④升高温度 ⑤加入催化剂,能使平衡向正向移动的是( )
-
(1) 利用反应2NO(g)+2CO(g)=N2(g)+2CO2(g),可实现汽车尾气的无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比m[m=
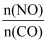 ]的关系如图1所示。
]的关系如图1所示。 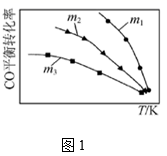
①该反应的ΔH0(填“>”、“<”或“=”)。
②投料比m1、m2、m3中,最大的是。
③随着温度的升高,不同投料比下CO平衡转化率趋于相近的原因是。
-
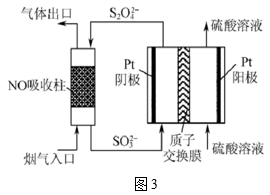
(2) 工业生产排放的烟气中同时存在SO2、NOx和CO,利用它们的相互作用可将SO2、NOx还原成无害物质,主要反应有:
2CO(g)+2NO(g)=2CO2(g)+N2(g)ΔH=akJ·mol-1
4CO(g)+2NO2(g)=4CO2(g)+N2(g)ΔH=bkJ·mol-1
4CO(g)+2SO2(g)=4CO2(g)+S2(g)ΔH=ckJ·mol-1
则2NO2(g)+S2(g)=N2(g)+2SO2(g)的ΔH=kJ·mol-1。
-
(3) NH3催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化后的V2O5作催化剂,NH3将NO还原成N2的一种反应历程如图2所示,则总反应方程式为。
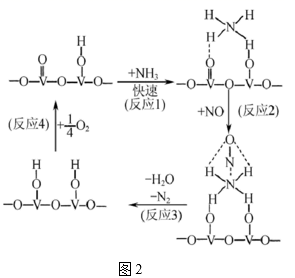
-
(4) 用间接电化学法去除烟气中NO的原理如图3所示。Pt阴极的电极反应式为。
 2NH3 , 5min内N2的物质的量减少了2mol,则用N2表示的反应速率为( )
2NH3 , 5min内N2的物质的量减少了2mol,则用N2表示的反应速率为( )
-
(1) 氮原子最外层运动状态不同的电子有种,N2的电子式:。已知N4分子中所有原子均满足最外层8电子稳定结构,写出N4的结构式。
已知: 2NO(g)+2CO(g)
 N2(g)+2CO2(g) +746.5 kJ
N2(g)+2CO2(g) +746.5 kJ -
(2) 恒温、恒容条件下,将2.0mol NO和1.0mol CO充入一个容积为2L的密闭容器中进行上述反应,反应过程中部分物质的物质的量变化如图所示。
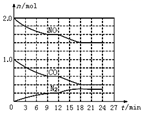
0~9min内N2的平均反应速率v(N2)=mol/(L·min);第12min时CO2的浓度为 mol/L;第12min时改变的反应条件可能为(填字母代号);
a.升高温度 b.加入NO c.加催化剂 d.减小压强 e.降低温度
-
(3) 如图是该平衡混合气中N2的体积分数随温度或压强变化的曲线。(图中L(L1、L2)、X可能是温度或压强。)可以确定X代表的是(填“温度”或“压强”),L1与L2的大小关系是L1 L2(选填“<”、“>”或“=”),你的理由是。

-
(4) 尿素溶液也可用于处理汽车尾气,所得产物都是无污染的气态物质,化学方程式如下:2CO(NH2)2+4NO+O2→2CO2+4N2+4H2O(反应条件省略)。经测定,每吸收30gNO能排放热量321.7kJ,则该反应的热化学方程式为。
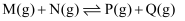 在不同温度
在不同温度 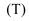 时的平衡常数
时的平衡常数 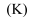 如下:
如下: | | 700 | 800 | 830 | 1000 | 1200 |
| | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
密闭容器中,某温度(T)、某时刻(t)时,反应混合物中M、N、P,Q的浓度分别为 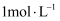 、
、 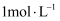 、
、 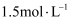 、
、 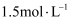 。
。
下列说法正确的是( )
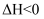 B . 若
B . 若 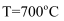 ,则t时刻反应向正反应方向进行
C . 若t时刻反应达到化学平衡,则
,则t时刻反应向正反应方向进行
C . 若t时刻反应达到化学平衡,则 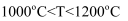 D . 当
D . 当 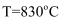 达到化学平衡时,
达到化学平衡时, 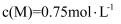
-
(1) 已知:CO(g)、H2(g)、CH3OCH3(g)的燃烧热ΔH分别为-283kJ·mol-1、-285.8kJ·mol-1、-1460kJ·mol-1 , H2O(g)=H2O(l) ΔH1=-44 kJ·mol-1。则2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH2=,该反应能否自发进行与有关。
-
(2) T1 ℃时,在恒容密闭容器中通入CH3OCH3 ,发生反应CH3OCH3(g)⇌CO(g)+H2(g) +CH4(g) ,测得容器内初始压强为50kPa,反应过程中反应时间t与气体总压p总的关系如下表所示。
反应时间t/s
0
100
350
850
2000
2500
气体总压p总/kPa
50.0
55.0
65.0
83.2
125.0
125.0
①该温度下,反应达到平衡时,CH3OCH3的分解率为;t=350s时,混合气体的平均摩尔质量为(保留三位有效数字)g·mol-1。
②若反应达到平衡后,升高温度,CH3OCH3的浓度增大,则正反应为(填“放热”或“吸热”)反应。
③该温度下,要缩短反应达到平衡所需的时间,可采取的措施是。
-
(3) 在T2℃、p0kPa(恒温、恒压)下,将等物质的量的CO与H2通入容积为VL的容器内,发生反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g)。反应达到平衡时,测得容器容积为0.6VL,用气体分压[气体分压(p)=气体总压(p总)×体积分数]代替平衡浓度表示的平衡常数Kp=(kPa)-4。反应速率v=v正-v逆=k正p2(CO)·p4(H2)-k逆p(CH3OCH3)p(H2O),k正、k逆分别为正、逆反应速率常数,p为气体的分压。该温度下,当容器体积为0.8VL时,
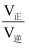 =。
=。
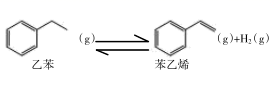
回答下列问题:
-
(1) 向甲、乙两个容积均为2L的容器中分别通入2mol乙苯,分别在T1、T2温度下进行上述反应,经过一段时间后达到平衡,反应过程中n(H2)随时间t变化情况如下表:
t/s
0
3
6
12
24
36
T1n甲(H2)/mol
0
0.36
0.60
0.80
0.80
0.80
T1n乙(H2)/mol
0
0.30
0.50
0.64
0.72
0.72
①0~3s内,T2温度下v(乙苯)=;T1T2(填>、<或=)。
②下列能说明该反应达到平衡状态的是。
A.v(苯)=v(H2)
B.c(苯乙烯):c(H2)保持不变
C.气体的平均摩尔质量保持不变
D.体系的压强保持不变
-
(2) 某同学查阅相关资料得知,该反应的平衡常数K与温度T存在如下关系式:1gK=-
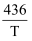 +2.86,根据(1)中实验结果推断该式是否正确,并说明理由。
+2.86,根据(1)中实验结果推断该式是否正确,并说明理由。
-
(3) 该反应是气体分子数增多的反应,降低压强对生产苯乙烯有利,但工业生产中减压操作也有不利之处,写出两点。
-
(4) 工业上为避免减压操作,采用的是恒定压强下通入水蒸气的方法,下图反映了维持总压分别为112kPa和224kPa时乙苯脱氢反应的转化率和水蒸气/乙苯用量比的关系。
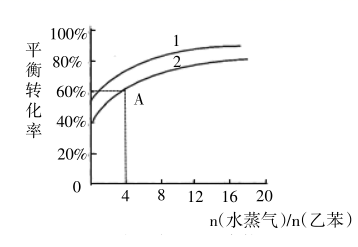
其中曲线1代表的压强是,A点对应的平衡常数Kp=(以分压表示,分压=总压×物质的量分数)。
 和
和 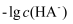 、
、  和
和 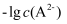 关系如图所示,下列说法正确的是( )
关系如图所示,下列说法正确的是( ) 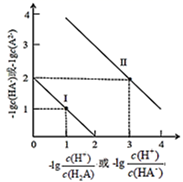
 = 2
= 2  +A2-
D . 向H2A 溶液中加入等体积等浓度的NaOH 溶液,完全反应后溶液显碱性
+A2-
D . 向H2A 溶液中加入等体积等浓度的NaOH 溶液,完全反应后溶液显碱性

已知:
Ⅰ、FePO4、CrPO4、AlPO4、Ni3(PO4)2的Ksp依次为1.3×10−22、2.4×10−23、5.8×10−19、5.0×10−31。
Ⅱ.Cr及其化合物的性质与铝类似。
回答下列问题:
-
(1) “电解Ⅰ”时,需严格控制电压,除了回收铜之外,第二个目的是,可通过一种试剂证明第二个目的是否达成,该试剂为(填化学式)。
-
(2) “除杂”时,若镍离子浓度为0.05mol·L−1 , 则应调整溶液中PO
 浓度范围为 mol·L−1 (溶液中离子浓度≤10-5mol·L−1时,认为该离子沉淀完全;
浓度范围为 mol·L−1 (溶液中离子浓度≤10-5mol·L−1时,认为该离子沉淀完全;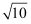 =3.2)。
=3.2)。
-
(3) “转溶”时,氢氧化钠加入量不宜过多,其原因为(用离子方程式表示)。
-
(4) “浸出Ⅱ”时,采取了多次浸取的方式,其目的为。
-
(5) “萃取Ⅱ”时,发生的反应为Cu(NH3)
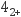 +2HR=CuR2+2NH
+2HR=CuR2+2NH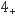 +2NH3和Ni(NH3)
+2NH3和Ni(NH3)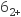 +2HR=NiR2+2NH
+2HR=NiR2+2NH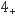 +4NH3和,则“反萃取Ⅱ”时含铜微粒发生反应的离子方程式为。
+4NH3和,则“反萃取Ⅱ”时含铜微粒发生反应的离子方程式为。
-
(6) “电解Ⅱ”时,若维持电流强度为0.5A,电流效率为90%,电解8min,理论上可获得铜g.(已知:电流效率是指电解时电极上实际沉积与理论沉积物质的量之比,F=96500C·mol-1)
-
(7) 流程中除了有机相之外,可以循环利用的物质还有(填化学式)。
-
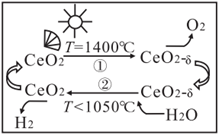
(1) 以
 为脱硝剂时,可将
为脱硝剂时,可将  还原。
还原。 已知:
i.
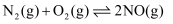
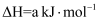
ii.
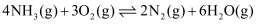
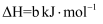
则反应:
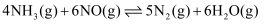 的
的 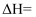
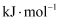 。
。 -
(2) 将
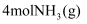 和
和  放在一密闭容器中,一定条件下发生反应ii。
放在一密闭容器中,一定条件下发生反应ii。 ①充分反应后,测得反应热量变化(填“大于”、“小于”或“等于”)
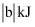 ,原因是。
,原因是。②若加入催化剂,该反应的
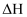 (填“变大”、“不变”或“变小”)。
(填“变大”、“不变”或“变小”)。③该反应的
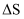 0(填“大于”、“小于”或“等于”)。
0(填“大于”、“小于”或“等于”)。 -
(3)
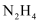 —空气燃料电池是一种高效低污染的新型电池,其结构如图所示。通入
—空气燃料电池是一种高效低污染的新型电池,其结构如图所示。通入  的一级为电池的(填“正极”或“负极”)。通入
的一级为电池的(填“正极”或“负极”)。通入 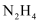 一极的电极反应式为。
一极的电极反应式为。 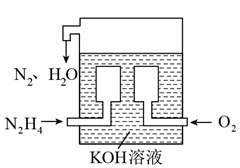
-
(4) 若用该燃料电池作电源,用惰性电极电解
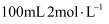 的
的 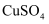 溶液,相同条件下,当两极收集到的气体体积相等时,理论上消耗的
溶液,相同条件下,当两极收集到的气体体积相等时,理论上消耗的 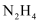 的物质的量为
的物质的量为 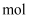 。
。
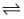 3Z(g),X、Y、Z的起始物质的量依次为2mol、1mol、3mol,当反应达平衡时,各物质的浓度可能是( )
3Z(g),X、Y、Z的起始物质的量依次为2mol、1mol、3mol,当反应达平衡时,各物质的浓度可能是( )
ⅰ.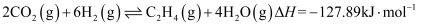
ⅱ.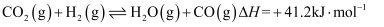
ⅲ.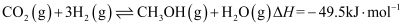
下列说法正确的是( )
 B . 反应ⅰ中H2的转化率与CO2的转化率相等
C . 反应ⅲ反应物总能量小于生成物总能量
D . 反应达平衡后,缩小容器体积,反应ⅱ平衡不移动
B . 反应ⅰ中H2的转化率与CO2的转化率相等
C . 反应ⅲ反应物总能量小于生成物总能量
D . 反应达平衡后,缩小容器体积,反应ⅱ平衡不移动
- 已知,若,则_______
- 中央电视台历史纪录片《大国崛起》解说词写道:17世纪,英国“在历史性的转变中抢了先机,已经率先到达了现代文明的入口处……
- 已知氮化钠(Na3N)在熔融时能导电,与水作用时有NH3产生。试回答下列问题: (1)Na3N中存在的离子为______
- 阅读下面的作品,完成小题。 采春 乔忠延 ①冬季日短夜长。农人说,十月里天碗里转,好婆姨做不熟三顿饭。是呀,刚刚日头还在
- 53. I’m afraid I can’t keep _______ my classmates as I’ve mi
- 结合下列材料,回答问题。 湖泊是湖盆、湖水和水中所含物质、生物等所组成的自然综合体,并参与自然界的物质和能量循环。一般来
- 过(1,1)点与y=x3相切的直线的斜率为__________.
- 阅读下面文章。完成1—3题。 军人之家 巴利斯 维拉的丈夫巴都林离开她上前线两年了。一天,邮递员送来了一封信,信上说,巴
- 把一木块放在水平桌面上保持静止,下面说法正确的是( )A.木块对桌面的压力与桌面对木块的支持力是一对平衡力B.木块对
- 下列能够正确体现中国古代君臣关系演变趋势的是 A. 坐而论道、颔首直立、伏地跪拜、三跪九叩 B. 坐而论道、颔首
- 如图所示,质量m=1kg、长L=0.8m的均匀矩形薄板静止在水平桌面上,其右端与桌子边缘相平.板与桌面间的动摩擦因数为μ
- 在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3Sn2+ +18Cl+ aH3AsO3+ bH+=aAs + 3
- 下列叙述不正确的是() A.在烷烃中,含碳质量分数最大接近85.7% B.所有烷烃和蛋白质中都存在碳碳单键 C.在蛋白质
- 熔融氢氧化钠反应选用的器皿是( ) A.陶瓷坩埚
- 在如图的地板行走,随意停下来时,站在黑色地板上的概率是( ) A、 B、 C、
- 左右两个电路都是从左端输入信号,从右端输出信号.图18-3-11中输入的是高频、低频混合的交流信号,要求只输出低频信号;
- 如图,数轴上两点分别对应实数,则下列结论正确的是( )A. B.C. D.
- 22. 若某幼儿垂体因故受到损伤,一般不引起 A. 抗寒能力减弱 B. 血糖升高 C. 生长发育迟缓 D.
- 根据下列热化学方程式 (1)C(s) + O2(g)= CO2(g)
- 下图表示细胞分裂时细胞内每条染色体DNA随细胞分裂所发生的变化。下列哪一项的细胞不能与图中ab所对应每条染色体DNA的含