燃烧热 知识点
燃烧热 知识点题库
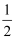 O2(g)═CO2(g)△H=﹣283kJ•mol﹣1
O2(g)═CO2(g)△H=﹣283kJ•mol﹣1
 C2H5OH(l)+
C2H5OH(l)+ 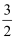 O2(g)=CO2(g)+3/2H2O(l) △H = -Q kJ/mol
D . C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H = -2Q kJ/mol
O2(g)=CO2(g)+3/2H2O(l) △H = -Q kJ/mol
D . C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H = -2Q kJ/mol
-
(1) 已知甲醇的燃烧热为726.5kJ/mol,则甲醇燃烧的热化学方程式为.
-
(2) 利用合成气主要成分为CO和H2)在催化剂的作用下合成甲醇,已知反应中有关物质的化学键键能数据如下表所示:
化学键
H-H
C-O
C≡O
H-O
C-H
E/(kJ/mol)
436
343
1076
465
413
则: CO(g)+2H2(g)⇌CH3OH(g)△H=kJ•mol-1 , 每消耗标准状况下8.96LCO时转移电子的物质的量是.
-
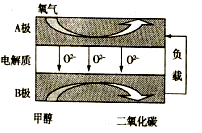
(3) 以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。如图是月前研究较多的一类固体氧化物燃料电池工作原理示意图。B极为电池极,B极的电极反应式为
 体积,CO2占
体积,CO2占 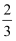 体积,已知:C(s)+
体积,已知:C(s)+  O2(g)=CO(g)△H=-Q1kJ/mol,CO(g)+
O2(g)=CO(g)△H=-Q1kJ/mol,CO(g)+  O2(g)=CO2(g)△H=-Q2kJ/mol,与这些焦炭完全燃烧相比较,损失的热量是中正确的是()
O2(g)=CO2(g)△H=-Q2kJ/mol,与这些焦炭完全燃烧相比较,损失的热量是中正确的是()
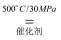 2NH3(g) △H = -38.6kJ•mol-1
D . 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2Al2O3(s) △H = -2834.9kJ•mol-1 , 4Al(s) + 2O3(g) ═ 2Al2O3(s) △H = -3119.1kJ•mol-1 , 则O2比O3稳定
2NH3(g) △H = -38.6kJ•mol-1
D . 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2Al2O3(s) △H = -2834.9kJ•mol-1 , 4Al(s) + 2O3(g) ═ 2Al2O3(s) △H = -3119.1kJ•mol-1 , 则O2比O3稳定
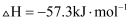 ,则
,则  和
和 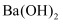 反应的中和热
反应的中和热 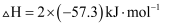 B .
B . 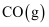 的燃烧热是
的燃烧热是 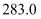
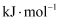 ,则
,则 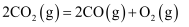 反应的
反应的 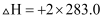
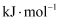 C . 需要加热才能发生的反应一定是吸热反应
D . 乙烷的燃烧热就是1mol乙烷燃烧生成气态水和二氧化碳所放出的热量
C . 需要加热才能发生的反应一定是吸热反应
D . 乙烷的燃烧热就是1mol乙烷燃烧生成气态水和二氧化碳所放出的热量
 C(金刚石)△H=+1.9 kJ/mol”可知金刚石比石墨稳定
B . 在101KPa时,1mol碳燃烧所放出的热量为碳的燃烧热
C . 相同的条件下,如果1 mol氢原子所具有的能量为E1 , 1 mol氢分子的能量为E2 , 则2E1﹥E2
D . HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4 和Ca(OH)2 反应的中和热为△H=-(2×57.3)kJ/mol
C(金刚石)△H=+1.9 kJ/mol”可知金刚石比石墨稳定
B . 在101KPa时,1mol碳燃烧所放出的热量为碳的燃烧热
C . 相同的条件下,如果1 mol氢原子所具有的能量为E1 , 1 mol氢分子的能量为E2 , 则2E1﹥E2
D . HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4 和Ca(OH)2 反应的中和热为△H=-(2×57.3)kJ/mol
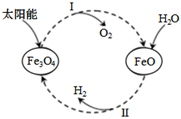
过程Ⅰ:……
过程Ⅱ:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2 kJ·mol﹣1
下列说法正确的是( )
 O2(g) ΔH=﹣156.6 kJ·mol﹣1
C . 氢气的摩尔燃烧焓为ΔH=﹣285.8 kJ·mol﹣1
D . 铁氧化合物循环制H2具有成本低、产物易分离等优点
O2(g) ΔH=﹣156.6 kJ·mol﹣1
C . 氢气的摩尔燃烧焓为ΔH=﹣285.8 kJ·mol﹣1
D . 铁氧化合物循环制H2具有成本低、产物易分离等优点
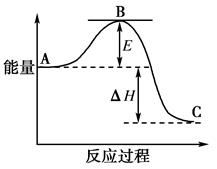
已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
-
(1) 图中A、C分别表示、,E的大小对该反应的反应热(填“有”或“无”)影响;
-
(2) 该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?,理由是;
-
(3) 图中ΔH=kJ·mol-1;
-
(4) 已知单质硫的燃烧热ΔH=-296 kJ·mol-1 , 计算由S(s)生成1 mol SO3(g)的ΔH(写出计算过程)。
-
(1) 用离子方程式表示 NH4Cl 溶液显示酸性的原因:。
-
(2) 有机物 M 经过太阳光光照可转化成 N,转化过程如下:
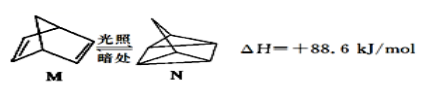
则 M、N 相比,较稳定的是。
-
(3) 已知在常温常压下:
①2CH3 OH(l)+3O 2 (g) =2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式。
-
(1) 氢气是一种环保的气体,不会污染大气且热值高。相关化学键的键能表示如表:
化学键
O=O
H—H
O—H
键能E/(kJ·mol-1)
a
b
c
则氢气燃烧热的△H=kJ/mol(用含a、b、c代数式表示)
-
(2) 催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1。在T1℃时,将0.10molCO与0.40molH2O充入5L的容器中,反应平衡后H2的物质的量分数x(H2)=0.08。
CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1。在T1℃时,将0.10molCO与0.40molH2O充入5L的容器中,反应平衡后H2的物质的量分数x(H2)=0.08。①反应平衡常数K=。(结果保留2位有效数字)
②保持K不变,提高CO平衡转化率措施有:。(任意一条)
③由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为。(填字母)
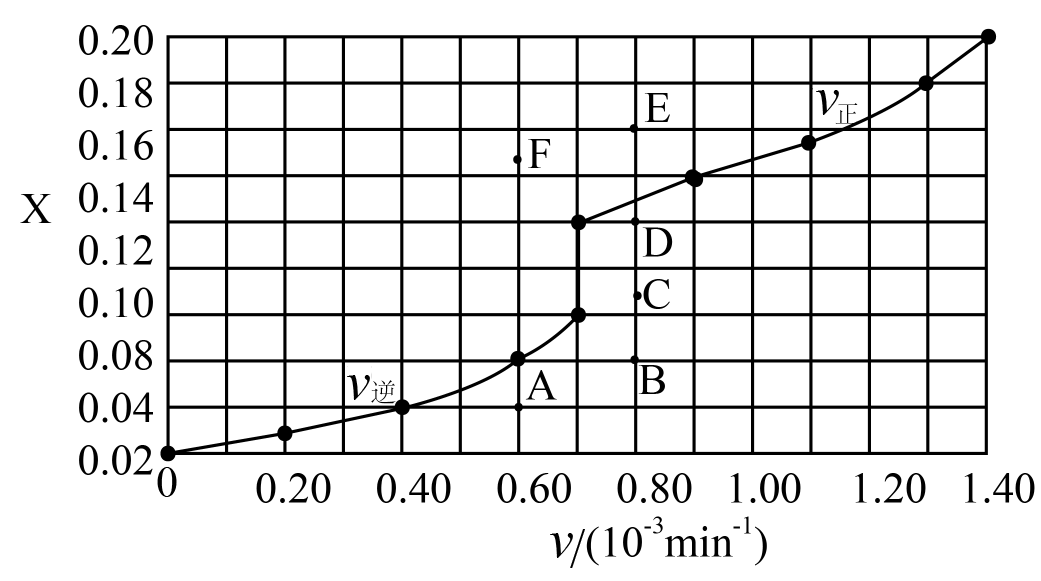
④研究表明,CO催化变换反应的速率方程为:v=k[x(CO)•x(H2O)-
 ],式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,KP为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的KP(填“增大”或“减小”或“不变”)。根据速率方程分析,T>Tm时v逐渐减小的原因是。
],式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,KP为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的KP(填“增大”或“减小”或“不变”)。根据速率方程分析,T>Tm时v逐渐减小的原因是。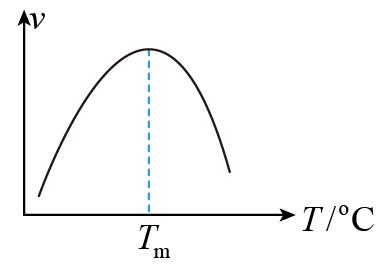
-
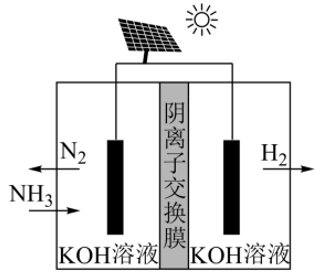
(3) 氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。阳极的电极反应式为。

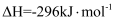 B .
B . 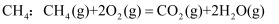
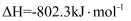 C .
C . 
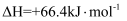 D .
D . 
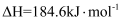
- 设f(x)、g(x)是R上的可导函数,分别是f(x)、g(x)的导函数,且,则当时,有( ) A. f(x)g(x
- 如图所示的电路,电压表的示数为2V,电流表的示数为1A,电路中的电源电压为5V,则R2的电阻为多少。
- 若,则等于 ( ) A. B. C. D.
- —How difficult physics it is! I really want to drop it !
- He is only too ready to help others,seldom _____, refusing t
- 既是我国大型钢铁基地,又是我国重要的纺织工业基地的是A.北京、鞍山、太原、成都
- 发达国家产业结构中比重最大的是( )A.第一产业
- 下图是2008年北京奥运会开幕式展示中国传统文化的画卷,既表达了中国传统文化中的“和谐”理念,又向世界展示了当代中国致力
- 既遵守了城邦法律又捍卫了思想自由和人格尊严的勇于就死的先哲是( )A、普罗塔戈拉 B、苏格拉底
- 亚特兰大奥运会提出了科技奥运的主题;悉尼奥运会确定了绿色奥运的主题;雅典奥运会展示了人文奥运的主题。北京奥运会把“绿色奥
- 古诗文默写。(8分)【小题1】四面边声连角起,千嶂里, ▲ 。【小题2】鸡声茅店月,
- 近现代.由于政治、经济、历史等多种因素的影响,使国家结构复杂,产生了多种结构形式。不同结构形式的划分主要是根据: A.国
- 下列变化不能通过一步反应实现的是 () A. HgO→Hg B.NaNO3→NaCl
- 如图所示的实验操作中正确的是() A. 量取液体 B. 加热液体 C. 滴加液体 D. 点酒精灯
- 每个肾脏的肾单位大约有( ) A.100个 B.100万个 C.1000万个 D.
- 1......
- 19.对于多细胞生物而言,下列有关细胞生命历程的说法正确的是( ) A.细胞分化导致细胞中的遗传物质发生改变
- 下列细胞器在其生命活动过程中均既需要消耗水又可产生水的是 ①核糖体 ②叶绿体
- x>2(6分)解不等式组,并把解集在数轴上表示出来.
- A sign is another kind of language. Here are some of them th



