化学反应中能量的转化 知识点题库
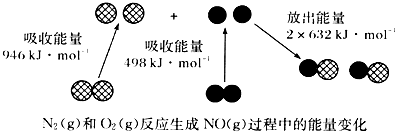
则反应:A(g)+B(g)=2C(g)( )
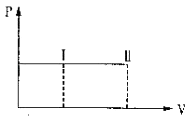

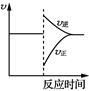 表示对某化学平衡体系改变温度后反应速率随时间的变化
B .
表示对某化学平衡体系改变温度后反应速率随时间的变化
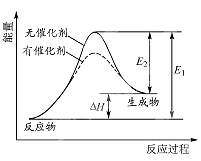
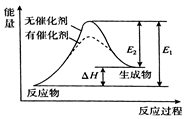
B . 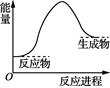 表示反应物断键吸收的总能量大于生成物成键放出的总能量
C .
表示反应物断键吸收的总能量大于生成物成键放出的总能量
C . 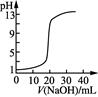 表示0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化
D .
表示0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化
D . 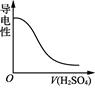 表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况
表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况
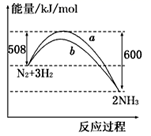
 2NH3 △H=-92 kJ/mol
B . a曲线是加入催化剂时的能量变化曲线
C . 加入催化剂,该化学反应的反应热不改变
D . 在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为92kJ
2NH3 △H=-92 kJ/mol
B . a曲线是加入催化剂时的能量变化曲线
C . 加入催化剂,该化学反应的反应热不改变
D . 在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为92kJ
-
(1) 氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g)
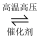 2NH3(g)。
2NH3(g)。 ①合成氨的反应中的能量变化如图所示。
该反应是反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量(填“大于”或“小于”)生成物化学键形成放出的总能量。
②在一定条件下,将一定量的N2和H2的混合气体充入某定容密闭容器中,一段时间后,下列叙述不能说明该反应达到平衡状态的是(填序号)。
A.容器中混合气体的密度不随时间变化
B.单位时间内断裂3molH-H键的同时断裂6molN-H键
C.N2、H2、NH3的物质的量之比为1:3:2
D.容器中混合气体的平均相对分子质量不随时间变化
-
(2) 容器容积为1L,T2℃在起始体系中加入1molN2、3molH2 , 经过5min反应达到平衡时放出热量55.44kJ。保持容器体积和温度不变,若起始时向容器内放入2molN2和6molH2 , 达平衡后放出的热量为Q , 则Q110.88kJ(填“>”、“<”或“=”)。
-
(3) 目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),在体积为1L的密闭容器中,充入1molCO2和3molH2 , 测得CO2和CH3OH(g)的浓度随时间变化如图所示。达平衡时容器内平衡时与起始时的压强之比。
CH3OH(g)+H2O(g),在体积为1L的密闭容器中,充入1molCO2和3molH2 , 测得CO2和CH3OH(g)的浓度随时间变化如图所示。达平衡时容器内平衡时与起始时的压强之比。 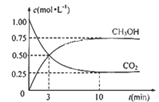
-
(4) 有可逆反应Fe(s)+CO2(g)
 FeO(s)+CO(g)∆H>0。
FeO(s)+CO(g)∆H>0。 ①若起始时把Fe和CO2放入体积固定的密闭容器中,CO2的起始浓度为2.0mol/L,某温度时达到平衡,此时容器中CO的浓度为1.0mol/L,则该温度下上述反应的平衡常数K=。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件,升高温度,反应混合气体中CO2的物质的量分数变化(选填“增大”、“减小”、“不变”)。
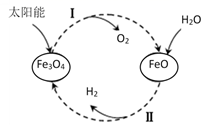
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g)ΔH=+313.2kJ/mol
过程Ⅱ:……
下列说法错误的是( )
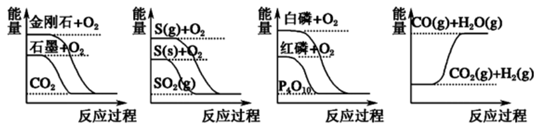
据此判断下列说法中正确的是( )
-
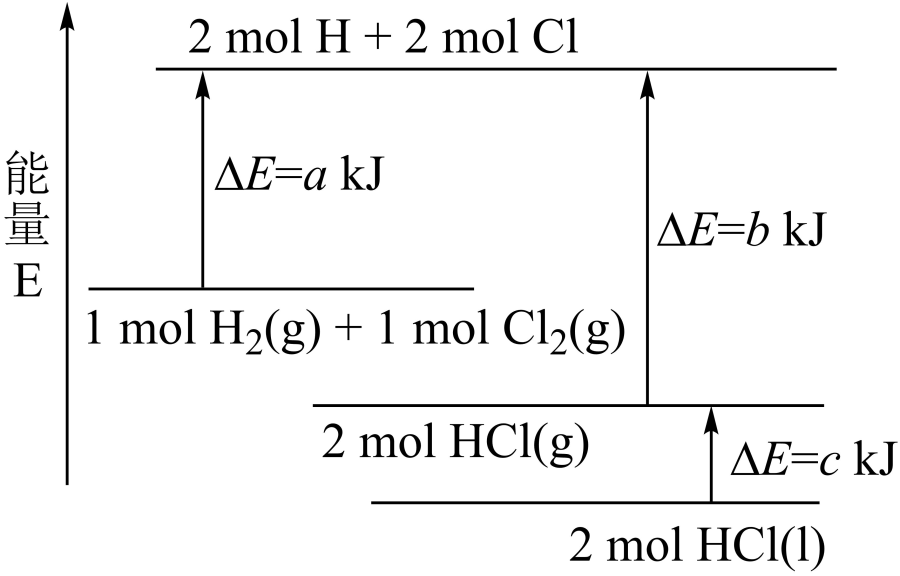
(1) I. H2+Cl2=2HCl的反应过程如图所示:
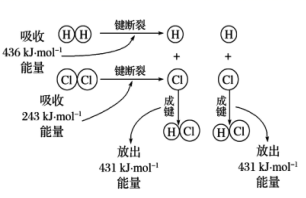
①根据如图填写下表:
化学键
断裂或形成1mol化学键时能量变化
反应中能量变化
Cl-Cl
吸收243kJ
共吸收679kJ
H-H
吸收436kJ
H-Cl
放出431kJ
共放出kJ
②该反应为反应(填“放热”或“吸热”)。
-
(2) 硅是太阳能电池的重要材料。工业冶炼纯硅的原理是:
粗硅冶炼:(a)SiO2+2C
 Si+2CO↑;
Si+2CO↑;精炼硅:(b)Si+3HCl
 SiHCl3+H2;
SiHCl3+H2;(c)SiHCl3+H2
 Si+3HCl
Si+3HCl化学反应与能量变化如图所示,回答下列问题:
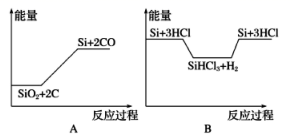
①(a)是反应,(b)是反应;(c)是反应(填“吸热"或“放热”)。
②反应(b)破坏反应物中的化学键所吸收的能量(填“大于”或“小于”)形成生成物中化学键所放出的能量。
-
(3) II.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
①该电池的负极材料是,电解质溶液是。
②正极上出现的现象是。
③若导线上转移电子1mol,则生成银g。
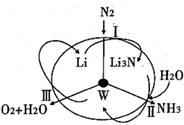
 是中间产物
B . 过程II生成的W为LiOH
C . 反应III中能量转化的方式是化学能转变为电能
D . 整个过程中锂的总量保持不变
是中间产物
B . 过程II生成的W为LiOH
C . 反应III中能量转化的方式是化学能转变为电能
D . 整个过程中锂的总量保持不变
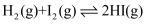 能量历程如图所示。下列说法正确的是( )
能量历程如图所示。下列说法正确的是( )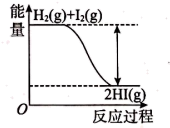
 的能量一定高于
的能量一定高于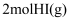 的能量
B . 拆开
的能量
B . 拆开 和
和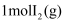 所需能量低于拆开
所需能量低于拆开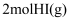 所需能量
C . 该反应不需要加热就能发生
D . 恒温恒容条件下,当容器内压强不再改变时可判定反应已达平衡
所需能量
C . 该反应不需要加热就能发生
D . 恒温恒容条件下,当容器内压强不再改变时可判定反应已达平衡
-
(1) 下列反应属于吸热反应的是。
①铝片和盐酸反应 ②酸碱中和反应
③
 晶体与
晶体与 混合搅拌 ④碳酸钙分解
混合搅拌 ④碳酸钙分解⑤
 在
在 中燃烧 ⑥灼热的碳与
中燃烧 ⑥灼热的碳与 的反应
的反应 -
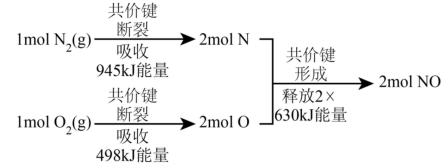
(2) 已知汽缸中氮气和氧气反应生成一氧化氮的能量变化值如图所示,则由该反应生成1molNO时,应(填“释放”或“吸收”)kJ能量。
-
(3) 某学习小组依据氧化还原反应原理:
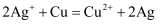 设计成的原电池如图所示。
设计成的原电池如图所示。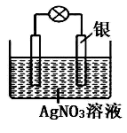
①从能量转化角度分析,上述原电池将化学能转化为;
②负极的电极材料为;(填化学式)
③正极发生的电极反应;
④若银电极增重5.4g,外电路转移电子的物质的量mol。
-
(4) 为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关反应一段时间后的实验现象,下列说法正确的是____。
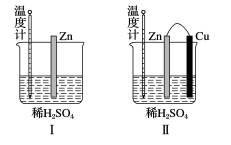 A . 图I中温度计的示数高于图II的示数 B . 图I和图II中温度计的示数相等,且均高于室温 C . 图I和图II的气泡均产生于锌棒表面 D . 图II中产生气体的速率比I慢
A . 图I中温度计的示数高于图II的示数 B . 图I和图II中温度计的示数相等,且均高于室温 C . 图I和图II的气泡均产生于锌棒表面 D . 图II中产生气体的速率比I慢
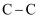 、
、 、
、 , 丙酮在激光强度为
, 丙酮在激光强度为 时,在特定的时间间隔内这4种类型的化学键的键长变化如图2所示。
时,在特定的时间间隔内这4种类型的化学键的键长变化如图2所示。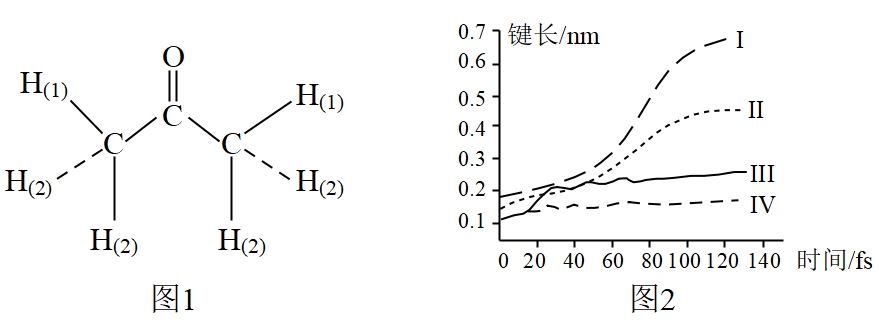
下列判断错误的是( )
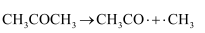 D . 丙酮在该条件下的光解反应中只有化学键的断裂
D . 丙酮在该条件下的光解反应中只有化学键的断裂
- 下列各句中,没有语病的一句是 ( ) A.由中国新兴建设开发总公司赞助建造的第二十一届世界大学生运动会主舞台,在经过短短
- 已知对于圆x2+(y-1)2=1上任意一点P(x,y),不等式x+y+m≥0恒成立,求实数m的取值范围.
- —Did you find your lostkey?—No, but I think ________ must ha
- 已知双曲线 (a>0,b>0)的右焦点为F,若过点F且倾斜角为60°的直线与双曲线的右支有且只有一个交点,
- —What _________sunny day it is ! Let’s go and visit _______W
- 锌的核电荷数为30,其最外电子层上只有2个电子,常显+2价。据此,请画出锌离子的结构示意图。
- 下列各组词语中划线的字的读音,与所给注音全都相同的一组是( ) A.供gōng 供稿 供养 供销 口
- 右图是亚洲中纬度地区一种适应环境、别具地方特色的民居,称为土拱。这种民居较高大,屋顶为拱顶或平顶,墙体由土坯砌成,厚度很
- 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的
- 下列物质中,氯元素化合价最低的是()A. Cl2 B. HCl04 C. KCl03 D. KC1
- 下图中能正确表示在减数分裂过程中一个细胞中DNA的含量变化的图像(纵轴表示一个细胞中的DNA的相对含量,横轴表示时期t)
- 世界的水稻生产,绝大多数分布在 A.非洲刚果盆地 B.南美洲亚马孙平原 C.东亚、东
- 一瓶NaCl溶液里各部分的性质() A.上面跟下面不相同 B.完全不相同 C.有
- 明清时期商业繁荣,大量农产品和手工业产品投放市场。导致明清时期商品经济发展的原因有( ) ①国外高产农作物
- 已知sinα=,且α是第二象限角,则tanα是( )A. B.
- 两数1和4的等差中项和等比中项分别是( ) A.5,2 B.5, C.,4
- 互联网的发展催生了新的经济形式,学生小符就是一种叫“换客”的时尚一族。他将自己的闲置物品发布到相关网站,注明自己所需要的
- 下图实线AB为某一纬线的一部分,虚线AC为晨昏线,两线相切于A点,O点为极点。完成3~4题。3.如果C点地方时为4时,A
- 酵母菌是人类的第一种“家养微生物”。在一个固定容积的培养液中,单位时间内在不同的氧气浓度下,下图所示的酵母菌相关指标与实
- “有健康才有将来”,健康是人类社会永恒的主题,各种疾病在不同程度上影响着人们健康,下列关于各种疾病的正确叙述是 A.白化



