元素周期律和元素周期表的综合应用 知识点题库
X、Y、Z、W均为短周期元素,它们在周期表中相应位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中错误的是( )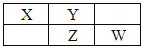
A . Y的气态氢化物的稳定性较Z的强
B . 原子半径:W>Z>Y>X
C . W的最高价氧化物对应水化物的酸性较Z的强
D . 四种元素的单质中,Z的熔、沸点最高
下列性质的比较,正确的是( )
A . 酸性:H2SiO3 >H2CO3
B . 碱性Mg(OH)2 >Al(OH)3
C . 稳定性 SiH4 >PH3
D . 原子半径N > C
类比推理是化学中常用的思维方法.下列推理正确的是( )
A . CO2是直线型分子,推测CS2也是直线型分子
B . SiH4的沸点高于CH4 , 推测H2Se的沸点高于H2S
C . Fe与Cl2反应生成FeCl3 , 推测Fe与I2反应生成FeI3
D . NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr
有A,B,C,D,E五种短周期的主族元素,其原子序数依次增大.其中只有C是金属,D的单质是黄色固体,A,B,D在周期表中的相对位置关系如图所示,下列说法正确的是( )
![]()
A . E元素位于周期表中的第三周期、ⅥA族
B . B的简单阴离子比D的简单阴离子还原性强
C . B与C形成的化合物中一定含有共价键
D . A,B两元素形成的常见化合物的分子中均含有极性键
已知短周期元素的离子.aA2+、bB+、cC3﹣、dD﹣都具有相同的电子层结构,则下列叙述正确的是( )
A . 原子半径:A>B>C>D
B . 原子序数:d>c>b>a
C . 离子半径:C>D>B>A
D . 单质的还原性:A>B>D>C
元素周期表里金属元素和非金属元素分界线附近的元素可能用于( )
A . 制新农药
B . 制半导体材料
C . 制新医用药物
D . 制高温合金
短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是( )
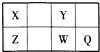
A . 钠与W可能形成Na2W2化合物
B . 由Z与Y组成的物质在熔融时能导电
C . W得电子能力比Q强
D . X有多种同素异形体,而Y不存在同素异形体
A、B、C、D、E、F均为短周期元素,原子序数依次递增.A元素原子核内无中子.B元素原子核最外层电子数是次外层电子数的2倍.C元素是地壳中含量最多的元素.D是短周期元素中金属性最强的元素.E与F的位置相邻,F的最高价氧化物的水化物为最强酸.
-
(1) 推断B在元素周期表中的位置:第周期,第族.
-
(2) 写出F的电子排布式:.
-
(3) C、D可形成淡黄色的粉末,其电子式为.
-
(4) 写出A与C形成的10电子微粒的化学式:、、.
短周期元素的离子  、
、  、
、  、
、  都具有相同的电子层结构,下列推断错误的是( )
都具有相同的电子层结构,下列推断错误的是( )
 、
、  、
、  、
、  都具有相同的电子层结构,下列推断错误的是( )
都具有相同的电子层结构,下列推断错误的是( )
A . 原子序数: 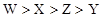 B . 离子半径:
B . 离子半径: 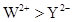 C . 还原性:
C . 还原性: 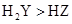 D . 碱性:
D . 碱性: 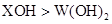
短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的电子数是其电子层数的3倍,Y的非金属性在所有短周期元素中最强,Z的最外层电子数与最内层电子数相等,W是地壳中含量第二多的元素。下列叙述正确的是( )
A . 原子半径的大小顺序:r(Z)>r(W)>r(Y)>r(X)
B . Y的单质与H2化合时,点燃安静燃烧,光照则会发生爆炸
C . 最简单气态氢化物的稳定性:X>W
D . 单质Z不能与水发生化学反应
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
A . X与Y形成化合物时,X显负价,Y显正价
B . 第一电离能Y一定小于X
C . 最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性
D . 气态氢化物的稳定性:HmY小于HnX
短周期主族元素X、Y、Z、W在周期表中的位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍,下列说法一定正确的是( )
| X | |||
| Y | Z | W |
A . Z的简单气态氢化物的热稳定性比W的强
B . 元素X与Y可形成化合物YX
C . Z的氧化物形成的晶体是分子晶体
D . W元素的氧化物的水化物是强酸
对Na、Mg、Al的有关性质的叙述正确的是( )
A . 离子半径:Na+>Mg2+>Al3+
B . 原子半径:Na<Mg<Al
C . 离子的氧化性:Na+>Mg2+>Al3+
D . 单质的还原性:Na<Mg<Al
下列说法错误的是( )
A . 有化学键断裂的过程不一定是化学过程
B . NH4Cl 和 Na2SO4 晶体中含有的化学键类型相同
C . H2O 比 H2S 更稳定,是因为氧的非金属性更强
D . 离子晶体中一定含有离子键,分子晶体中一定含有共价键
-
(1) Ⅰ.有下列各组物质:A .
 和
和  (臭氧)
B .
(臭氧)
B .  和
和  C .
C .  和
和 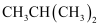 D .
D . 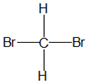 和
和 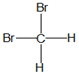 E . 葡萄糖和果糖
F . 淀粉和纤维素
G . 液氯和氯气
E . 葡萄糖和果糖
F . 淀粉和纤维素
G . 液氯和氯气 ______组两物质互为同位素
-
(2) 组两物质互为同素异形体
-
(3) 组两组物质互为同分异构体
-
(4) 组中的物质是同一物质
-
(5) Ⅱ.科学家合成出了一种新化合物(如图所示),其中
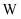 、
、  、
、  、
、 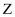 为同一短周期元素,
为同一短周期元素, 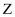 核外最外层电子数是
核外最外层电子数是  核外电子数的一半。
核外电子数的一半。 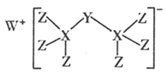
元素
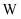 的名称是。
的名称是。 -
(6) 元素
 、
、  、
、 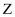 非金属性的从大到小的顺序为。(填元素符号)
非金属性的从大到小的顺序为。(填元素符号)
-
(7) 该新化合物中(填元素符号)通过得到电子达到8电子稳定结构。
氧、碳等非金属元素形成的物质种类繁多、性状各异。
-
(1) 氧、氟、氮三种元素都可形成简单离子,它们的离子半径最小的是(填离子符号),硅元素在元素周期表中的位置是。CO2和SiO2是同一主族元素的最高正价氧化物,常温下CO2为气体,SiO2为高熔点固体。请分析原因:。
-
(2) 比较硫和氯性质的强弱。热稳定性H2SHCl(选填“<”、“>”或“=”,下同);酸性:HClO4H2SO4。用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:。
-
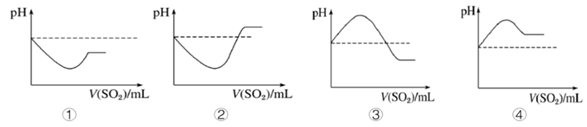
(3) 红酒中添加一定量的SO2 可以防止酒液氧化,这利用了SO2 的性。若将SO2气体通入H2S水溶液中直至过量,下列表示溶液的pH随通入SO2气体体积变化的示意图正确的是(填序号)。
已知NaHSO3溶液呈酸性,而HSO
 既能电离又能水解。则在NaHSO3溶液中c(H2SO3)c(SO
既能电离又能水解。则在NaHSO3溶液中c(H2SO3)c(SO  )(选填“<”、“>”或“=”) 。
)(选填“<”、“>”或“=”) 。 -
(4) 亚硫酸钠和碘酸钾在酸性条件下反应生成硫酸钠、硫酸钾、碘和水,配平该反应方程式
_Na2SO3+_KIO3+_H2SO4
 _Na2SO4+_K2SO4+_I2+_ H2O
_Na2SO4+_K2SO4+_I2+_ H2O
我国科学家潘锦功发明了“碲化镉薄膜太阳能电池”,被科学家称为“挂在墙壁上的油田”。下列说法错误的是( )

A . 周期表中碲和镉都位于长周期
B . 该电池将光能全部转化成电能
C . 推广使用该电池有利于“碳中和”
D . 保护层压件的铝合金属于金属材料
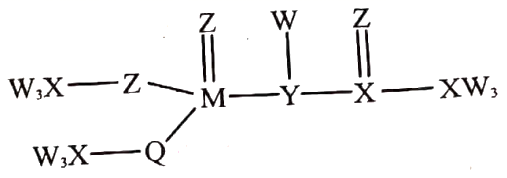
一种低毒杀虫剂的结构如图所示,其组成元素W、X、Y、Z、M、Q为原子序数依次增大的短周期主族元素,其中W的原子核内只有1个质子,原子核外电子的数目Q比Z多8个。下列说法正确的是( )
A . 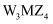 是一种强酸
B . 简单氢化物沸点:
是一种强酸
B . 简单氢化物沸点: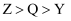 C . 简单离子半径:
C . 简单离子半径: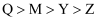 D .
D . 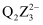 和
和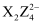 均能使酸性高锰酸钾溶液褪色
均能使酸性高锰酸钾溶液褪色
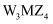 是一种强酸
B . 简单氢化物沸点:
是一种强酸
B . 简单氢化物沸点: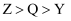 C . 简单离子半径:
C . 简单离子半径: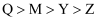 D .
D . 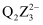 和
和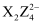 均能使酸性高锰酸钾溶液褪色
均能使酸性高锰酸钾溶液褪色
短周期主族元素X、Y、Z、W原子序数依次增大,X原子的原子核内只有1个质子,Y原子最外层比W原子最外层多1个电子,Z的单质是空气中含量最高的气体,W的单质在常温下接触浓硫酸会钝化。下列说法正确的是( )
A . 原子半径:Y<Z<W
B . Y的简单气态氢化物的沸点比Z的高
C . X、Y形成的化合物只含有极性键
D . X与Z可形成离子化合物
X、Y、Z三种短周期元素在周期表中的位置如图所示。下列说法正确的是( )
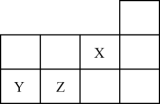
A . 原子半径:Z>Y>X
B . 第一电离能:X>Y>Z
C . 简单氢化物的键角:Z>Y
D . 最高正化合价:X>Z>Y
最近更新
- 如图,在平面直角坐标系xOy中,二次函数图象的顶点坐标为(4,﹣3),该图象与x轴相交于点A、B,与y轴相交于点C,其中
- 如你生活在秦朝时期,遇上了当时的一个官吏,你认为这位官吏说的哪些话是可信的①我刚刚拜会了我县的县令②官府用小篆字体发布了
- 斯堪的纳维亚半岛两侧有许多崖壁陡峭、幽深曲折的峡湾,形成原因是( ) A.断裂作用而成 B.冰川作用
- 下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是:A.半导体材料砷化镓
- 在CuSO4中铜元素、硫元素、氧元素的质量比为( ) A.2∶1∶2 B.1∶1∶4 C.4∶2
- 大陆跟台湾真正地一切相同,除了有不同的政治制度。
- 阅读下面诗歌,完成(1)(2)(3)题。 天仙子 张先《水调》数声持酒听,午醉醒来愁未醒。送春春去几时回?临晚镜,伤流景
- “华南虎照片事件”终于尘埃落定,所谓“华南虎照片”系假照片,“拍照人”周正龙涉嫌诈骗被逮捕。下列叙述不符合生物学原理的
- 如图所示为等刻度轻质杠杆,A处挂4牛的物体,若使杠杆在水平位置平衡,则在B处施加力,用力的大小不可能的是
- 先化简,再求值:,其中,.
- 许多人购物和旅游时经常使用信用卡。。信用每作为电子货币的一种,在使用过程中执行的货币职能有
- ((08潍坊))如图所示,是小明同学探究“怎样产生感应电流”的实验装置.ab是一根铜棒,通过导线连接在灵敏电流计的两接线
- 我国古代农耕经济形成南稻北粟局面取决于 A.自然条件 B.政府政策 C.居民口味
- 已知集合 A. B.
- 下列各个句子没有语病的一句是(3分) A.我们仔细调查研究的结果,认为他要负全部责任,但他却百般抵赖,拒不承担由于酒后开
- 一个两位数,个位数字比十位数字大3,个位数字的平方刚好等于这个两位数,则这个两位数是________.
- ()(本小题满分10分) 已知等差数列{}中,求{}前n项和. w.w.w.k.s.5.u.c.o.m
- 下列关于“校园生物调查”的叙述中,不正确的是( ) A.调查生物可不必太注意草丛和落叶里的小生物,只须注意较大的
- 下列词语中没有错别字的一组是( ) A、谛造 矫键 四不像 解铃还须系铃人 B、渲泄 内
- 下列事例中的物态变化,属于液化现象的是 A.从冰箱中取出的冰块化成水 B.冬天,藏眼镜的人从室外进入温暖的室



