卤族与氮族及其应用 知识点题库
下列反应中的氨与反应4NH3 + 5O2 → 4NO + 6H2O中的氨作用相同的是( )
A . 2Na + 2NH3 → 2NaNH2 + H2↑
B . 2NH3 + 3CuO → 3Cu + N2 +3H2O
C . 4NH3 + 6NO → 5N2 + 6H2O
D . 3SiH4 + 4NH3 → Si3N4 + 12H2
已知甲、乙、丙、丁是中学化学常见的物质,一定条件下可发生如图转化:下列相关离子方程式或化学方程式错误的是( )
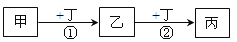
A . ①可能为CH4+Cl2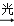 CH3Cl+HCl
B . ①可能为Fe+2Fe3+═3Fe2+
C . ②可能为2NO+O2═2NO2
D . ②可能为CO32﹣+H2O+CO2═2HCO3﹣
CH3Cl+HCl
B . ①可能为Fe+2Fe3+═3Fe2+
C . ②可能为2NO+O2═2NO2
D . ②可能为CO32﹣+H2O+CO2═2HCO3﹣
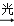 CH3Cl+HCl
B . ①可能为Fe+2Fe3+═3Fe2+
C . ②可能为2NO+O2═2NO2
D . ②可能为CO32﹣+H2O+CO2═2HCO3﹣
CH3Cl+HCl
B . ①可能为Fe+2Fe3+═3Fe2+
C . ②可能为2NO+O2═2NO2
D . ②可能为CO32﹣+H2O+CO2═2HCO3﹣
如图,下列描述不正确的是( )
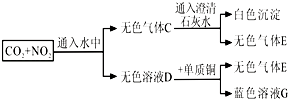
A . C的成分是气体E与二氧化碳的混和气体
B . 浓热的D溶液能把碳单质氧化为二氧化碳
C . 气体E遇空气会被氧化成红棕色的气体
D . 溶液G是蓝色的硫酸铜溶液
从海带中提取碘单质,成熟的工艺流程如下,下列关于海水制碘的说法,不正确的是( )
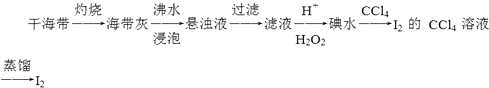
A . 实验室在蒸发皿中灼烧干海带,并且用玻璃搅拌
B . 含I﹣的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C . 在碘水中加入几滴淀粉溶液,溶液变蓝色
D . 碘水中加入CCl4得到I2的CCl4的溶液,该操作为“萃取”
根据要求填空:
-
(1) 实验室里用二氧化锰和浓盐酸加热制取氯化,该反应的离子方程式为.也可以利用反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图甲所示.
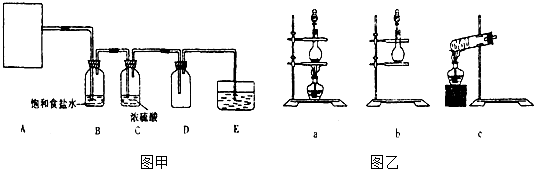
若以KMnO4和浓盐酸为原料制取氯气,则根据反应原理,图乙中合适的制气装置为.
-
(2) 装置B的作用是.
-
(3) 装置E的作用是.E中的试剂可选.
A.NaOH溶液 B.NaCl溶液 B.澄清石灰水 D.水
-
(4) 某同学通过 下列两种方式制取氯气:
①用8.7gMnO2与足量浓盐酸反应;
②用含14.6gHCl的浓盐酸与足量MnO2反应这两种方式产生Cl2的量的关系是 .
A . ①多 B . ②多 C . 一样多 D . 不确定.
下列叙述不正确的是( )
A . NH3易液化,液氨常作制冷剂
B . NO、NO2都是有毒气体
C . 铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处
D . 稀HNO3和活泼金属反应时主要得到氢气
氯的含氧酸根离子有ClO﹣、ClO2﹣、ClO3﹣、ClO4﹣等,有关它们的下列说法正确的是( )
A . ClO﹣中氯元素显+1价,具有很强的还原性
B . 这些离子结合H+的能力,ClO4﹣最强
C . ClO3﹣是NO3﹣的等电子体,其空间构型为平面三角形
D . ClO2﹣、ClO3﹣、ClO4﹣中的氯原子都采取sp3杂化,离子中相邻两个Cl﹣O键间键角依次增大
根据问题填空:
-
(1) 氨气是中学化学中常见气体之一,实验室制取氨气的化学方程式是,氨气的收集方法是,实验室用于干燥氨气的干燥剂是.
-
(2) 下列除杂方法正确的是.
①碳酸氢钠固体中混有碳酸钠,可以用加热的方法除去.
②镁粉中混有少量铝粉,可以用氢氧化钠溶液溶解,然后过滤.
③食盐中混有硫酸钠、氯化镁和氯化钙几种可溶性杂质,可以分别按顺序加入过量的氢氧化钠溶液、碳酸钠溶液、氯化钡溶液,最后用适量盐酸.
④氯气中混有少量氯化氢气体,可以通入饱和食盐水除去.
⑤氯化亚铁溶液中混有氯化铁溶液,加入铜粉除去.
下列有关实验操作、发生的现象、解释或结论都正确的是 ( )
选项 | 实验操作 | 发生的现象 | 解释或结论 |
A | 向亚硫酸钠溶液中,逐滴加入硝酸酸化的硝酸钡溶液 | 产生白色沉淀 | 产生的亚硫酸钡是难溶解入水的沉淀 |
B | 将SO2通入滴有酸性高锰酸钾溶液中 | 溶液紫红色褪去 | SO2具有漂白性 |
C | 常温下铜片插入硝酸中 | 产生红棕色气体 | 常温下铜和硝酸一定产生NO2 |
D | 向某溶液中加入NaHCO3 | 产生白色沉淀 | 该溶液可能原来含有氢氧化钡 |
A . A
B . B
C . C
D . D
化学在生活中有着广泛的应用,下列对应关系错误的是( )
| 选项 | 化学性质 | 实际应用 |
| A | NH3具有还原性 | 用作食品工业的制冷剂 |
| B | K2FeO4易与H2O反应生成Fe(OH)3 | 用作水的消毒剂和絮凝剂 |
| C | Ag2O具有氧化性 | 用作银锌纽扣电池正极的活性物质 |
| D | 硫酸铝能与小苏打溶液反应 | 用作泡沫灭火剂原料 |
A . A
B . B
C . C
D . D
硫酸铜在生产、生活中应用广泛。某化工厂用含少量铁的废铜渣为原料生产胆矾的流程如下:
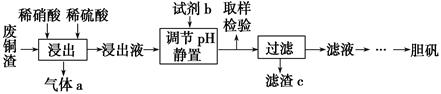
已知生成氢氧化物沉淀的pH如下表所示:
| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀 | 4.2 | 6.5 | 1.5 |
| 完全沉淀 | 6.7 | 9.7 | 3.7 |
-
(1) 写出浸出时铜与稀硫酸、稀硝酸反应生成硫酸铜的化学方程式:。
-
(2) 取样检验是为了确认Fe3+是否除净,你的检验方法是。
-
(3) 试剂b是,滤渣c是(均写化学式)。
-
(4) 气体a可以被循环利用,用化学方程式表示气体a被循环利用的原理为2NO+O2=2NO2、。
-
(5) 一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和O2气体,且n(SO3)∶n(SO2)=1∶2,写出硫酸铜受热分解的化学方程式:。
-
(6) 某同学设计了如下图所示的实验装置分别测定生成的SO2、SO3气体的质量和O2气体的体积。此设计有不合理之处,请说明理由:。
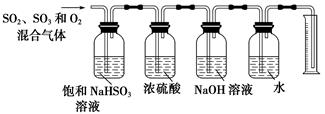
已知氨气极易溶于水,而难溶于有机溶剂CCl4.下列装置中不适宜做氨气的尾气吸收的是( )
A . 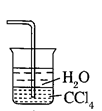 B .
B . 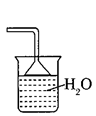 C .
C . 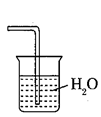 D .
D . 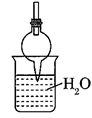
 B .
B .  C .
C .  D .
D . 
卤族元素包括元素,它们原子的最外层都有个电子,在化学反应中易得到个电子,因此均体现出较强的氧化性;但从F到I,电子层数依次增多,原子半径逐渐,原子核对最外层电子的引力逐渐,所以非金属性逐渐,单质的氧化性逐渐。
氮气进入超导试验、麻醉等领域,是应用了氮气性质中的( )
A . 能与氢气反应
B . 高温下能与金属反应
C . 沸点低
D . 密度与空气接近
在含有Fe2+、Fe3+、Al3+、NH4+的溶液中加入足量的Na2O2固体,再加入过量的稀盐酸,完全反应后,离子数目几乎没有改变的是( )
A . Fe2+
B . Fe3+
C . Al3+
D . NH4+
 都是有害气体。在某分子筛的催化作用下,
都是有害气体。在某分子筛的催化作用下,  可脱除废气中的NO和
可脱除废气中的NO和  ,生成两种无害物质,其反应历程如图所示。下列说法错误的是( )
,生成两种无害物质,其反应历程如图所示。下列说法错误的是( ) 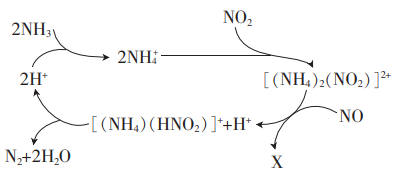
A . X是  和
和 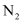 B . 汽车尾气中的氮氧化合物是汽油燃烧产生的
C . NO和CO都能结合血红蛋白,造成人体缺氧
D . 大量排放的NO和
B . 汽车尾气中的氮氧化合物是汽油燃烧产生的
C . NO和CO都能结合血红蛋白,造成人体缺氧
D . 大量排放的NO和  是形成光化学烟雾的一个重要原因
是形成光化学烟雾的一个重要原因
 和
和 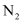 B . 汽车尾气中的氮氧化合物是汽油燃烧产生的
C . NO和CO都能结合血红蛋白,造成人体缺氧
D . 大量排放的NO和
B . 汽车尾气中的氮氧化合物是汽油燃烧产生的
C . NO和CO都能结合血红蛋白,造成人体缺氧
D . 大量排放的NO和  是形成光化学烟雾的一个重要原因
是形成光化学烟雾的一个重要原因
下列现象不能用于检验 的是( )
的是( )
 的是( )
的是( )
A . 气体遇浓盐酸产生白烟
B . 气体使湿润的蓝色石蕊试纸变红
C . 将气体通入酚酞溶液中,溶液变红
D . 气体遇氯气产生白烟
某化学小组制备Cl2并探究Cl2的性质,其装置如下图:
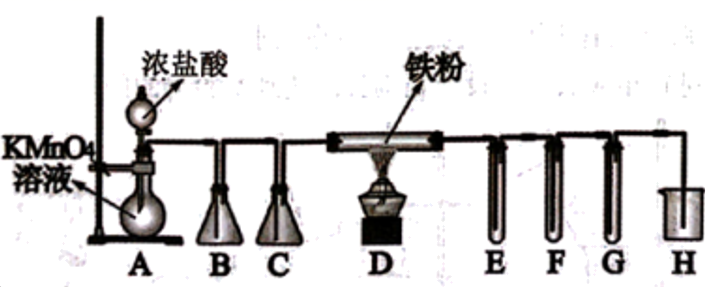
请回答下列问题:
-
(1) A中发生的反应方程式为2KMnO4+16HCl(浓)= 2KCl+5Cl2↑+2MnCl2+8H2O,该反应中氧化剂为,其离子方程式为。
-
(2) 此法制取的Cl2中会混有的杂质气体为和水蒸汽,为了除去杂质,C中所盛放的药品是。
-
(3) 若反应后装置D硬质玻璃管中有Fe粉剩余,将反应后的固体加水振荡,检验溶液中是否含有Fe2+的实验方案是:取少量溶解后的溶液于试管中,滴加少量。若观察到现象,且未见使湿润淀粉KI试纸变蓝的气体,则证明含Fe2+。(可供选择的试剂: KSCN 溶液、KMnO4 稀溶液、NaOH 溶液)
-
(4) E中装有紫色石蕊试液,则E中现象是。
-
(5) F中盛有FeBr2溶液,G中装有NaBr溶液,当G溶液中产生红棕色Br2时,F中发生反应的离子方程式为。
某同学用下列装置制备并检验Cl2的性质。下列说法正确的是( )
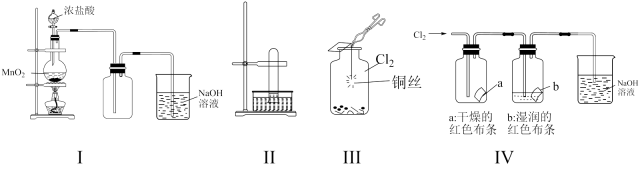
A . I图中:如果MnO2过量,盐酸就可全部消耗
B . II图中:如果倒置的试管充满了氯气,水槽内装满水,经足够长的时间光照,试管内最后剩余气体为氧气
C . III图中:生成蓝色的烟
D . IV图中:a、b中的有色布条褪色,将硫酸溶液滴入烧杯中至溶液呈酸性,结果有Cl2生成
2019年12月以来,我国部分地区突发的新冠病毒肺炎威胁着人们的身体健康。下列有关说法错误的是( )
A . 咳嗽、吐痰、打喷嚏、说话等形成的数以万计的飞沫,直径在1-100nm之间,进入到空气中形成的分散系属于胶体
B . 过氧化氢、活性炭、过氧乙酸等消毒液均可以将病毒氧化而达到消毒的目的
C . “84”消毒液是以NaClO为主要有效成分的消毒液
D . 双氧水分解能产生O2 , 体现了H2O2具有不稳定性
最近更新
- 2014年9月,广东省顺德区继续深入推进农村体制综合改革,在全区推广“手机村务通”建设,创新村务公开方式,扩大社会参与,
- 山西省的煤炭市场十分广阔,不是因为A.我国的能源消费以煤炭为主 B.煤质优良,具有低灰、低硫、低磷、发热量高
- 对“世界市场”含义的正确理解是 ①世界各个国家之间进行货币交往和商品交换的经济活动的总和 ②是伴随着社会
- The Golden Gate Bridge in San Francisco,California is one of
- I can guess you were in a hurry. You your sweater inside o
- 已知函数(注:是自然对数的底数),方程,有四个实数根,则的取值范围为( )A. B. C. D.
- 海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是() A.从海水中可以得到NaCl,电解熔融NaCl可制
- 为探究培养液中酵母菌种群数量的动态变化,某研究性学习小组完成了A、B、C三组 实验。定期对不同培养液中的酵母菌进行计数,
- 园艺师能将一株开单颜色的野菊花培育成具有多种颜色、多个花朵的塔菊,采用的是下列哪项技术
- 雾是近地面大气层中大量微小水滴或冰晶组成的悬浮体。2009年入冬以来,北京遭遇多次大雾天气,有些地区的能见度甚至只有50
- It’shelpful to put children in a situation ____ they can se
- 下列图形中,是轴对称图形的是( ) A. B. C. D.
- 右图中某地蕴藏着丰富的石油、天然气资源,其最可能位于 A.① B.② C.洋盆
- 阅读下列材料,回答问题。 材料1:材料2:1978年和2006年国民经济主要指标比较表 国内生产 总值(亿元) 国家财
- 银锌纽扣电池放电时的反应为:Zn+Ag2O=ZnO+2Ag,下列有关说法中不正确的是 A.该反应属于置换反应
- 下列离子方程式中,正确的是() A.铝溶解在NaOH溶液中:2Al+2OH-+6H2O===2[Al(OH)4]-+3H
- 在总压强为3×105帕下,将氮、氢混和气体通入合成塔,反应达平衡时,按的体积百分含量为20%,平衡时压强为A、1×107
- 如图甲所示,光滑导轨水平放置在与水平方向夹角斜向下的匀强磁场中,匀强磁场的磁感应强度B随时间的变化规律如图乙所示(规定斜
- 我们需要不断更新,不断完善对自己的认识,才能使自己变得更加完美。正确认识自己,就是要做到 A.努力发现自己的优点和长处
- 具有相同电子层结构的三种微粒An+、Bn-、C,下列分析正确的是( ) A.原子序数关系:C>B>A B.



