卤族与氮族及其应用 知识点题库
-
(1) 【观察】氯气的颜色、状态: 状态;闻氯气的气味: 气味.
-
(2) 【预测】氯气是一种非金属单质,它可能具有性质有 从元素化合价的角度分析,它可能具有性质有
-
(3) 【实验探究】
实验内容
实验操作
实验现象
推断生成物
氯气与铁反应
氯气与氢气反应
氯气与碘化钾溶液反应
-
(4) 【实验结论】(1)通过比较氯气和曾经学习过的氧气等非金属单质的性质,可推知氯气的化学性 ,能与 反应.
(2)在上述过程中,该同学都用到了哪些研究物质性质的方法? .
(3)说明闻气体气味的方法.
-
(1) Na3N的电子式 ,该化合物是由 键形成.
-
(2) Na3N与水反应方程式为 ,该反应属 (填基本反应类型)反应.
-
(3) Na3N放入足量盐酸中生成 种盐,其化学式为
-
(4) 比较Na3N中两种粒子的半径:r(Na+) r(N3﹣)(填“>”“=”或“<”)
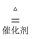 4NO+6H2O
B . 液氨具有腐蚀性和毒性,在使用过程中要防止液氨泄漏
C . 氨气比空气轻,标准状况下密度约为0.76 g•L﹣1
D . 氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全
4NO+6H2O
B . 液氨具有腐蚀性和毒性,在使用过程中要防止液氨泄漏
C . 氨气比空气轻,标准状况下密度约为0.76 g•L﹣1
D . 氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全
请根据以上信息和相关知识回答下列问题:
-
(1) 该“84消毒液”的物质的量浓度为 mol•L﹣1 .
-
(2) 该同学取100mL“威露士”牌“84消毒液”稀释后用于消毒,稀释后的溶液中c(Na+)=mol•L﹣1 . (假设稀释后溶液密度为1.0g•cm﹣3).
下列说法中错误的是:( )
| 实验 | 操作 | |
| A | 除去NaHCO3固体中混有的NH4Cl | 直接将固体加热 |
| B | 实验室收集Cu与稀硝酸反应成的NO | 向上排空气法收集 |
| C | 检验非金属性Cl>C | 在Na2SiO3溶液中加入足量HCl |
| D | 检验某溶液中是否有NH4+ | 取该溶液于干净的试管中,加NaOH浓溶液加热,并用湿润的红色石蕊试纸检验 |
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br2水将I-氧化成IO3- , 除去过量Br2 , 加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2 , 终点时消耗30 mL。
③另取50.00 mL试液,酸化后加入足量K2Cr2O7溶液处理,将释放出的I2和Br2蒸馏收集于含有过量KI的溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的Na2S2O3溶液滴定其中的I2至终点,消耗15.00 mL 。
-
(1) 写出第②步中用Br2水氧化I-的离子方程式:。
-
(2) 第②步除去过量Br2最简单的物理方法是;若未除去过量的Br2 , 对KBr含量测定结果的影响是(填“偏大”“偏小”或“无影响”)。
-
(3) 计算试样中KBr的质量分数(写出计算过程)。
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用洁净的铂丝蘸取待测液在酒精灯火焰上灼烧 | 火焰呈黄色 | 待测液中含Na+ , 不含K+ |
| B | 常温下,将铁片浸入足量浓硝酸 | 铁片不溶解 | 铁与浓硝酸不 反应 |
| C | 向某Na2SO3样品中加入足量Ba(NO3)2溶液,再加入足量稀盐酸 | 先产生白色沉淀,后沉淀不溶解 | Na2SO3已被氧化 |
| D | 将木炭与浓硫酸共热产生的气体依次通入过量的酸性高锰酸钾溶液和澄清石灰水中 | 高锰酸钾溶液紫色变浅,澄清石灰水变浑浊 | 反应产生SO2和CO2 |
-
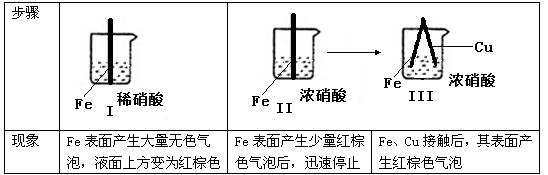
(1) 若A是铁,B是稀硝酸(过量),且A可溶于C溶液中。则铜与C反应的离子方式为。
-
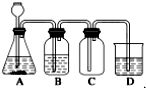
(2) 若C、D均为气体,且都能使澄清石灰水变浑浊,某探究性学习小组利用图中所列装置设计实验,若证明上述反应中有C、D生成。则B瓶溶液的作用是,装置D中所盛溶液是。
-
(3) 若C是无色有刺激性气味的气体,其水溶液呈弱碱性。用电离方程式解释其水溶液呈弱碱性的原因。
-
(4) 若A为黄绿色有刺激性气味的有毒气体,C、D焰色反应为黄色,则上述的反应的离子方程式为。A气体能使湿润的石蕊试纸(填写现象)
-
(5) 若A为铜,C能使品红溶液褪色,则上述的反应的化学方程式为。
 )、氯化亚砜(
)、氯化亚砜( 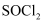 )常作氯化剂,用于制造药品、染料和表面活性剂。它们部分性质如下:
)常作氯化剂,用于制造药品、染料和表面活性剂。它们部分性质如下: | 物理性质 | 化学性质 | |
| | 熔点:-54.1℃ 沸点:69.1℃ | ①100℃分解生成 ②遇水蒸气产生大量白雾 |
| | 在空气中遇水蒸气发生剧烈反应,产生大量白雾 |
实验室合成  的原理:
的原理:  。某小组设计实验如图所示(夹持仪器已省略):
。某小组设计实验如图所示(夹持仪器已省略):
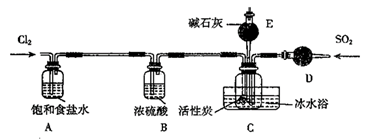
回答下列问题:
-
(1) D中试剂是 ,活性炭的作用是 ;
-
(2) 实验室常用高锰酸钾固体与浓盐酸在常温下反应制氯气,写出反应的离子方程式 ;
-
(3) 实验室用
 粉末与75%的浓硫酸反应制备
粉末与75%的浓硫酸反应制备  ,发现产生
,发现产生  很少,可能的原因是 ;
很少,可能的原因是 ;
-
(4) E中碱石灰的作用是 ;
-
(5) 氯化亚砜遇水蒸气发生反应的化学方程式是 ;实验室蒸干
 溶液不能得到无水
溶液不能得到无水  ,但是
,但是 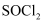 和
和  混合物加热,可得到无水
混合物加热,可得到无水  ,其主要原因是 ;
,其主要原因是 ;
-
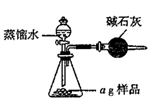
(6) 为了测定
 产品纯度(杂质不参与反应),称取a g
产品纯度(杂质不参与反应),称取a g  产品于锥形瓶中(如图所示),向锥形瓶中加入足量蒸馏水,充分反应后,用c
产品于锥形瓶中(如图所示),向锥形瓶中加入足量蒸馏水,充分反应后,用c 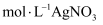 溶液滴定至终点(滴几滴
溶液滴定至终点(滴几滴  溶液作指示剂),消耗
溶液作指示剂),消耗 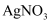 溶液为V mL。
溶液为V mL。 ①用棕色滴定管盛装
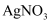 溶液,其原因是 ;
溶液,其原因是 ;②该
 产品的纯度为 ;
产品的纯度为 ;③实验中,控制分液漏斗活塞,缓慢滴加水,避免氯化氢挥发。如果操作时滴加水过快,测得结果 (填“偏高”“偏低”或“无影响”)。
- “创新是一个民族的灵魂。”中国作为一个历史悠久的国家,政治制度多有创新,而且体系完备、影响深远。 材料一 自古至周天下
- 下列含氧酸的酸酐,不能由单质跟氧气直接化合得到的是 A.H2SO3 B.H2CO3
- 一个已充电的电容器,若使它的电量减少3×10-4C,则其电压减少为原来的1/3,则 ( ) A.电容器原来的带电
- 物体在地面附近绕地球做圆周运动时的速度就叫做第一宇宙速度。关于第一宇宙速度,下列说法正确的是( ) A.第一
- 如图所示是一些准备用来测量待测电阻Rx阻值的实验器材,器材及其规格列表如下:器材 规格 待测电阻RX 阻值在900至10
- 根据汉语提示翻译完成下列句子。 1. 如果迟到了点,也没有关系.It’s OK if you _____ ______
- 已知纳米材料是指粒子直径在1~100nm的材料。美国IBM 制造出了第一批纳米碳管晶体管,发明了利用电子的波性为传递信息
- 在过去三年里,我们对待考试成绩既有欢呼,也有难过。下列关于对考试和分数的态度不正确的是 ( ) A.既要重视考试,关
- 下列命题:①幂函数中不存在既不是奇函数又不是偶函数的函数;②图象不经过点的幂函数一定不是偶函数;③如果两个幂函数的图象具
- 下图为某种群数量增长的“J”型曲线和“S”型曲线。若不考虑迁入和迁出,下列有关叙述错误的是()A.改善空间和资源条件有望
- 4.端粒是真核生物染色体末端的一种特殊结构,主要由特定的DNA序列与蛋白质构成,其主要生物学功能是保证染色体末端完整复制
- 下列关于利用细胞工程技术制备单克隆抗体的叙述,不正确的是( ) A.给小鼠注射抗原,是为了获得能产生相应抗体的B细
- (6分)某学生用打点计时器研究小车的匀变速直线运动。他将打点计时器接到频率为50Hz的交流电源上,实验时得到一条如图所示
- 下列各组固体物质,只用水不能进行鉴别的是( )A.K2SO4、KClB.CaCO3、Na2CO3C.CaO、Ca
- 下列对于废弃塑料制品的处理方法中,最为恰当的是( )A.将废弃物切成碎片,混在垃圾中填埋于土壤中B.将废弃物焚烧C
- Why doAmericans struggle with watching their weight, while t
- 某种生物甲植株的基因型是YyRr,甲与乙植株杂交,按自由组合定律遗传,他们的杂交后代表现型比值是3:3:1:1,则乙的基
- They are ________to fail if theycontinue at the risk of all
- 某国生产一件K商品的社会必要劳动时间为1小时,甲企业生产一件K商品所需的个别劳动时间为1.5小时,如果甲企业劳动生产率提
- 做铁丝在氧气里燃烧的实验时,预先在集气瓶里装少量水或细沙,其主要作用是 A.防止瓶底炸裂 B.降低瓶




