常见元素的化合价 知识点
常见元素的化合价:元素化合价是由一定元素的原子构成的化学键的数量。正常口诀: 一价钾钠氢和银;二价铜钙钡镁锌;三价铝铁四价硅;负一为氯负二氧。
常见元素的化合价 知识点题库
实验室中可用KMnO4来制取氧气.KMnO4中锰元素的化合价为( )
A . +7
B . +5
C . +3
D . ﹣7
下列元素中,最高正化合价数值最大的是( )
A . Na
B . P
C . S
D . C
金属A的氧化物分子式为A2O3 , 则A的化合价为 ,A的硝酸盐的化学式为
请指出氧在下列各物质中的化合价.
O3;Na2O2;Na2O.
在水溶液中YOn﹣3与S2﹣发生反应的离子方程式如下:YOn﹣3+3S2﹣+6H+=Y﹣+3S↓+3H2O,则YOn﹣3中Y元素的化合价和Y元素原子的最外层电子数分别是( )
A . +5、4
B . +5、7
C . +5、5
D . +7、7
硼的原子序数是5,硼的最高价氧酸的化学式不可能是( )
A . HBO2
B . H3BO3
C . H2BO3
D . H4B2O5
下列元素中,最高正化合价数值最大的是( )
A . C
B . F
C . S
D . Ne
下列元素中最高正化合价为+7价的是( )
A . Cl
B . H
C . N
D . He
元素周期表中ⅣA元素包括C、Si、Ge、Sn、Pb等,已知Sn的+4价稳定,而Pb的+2价稳定。结合所学知识,判断下列反应中(反应条件略)正确的是( )
①Pb+2Cl2=PbCl4 ②Sn+2Cl2=SnCl4 ③SnCl2+Cl2=SnCl4
④PbO2+4HCl=PbCl4+2H2O ⑤Pb3O4+8HCl=3PbCl2+Cl2↑+4H2O
A . ②③⑤
B . ②③④
C . ①②③
D . ①②④⑤
2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。下列叙述不正确的是( )
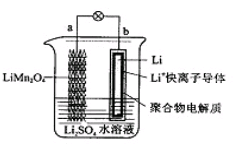
A . a为电池的正极
B . 电池充电反应为LiMn2O4=Li1-xMn2O4+xLi
C . 放电时,a极锂的化合价发生变化
D . 放电时,溶液中Li+从b向a迁移
下列元素中,最高正化合价数值最大的是( )
A . C
B . F
C . S
D . Na
某科研团队研究发现硼氢化钠(NaBH4)在催化剂Ru表面与水反应可生成H2 , 其反应机理如图所示:
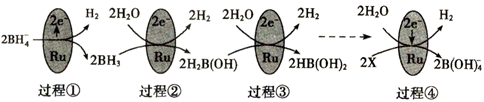
根据以上信息判断,下列叙述错误的是( )
A . 过程①至过程④中硼元素的化合价不变
B . X是H3BO3 , H3BO3和BH3两分子中H的化合价相等
C . 过程③和过程④各产生1molH2时转移的电子数不相等
D . 0.25molNaBH4的还原能力与标准状况下22.4LH2的还原能力相当(还原能力即生成H+失去电子的量)
元素铬的几种化合物存在下列转化关系:
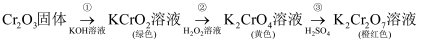 已知:2CrO
已知:2CrO  +2H+⇌Cr2O
+2H+⇌Cr2O 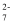 +H2O。下列判断错误的是( )
+H2O。下列判断错误的是( )
A . 反应①表明Cr2O3有酸性氧化物的性质
B . 反应②利用了H2O2的氧化性
C . 反应③中溶液颜色变化是由化学平衡移动引起的
D . 反应①②③中铬元素的化合价均发生了变化
最近我国科研人员发现了一种安全高效的点击化学试剂FSO2N3 , 下列有关元素F、S、O、N的说法正确的是( )
A . 基态s原子价电子轨道表示式: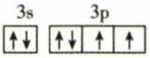 B . 第一电离能:F>S>O>N
C . 最高正价:F>S=O>N
D . S原子的基态原子核外未成对电子数最多
B . 第一电离能:F>S>O>N
C . 最高正价:F>S=O>N
D . S原子的基态原子核外未成对电子数最多
 B . 第一电离能:F>S>O>N
C . 最高正价:F>S=O>N
D . S原子的基态原子核外未成对电子数最多
B . 第一电离能:F>S>O>N
C . 最高正价:F>S=O>N
D . S原子的基态原子核外未成对电子数最多
三氟化氮(NF3)是一种无色无味的气体,它由氨气(NH3)和氟气(F2)在一定条件下直接反应得到:4NH3+3F2=NF3+3NH4F。下列有关NF,的叙述中错误的是( )
A . NF3是一种极性分子
B . NF3提供孤电子对的能力比NH3强
C . NF3中的N呈+3价
D . NF3中的N原子采取sp'杂化成键
科学家研制出了一种漂白效率极高的新型漂白剂结构如图,W、X、Y、Z均为原子序数依次增大的短周期元素。常温下,0.1mol·L-1Z的氢化物的水溶液pH=1,且Z与Y位于不同周期。下列叙述正确的是( )
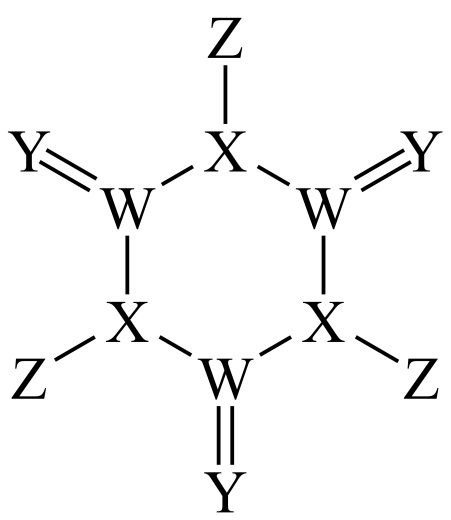
A . XY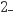 中X原子的杂化方式为sp3
B . 在此物质中Z的化合价应为+1价
C . WY2分子中σ与π键之比为1:2
D . 原子半径:Z>Y>X
中X原子的杂化方式为sp3
B . 在此物质中Z的化合价应为+1价
C . WY2分子中σ与π键之比为1:2
D . 原子半径:Z>Y>X
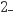 中X原子的杂化方式为sp3
B . 在此物质中Z的化合价应为+1价
C . WY2分子中σ与π键之比为1:2
D . 原子半径:Z>Y>X
中X原子的杂化方式为sp3
B . 在此物质中Z的化合价应为+1价
C . WY2分子中σ与π键之比为1:2
D . 原子半径:Z>Y>X
草酸( )是一种常用的化工原料,能形成多种化合物,其中草酸钠是一种常用的化工还原剂,草酸钙可用于陶瓷上釉等,回答下列问题:
)是一种常用的化工原料,能形成多种化合物,其中草酸钠是一种常用的化工还原剂,草酸钙可用于陶瓷上釉等,回答下列问题:
 )是一种常用的化工原料,能形成多种化合物,其中草酸钠是一种常用的化工还原剂,草酸钙可用于陶瓷上釉等,回答下列问题:
)是一种常用的化工原料,能形成多种化合物,其中草酸钠是一种常用的化工还原剂,草酸钙可用于陶瓷上釉等,回答下列问题:
-
(1)
 中C元素的化合价为。
中C元素的化合价为。
-
(2) 某同学用酸性
 溶液滴定含杂质的
溶液滴定含杂质的 测定样品的纯度(已知杂质不参与反应),实验步骤如下:
测定样品的纯度(已知杂质不参与反应),实验步骤如下:准确称取1g
 固体样品,配成
固体样品,配成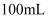 溶液,取出
溶液,取出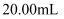 于锥形瓶中,再向锥形瓶中加入足量稀
于锥形瓶中,再向锥形瓶中加入足量稀 溶液,用
溶液,用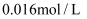 高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液
高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液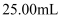 。
。①高锰酸钾溶液应装在滴定管中,滴定至终点时的实验现象是。
②下列操作可能使测量结果偏低的是。
a.盛装的
 的滴定管没润洗
的滴定管没润洗b.称取的
 样品部分含有结晶水
样品部分含有结晶水c.读数时滴定前俯视,滴定后仰视
d.滴定结束后滴定管尖端悬有一滴溶液
③计算样品中
 的纯度。
的纯度。 -
(3)
 是五种肾结石里最为常见的一种,患草酸钙结石的病人多饮白开水有利于结石的消融,请用必要的化学原理和简要的文字说明其原因。
是五种肾结石里最为常见的一种,患草酸钙结石的病人多饮白开水有利于结石的消融,请用必要的化学原理和简要的文字说明其原因。
K2FeO4具有强氧化性,酸性条件下,其氧化性强于Cl2、KMnO4 , 其制备的流程如下:
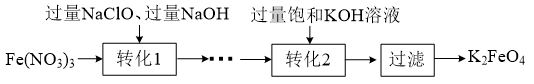
已知:K2FeO4能溶于水,微溶于浓KOH溶液,“转化1”时有 生成。下列有关说法正确的是( )
生成。下列有关说法正确的是( )
A . K2FeO4中铁元素的化合价是+3
B . “转化1”发生反应的离子方程式为:2Fe3++3ClO-+5H2O=2 +3Cl-+10H+
C . “转化2”能进行的原因是该条件下K2FeO4的溶解度比Na2FeO4小
D . 所得滤液含有大量的Na+、H+、
+3Cl-+10H+
C . “转化2”能进行的原因是该条件下K2FeO4的溶解度比Na2FeO4小
D . 所得滤液含有大量的Na+、H+、 、Cl-
、Cl-
 +3Cl-+10H+
C . “转化2”能进行的原因是该条件下K2FeO4的溶解度比Na2FeO4小
D . 所得滤液含有大量的Na+、H+、
+3Cl-+10H+
C . “转化2”能进行的原因是该条件下K2FeO4的溶解度比Na2FeO4小
D . 所得滤液含有大量的Na+、H+、 、Cl-
、Cl-
一种从含砷废水[砷主要以亚砷酸(H3AsO3)形式存在]中回收砷的工艺流程如图:
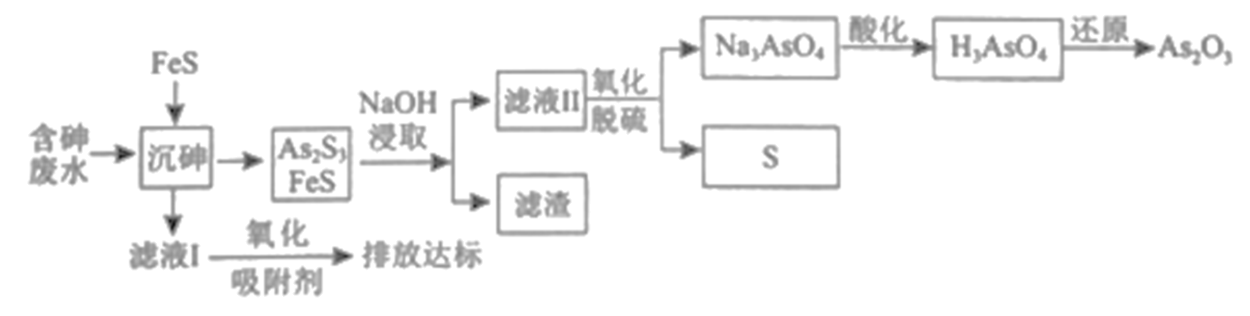
已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq)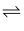 2AsS
2AsS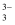 (aq)
(aq)
III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是( )
A . As2S3中砷元素的化合价为+3价
B . “沉砷”过程中FeS可以用过量的Na2S代替
C . 用氧气进行“氧化脱硫”涉及离子方程式AsS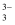 +2O2=AsO
+2O2=AsO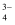 +3S↓
D . 能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸
+3S↓
D . 能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸
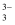 +2O2=AsO
+2O2=AsO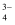 +3S↓
D . 能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸
+3S↓
D . 能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸
某元素原子最外层比次外层多5个电子,该元素的最高正化合价为( )
A . +5
B . +6
C . +7
D . 无最高正化合价
最近更新
- 在一定温度下,下列叙述不是可逆反应A(气)+3B(气)2C(气)+2D(固)达到平衡的标志的是 ①C的生成速率与C的分解
- 我国古代推动农业生产发展的重要因素不包括( )A、生产工具的改进
- 下列句子标点符号使用正确的一项目( )A、我国古人早已认识到:“人性善恶可变”,关键在教育。B、“哎!”陈红忽然
- 南极洲的象征是( )A.北极熊B.企鹅C.袋鼠D.大象
- 下列叙述中不正确的是( ) A.癌细胞一般能不断合成蛋白质和产生中心粒 B.生物的卵细胞虽然分化程度很高,但仍然具有较
- —— What do you think of the concert?—— Oh, it was______succe
- 由受精卵发育而来的雌蜂(蜂王)是二倍体(2n=32),由未受精的卵细胞发育而来的雄蜂是单倍体(n=16)。下列相关叙述正
- 下图以及《人民日报》报道“小麦亩产12万斤”“水稻亩产3万斤”“一棵白菜500千”的好消息。这些现象发生在( )。
- 阅读下面短文,掌握其大意,然后从方框中选出能填入文中空白处的最合适的单词,并将该单词的标号(A、B、C、D、E…)填写在
- As parents,it is wrong to ____________ your children when th
- 蚕豆根尖细胞在含3H标记的胸腺嘧啶脱氧核苷培养基中完成一个细胞周期,然后在不含放射性标记的培养基中继续分裂至中期,其染色
- —Doyou know if it______ tomorrow? —I hope it won’t . If
- (4分)在杨氏双缝干涉实验装置中,双缝的作用是A.遮住过于强烈的灯光B.形成两个振动情况相同的光源C.使白光变成单色光D
- 囊泡可用来运输和消化细胞产物。以下对囊泡的叙述错误的是 A.囊泡的转移有利于膜成分的更新 B.囊泡可把内质网加工的蛋白质
- 如图,菱形ABCD的边长为2,∠A=60°,点P和点Q分别从点B和点C出发,沿射线BC向右运动,且速度相同,过点Q作QH
- 在电场中( )A.某点的电场强度大,该点的电势一定高B.某点的电势高,检验电荷在该点的电势能一定大C.某点的场强为
- 一定量甲烷燃烧后的产物为CO、CO2和水蒸汽,此三种混合气体的质量为28.8g.当混合气体缓缓通过足量的无水氯化钙后,增
- 下列图标所示的国际和区域性经济组织中,中国加入的有 ①
- 费正清在《中国:传统与变迁》中指出:“理学并不仅仅是前秦和两汉儒学的继承和发展。它部分是对传统的重新发展,部分是全新的创
- 下图示意日本本州岛部分地区樱花初放日期,回答3-5题。3.导致该岛滨海地区樱花初放日期自南向北变化的主要因素是 A.地形



