工业合成氨 知识点题库
-
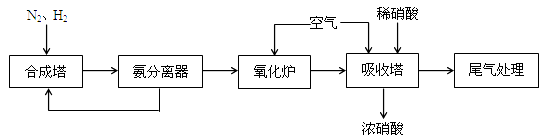
(1) N2约占空气体积的,从空气中分离出N2利用的原理是。
-
(2) 合成塔中发生反应的化学方程式是,该反应中的氧化剂是。22.4LN2(标准状况)完全反应时,转移电子的物质的量是。
-
(3) 氧化炉中发生反应的化学方程式是。
-
(4) 吸收塔中通入空气的作用是。
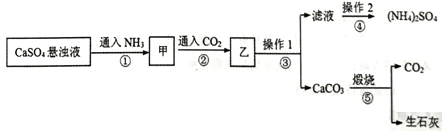
下列说法正确的是()
 2NH3。起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。
2NH3。起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。 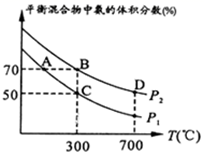
①恒压时,反应一定达到平衡状态的标志是(填序号)
A.N2和H2的转化率相等 B.反应体系密度保持不变
C.  保持不变 D.
保持不变 D. 
②该反应的平衡常数表达式K=,∆H。
③比较大小:P1P2 , 理由是
④平衡时B、D两点的正反应速率:υ(B)υ(D)。(填“<”或“>”或“=”)
-
(1) 氨气分解反应的热化学方程式如下:2NH3(g)
 N2(g)+3H2(g) ΔH
N2(g)+3H2(g) ΔH 若:N≡N键、H-H键和N-H键的键能分别记作a、b和c(单位:kJ·mol−1),则上述反应的ΔH=kJ·mol-1。
-
(2) 研究表明金属催化剂可加速氨气的分解。下表为某温度下等质量的不同金属分别催化等浓度氨气分解生成氢气的初始速率(mmol·min−1)。
催化剂
Ru
Rh
Ni
Pt
Pd
Fe
初始速率
7.9
4.0
3.0
2.2
1.8
0.5
①不同催化剂存在下,氨气分解反应活化能最大的是(填写催化剂的化学式)。
②温度为T,在一体积固定的密闭容器中加入2 mol NH3 , 此时压强为P0 , 用Ru催化氨气分解,若平衡时氨气分解的转化率为50%,则该温度下反应2NH3(g)
 N2(g)+3H2(g)用平衡分压代替平衡浓度表示的化学平衡常数Kp=。[已知:气体分压(p分)=气体总压(p总)×该气体的物质的量分数]
N2(g)+3H2(g)用平衡分压代替平衡浓度表示的化学平衡常数Kp=。[已知:气体分压(p分)=气体总压(p总)×该气体的物质的量分数] -
(3) 关于合成氨工艺的理解,下列正确的是________。A . 合成氨工业常采用的反应温度为500℃左右,可用勒夏特列原理解释 B . 使用初始反应速率更快的催化剂Ru,能提高平衡时NH3的产量 C . 合成氨工业采用10 MPa~30 MPa,是因常压下N2和H2的转化率不高 D . 分离空气可得N2 , 通过天然气和水蒸气转化可得H2 , 原料气须经过净化处理,以防止催化剂中毒和安全事故发生
-
(4) 恒温条件下,在一体积固定的密闭容器中加入1mol N2和3mol H2 , 用Ru催化合成NH3 , NH3的体积分数随时间变化如图所示。保持其它条件不变,在t1时刻,再加入一定量物质的量之比为1∶3的N2和H2 , t2时刻重新达到平衡。画出t1~t3时刻NH3体积分数的变化趋势。
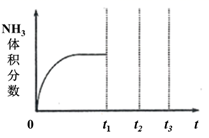
-
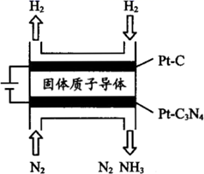
(5) 电化学法也可合成氨。如图是用低温固体质子导体作为电解质,用Pt−C3N4作阴极催化剂电解H2(g)和N2(g)合成NH3的原理示意图,Pt−C3N4电极反应产生NH3的电极反应式。
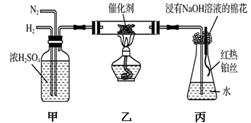
 ,说明直接发生反应NH3+2O2
,说明直接发生反应NH3+2O2 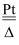 HNO3+H2O
HNO3+H2O
回答下列问题:
-
(1) I.合成氨反应的机理研究:N2和H2在活性铁表面催化合成NH3的机理如图所示,其中(ad)表示物种的吸附状态。
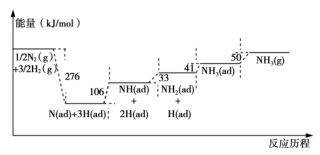
根据反应历程图,写出合成氨反应的热化学方程式。
-
(2) 合成氨经历如下五个过程:
 N2(g)+
N2(g)+ 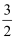 H2(g)→N(ad)+3H(ad)i
H2(g)→N(ad)+3H(ad)iN(ad)+3H(ad)→NH(ad)+2H(ad)ii
NH(ad)+2H(ad)→NH2(ad)+H(ad)iii
NH2(ad)+H(ad)→NH3(ad)iv
NH3(ad)→NH3(g)V
下列说法正确的是___________(填选项字母)。
A . 升高温度,过程i的反应速率减慢,过程ii的反应速率加快 B . 增大压强,有利于提高过程i的转化率 C . 使用催化剂时,反应 N2(g)+
N2(g)+ 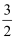 H2(g)→N(g)+3H(g)ΔH<0
H2(g)→N(g)+3H(g)ΔH<0
-
(3) II.合成氨反应的反应条件研究:实验测定不同条件下,平衡时氨气的含量与起始氢氮比[
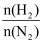 ]之间的关系如图所示。
]之间的关系如图所示。 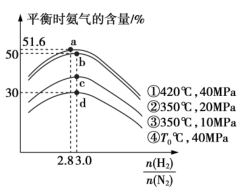
T0420℃(填“<”“>”或“=”,下同)。
-
(4) a点时的转化率:a(N2)a(H2)。
-
(5) a、b、c、d四点对应的平衡常数由大到小的顺序为(用Ka、Kb、Kc、Kd表示)。
-
(6) b点对应的平衡常数Kb=MPa-2(用体系中各物质的分压表示平衡常数,物质的分压=物质的量百分含量×容器的总压,列出计算式即可)。
III.合成氨的工业化研究:合成氨的原料气中的杂质会影响氨的合成效率,已知某原料气中含有20%N2、40%H2、30%CO、3%Ar。
-
(7) 在恒压条件下,单位时间通入的气体总量一定时,杂质稀有气体Ar会使N2的平衡转化率降低的原因为。
-
(1) 实验室制取氨气的化学原理是(用化学方程式表示),验满方法是。
-
(2) 已知:N2(g)+3H2(g)
 2NH3(g) △H=-92kJ·mol-1 , 工业合成氨温度选择700K的原因是。
2NH3(g) △H=-92kJ·mol-1 , 工业合成氨温度选择700K的原因是。
-
(3) 利用NH3处理硝酸工业尾气中的NOx , 将其转化为无毒物质,该反应的化学方程式为。
-
(4) 水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图:
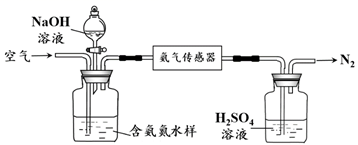
①利用平衡原理分析含氨氮水样中加入NaOH溶液的作用。
②若利用氨气传感器将1L水样中的氨氮完全转化为N2时,转移电子的物质的量为3.9×10-4mol,则水样中氨氮(以氨气计)含量为mg·L-1。
-
(5) 联氨(N2H4)为二元弱碱,在水中的电离方式与氨类似。25℃时,联氨的电离常数Kb1=3×10-6mol·L-1 , Kb2=7.6×10-15mol·L-1。联氨和盐酸按物质的量之比1∶1反应的离子方程式是,所得溶液呈性(填“酸”、“中”或“碱”)。
-
(1) 氨气分解反应的热化学方程式如下:2NH3(g)
 N2(g)+3H2(g)ΔH。若:N
N2(g)+3H2(g)ΔH。若:N  N键、H—H键和N—H键的键能值分别记作a、b和c(单位,kJ•mol-1),则上述反应的ΔH=(用含(a、b、c的代数式表示)kJ•mol-1。
N键、H—H键和N—H键的键能值分别记作a、b和c(单位,kJ•mol-1),则上述反应的ΔH=(用含(a、b、c的代数式表示)kJ•mol-1。
-
(2) 研究表明金属催化剂可加速氨气的分解。某温度下,用等质量不同金属分别催化等浓度的氨气,测得氨气分解生成氢气的初始速率(单位mmol•min-1)与催化剂的对应关系如表所示。
催化剂
Ru
Rh
Ni
Pt
Pd
Fe
初始速率
7.9
4.0
3.0
2.2
1.8
0.5
①在不同催化剂的催化作用下,氨气分解反应的活化能最大的是(填写催化剂的化学式)。
②温度为T时.在恒容的密闭容器中加入2molNH3此时压强为p0用Ru催化氨气分解,若平衡时氨气的转化率为50%.,则该温度下反应2NH3(g)
 N2(g)+3H2(g)的化学平衡常数Kp=。(用平衡分压代替平衡浓度计算,气体分压p分=气体总压P总×体积分数)
N2(g)+3H2(g)的化学平衡常数Kp=。(用平衡分压代替平衡浓度计算,气体分压p分=气体总压P总×体积分数) -
(3) 关于合成氨工艺的理解,下列说法错误的是____________(填字母)。A . 合成氨工业常采用的反应温度为500℃左右,主要是为了节约能源 B . 使用初始反应速率更快的催化剂Ru.,不能提高平衡时NH3的产率 C . 合成氨工业采用的压强为10MPa~30MPa,是因为常压下N2和H2的转化率不高
-
(4) 电化学法合成氨:利用低温固体质子导体作电解质,用Pt—C3N4作阴极,催化电解H2(g)和N2(g)合成NH3原理示意如图所示。
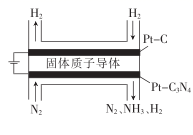
①Pt—C3N4 , 电极上产生NH3的电极反应式为。
②实验研究表明,当外加电压超过一定值后,发现阴极产物中氨气的体积分数随着电压的增大而减小,分析其可能原因:。
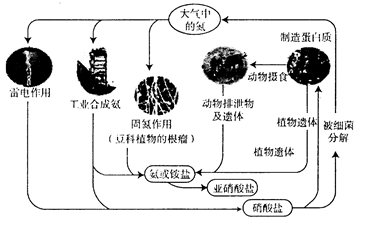
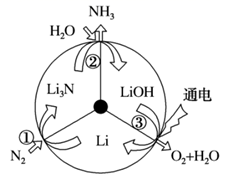
 发生了氧化反应
B . 反应①和②均属于“氮的固定”
C . 反应③为
发生了氧化反应
B . 反应①和②均属于“氮的固定”
C . 反应③为 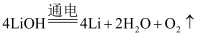 D . 三步循环的总结果为
D . 三步循环的总结果为 
-
(1) 下列有关获取原料气的说法正确的是___________。A . 可通过液化空气分离法得到氮气 B . 可用煤、天然气与水蒸气反应制备水煤气,进而获取氢气 C . 原料气需经净化处理以防催化剂中毒 D . 电解水法获取氢气是一种较为廉价且高效的方法
-
(2) 原料气中的杂质气体H2S可用过量氨水净化吸收,写出化学反应方程式。
-
(3) 工业生产中氮气与氢气按物质的量之比为1:2.8进行投料,合成塔压强p恒定。若起始时氮气通入量为xmol,一段时间后测得氮气的平衡转化率为80%,用平衡分压代替平衡浓度表示平衡常数的KP=(用p表示,气体分压=总压ⅹ物质的量分数)
-
(4) 据统计,每年全世界在合成氨工业中向外排放CO2高达40亿吨,为循环使用CO2减少浪费,常见的方法是利用合成氨的产品NH3和副产品CO2合成尿素:
①2NH3(g)+CO2(g)
 NH2COONH4(l)
NH2COONH4(l) 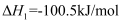 Ea1
Ea1②NH2COONH4(l)
 CO(NH2)2(l)+H2O(l)
CO(NH2)2(l)+H2O(l) 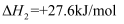 Ea2
Ea2副反应:NH2COONH4+H2O=(NH4)2CO3
已知活化能大小:Ea1<<Ea2
某科研小组模拟工业合成尿素生产,发现反应温度在140℃时生成尿素的反应速率反而比80℃小,可能原因是。
-
(5) 工业合成尿素中,通常氨碳投料比大于2,请分析可能原因___________。A . 氨易获得,成本较低 B . 氨过剩可提高二氧化碳的转化率,加快合成速率 C . 氨气可与体系内水结合,减少氨基甲酸铵水解,抑制副反应发生 D . 氨结合水,促进反应②正向移动
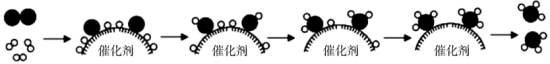
下列说法正确的是( )
 表示氢气分子
B . 过程中有“NH”“NH2”原子团生成
C . 催化剂增大了氢气的平衡转化率
D . 反应结束后催化剂的质量增加
表示氢气分子
B . 过程中有“NH”“NH2”原子团生成
C . 催化剂增大了氢气的平衡转化率
D . 反应结束后催化剂的质量增加
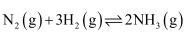 ,
, 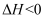 , 下列关于合成氨工业的说法不正确的是( )
, 下列关于合成氨工业的说法不正确的是( )
-
(1)
 的结构式是。
的结构式是。 常用作粮食、瓜果的保护气,其主要原因是。
常用作粮食、瓜果的保护气,其主要原因是。
-
(2) 目前工业合成氨的原理是
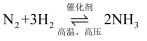 , 该反应正反应为放热反应。下列催化剂措施中,能加快该反应的化学反应速率的是____(填标号)。
A . 其他条件不变,适当增大
, 该反应正反应为放热反应。下列催化剂措施中,能加快该反应的化学反应速率的是____(填标号)。
A . 其他条件不变,适当增大 的浓度
B . 其他条件不变,降低反应体系的温度
C . 其他条件不变,减小反应体系的压强
D . 其他条件不变,使用更高效的催化剂
的浓度
B . 其他条件不变,降低反应体系的温度
C . 其他条件不变,减小反应体系的压强
D . 其他条件不变,使用更高效的催化剂
-
(3) 三元催化器是汽车排气系统重要的机外净化装置,可同时将碳氢化合物、一氧化碳和氮氧化物(
 )三种污染物转化为无害物质,其工作原理如下图所示。反应过程中被氧化的元素名称是。若
)三种污染物转化为无害物质,其工作原理如下图所示。反应过程中被氧化的元素名称是。若 为
为 , 则写出
, 则写出 和
和 反应的化学方程式为。
反应的化学方程式为。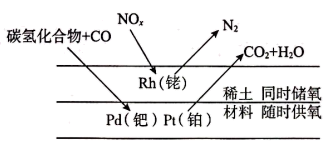
-
(4) 某汽车安全气囊的气体发生剂主要含有叠氮化钠(
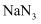 )、氧化铁、高氯酸钾、碳酸氢钠等物质。
)、氧化铁、高氯酸钾、碳酸氢钠等物质。①其中叠氮化钠是气体发生剂,受撞击时产生氮气和金属钠。若该反应生成67.2L(标准状况下)氮气时,转移电子的物质的量为
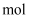 。
。②高氯酸钾是助氧化剂,在反应过程中与金属钠作用生成氯化钾和氧化钠。鉴别高氯酸钾中钾元素的实验操作及现象为。
- 18.下列各句中没有语病的一句是 ( ) A 美韩两国防务部门当日发表联合声明,正式宣布决定在驻韩美军部署“萨德
- 已知函数,若的最小值为,则实数的取值范围是_________
- 宇宙飞船在半径为R1的轨道上运行,变轨后的半径为R2,R1>R2,宇宙飞船绕地球做匀速圆周运动,则变轨后宇宙飞船的
- 化学与生产生活密切相关,现有①纯碱 ②盐酸 ③熟石灰.(填序号) (1)胃液中含有的物质 (2)可用于生产洗涤剂的物
- Only when I left my parents for Italy______ how much I loved
- 生态系统一般都包括:A.生产者和非生物部分 B.消费者和非生物部分 C.生产者,消费者和分解者 D.生产者、消费者,分解
- 长江中下游平原与四川盆地的大致界线是( ) A.秦岭 B.大别山
- 设{an}是等比数列,给出下列四个命题: ①{}是等比数列; ②{an+1}是等比数列; ③是等比数列; ④{
- 实验室制氨气通常有三种方法:①用固体氢氧化钙和氯化铵反应(装置同课本);②称取7.9 g碳酸氢铵固体放入试管内,再加入8
- F为椭圆的一个焦点,若椭圆上存在点A使为正三角形,那么椭圆的离心率为 。
- 用化学用语填空: (1)4个氧分子 ; (2)2个氮原子 ; (3)镁
- 如图右所示,将两个铅柱的底面削平、削干净,然后紧紧地压在一起,两铅块就会结合起来,甚至下面吊一个钩码都不能把它们拉开.这
- 国务院把清明、端午、中秋等传统节日列为国家法定假日,对传统节日文化进行了科学、有效的重构与再创造,使之有机“长入”今日的
- 设平面内有n个圆两两相交,且没有三个或三个以上的圆相交于同一点,它们把平面分成的区域数为p(n),如果该平面内再增一个符
- 与我国新疆接界的邻国分别属于A.西亚、中亚地区B.西亚、中亚、东亚、南亚地区C.西亚、东亚、北亚地区D.西亚、中亚、东亚
- 光滑斜面的长度为L,一物体自斜面顶端由静止开始匀加速滑至底端,经历的时间为t,则错误的是:( )A.物体运动全
- 化学是研究物质的结构、性质以及变化规律的科学,研究元素知识是学好化学的基础。下表包含部分元素的相关信息,完成以下填空:(
- 对右表中历史现象起直接推进作用的是A.辛亥革命 B.抗日战争的胜利结束 C.南京解放 D.中华人民共和国成立
- 对亚马孙流域这片全球最大的热带雨林的前景,正确的说法是 A.面对雨林正在遭受毁灭性破坏的严峻形势,应该把保护放在首位
- 下列关于物质的性质和用途说法正错误的是( ) A.石墨有滑腻感,可以做电极 B



