酸碱指示剂的性质及应用 知识点题库
选项 | 实验操作 | 现象 | 结论 |
A | 用黄铜片在铜片上刻画 | 铜片上有划痕 | 黄铜的硬度比铜大 |
B | 用小木棍蘸少量浓硫酸 | 木棍变黑 | 硫酸有强酸性 |
C | 向某溶液中滴入无色酚酞试液 | 无色酚酞试液不变色 | 无色溶液一定是酸 |
D | 向某溶液中滴入稀硫酸 | 有气泡产生 | 该物质一定含CO32﹣ |
选项 | 物质 | 目的 | 主要实验操作 |
甲 | CO、CH4气体 | 鉴别 | 点燃,火焰上方罩干冷烧杯,观察现象 |
乙 | Na2CO3(NaOH)溶液 | 检验 | 滴加酚酞试液,观察溶液颜色的变化 |
丙 | HCl(H2SO4)固体 | 除杂 | 加入适量BaCl2溶液 |
丁 | MnO2、KCl 固体 | 分离 | 溶解、过滤、洗涤、烘干、蒸发 |
-
(1) 维生素C(C6H8O6)的相对分子质量为176,其计算式为。
-
(2) 取维生素C片溶于水,滴入紫色石蕊溶液变红色,说明其溶液显(填“酸”或“碱”)性。

-
(1) 设备4中经过操作,将水和石膏固体进行分离。
-
(2) 设备1的作用是通过喷淋水脱去烟气中的SO2 , 生成一种酸——亚硫酸(H2SO3),该反应的化学方程式为。
-
(3) 若将二氧化硫气体通入紫色的石蕊溶液中,猜想可能出现的现象是。
-
(4) 脱硫工艺流程中。可以循环利用的物质是。
| 方案 | 实验目的 | 实验设计 |
| A | 除去KCl中混有的少量KClO3 | 取样,加入二氧化锰充分加热 |
| B | 除去氧化钙中少量的碳酸钙 | 取样,加入足量的水,溶解、过滤 |
| C | 除去氮气中含有少量的氧气 | 通过灼热的铜网 |
| D | 探究稀盐酸与氢氧化钠溶液是否恰好完全反应 | 向反应后的溶液中滴加酚酞溶液 |

-
(1) A实验中观察到的现象是
-
(2) B实验中发生反应的化学方程式为
实验完毕后,小亮同学在整理仪器时,将上述实验后的废液倒入同一个洁净的成液缸中,发现混合后的废液仍然浑浊并显红色,于是引起了他的质疑和探究兴趣。
-
(3) (提出问题)混合废液中可能含有的碱性物质有哪些?
(作出猜想)他断定混合废液中一定含有氢氧化钠,理由是;并对是否含有其它碱性物质作出猜想:猜想Ⅰ:
 ;猜想Ⅱ:
;猜想Ⅱ: 
-
(4) (实验验证)小亮认为只要用反应物(饱和石灰水和碳酸钠溶液)就可以验证猜想。于是他对混合废液进行过滤,并取少量滤液进行了下列实验:
实验操作
实验现象
实验结论
 M是
M是猜想Ⅱ错误
 N是
N是猜想Ⅰ正确
-
(5) (反思与交流)
验证完毕,小刚同学受到启发,于是他又设计了一个实验,进一步验证混合废液中含有的碱性物质。他取一定最的滤液于试管中,然后逐滴滴加稀盐酸至过量,反应过程和产生的现象如图所示。分析图象数据可以得出混合废液中含有的碱性物质一定是

-
(6) (拓展应用)为了把以上废液安全排放,你的做法是。

-
(1) 课外小组的同学自制一块多槽铁板,设计如图A所示装置,用以探究燃烧的条件。(说明:金属板上白磷足量)。请回答下列问题
①证明可燃物燃烧需要一定温度的依据是。
②将过氧化氢溶液滴入盛有MnO2的金属槽中,发生反应的化学方程式。
③有同学提出“将NaOH换成水,然后将水换成浓硫酸,也可以完成探究活动“,你认为是否可行,为什么?
-
(2) 如图B所示的装置进行验证质量守恒定律,试剂a可以是(写出一种即可)。证明质量守恒定律成立的现象是。
-
(3) 根据如图C所示实验,Y烧杯中溶液由红色变为无色。
①该实验可证明微粒具有的性质是。
②请用化学方程式表示红色变为无色的原因。
③该实验得出氢氧化钡的化学性质有。
|
物质 |
①水 |
②水垢清除剂 |
③肥皂水 |
④白醋 |
⑤雪碧 |
|
颜色 |
紫色 |
红色 |
蓝色 |
红色 |
红色 |
判断上述物质中,显酸性的有(填序号)。

试管编号 | ① | ② | ③ | ④ |
试管内试剂 | NaOH溶液 | MgCl2溶液 | Na2CO3溶液 | Ba(NO3)2溶液 |
加入稀硫酸后的现象 | 无明显现象 | 无明显现象 | 产生气泡 | 白色沉淀生成 |
-
(1) 根据以上实验现象,可以判断试管③④中发生了复分解反应。小明同学向盛有NaOH溶液的试管中先加了一种试剂,再加稀硫酸,从而能说明试管①中也发生了反应,这种试剂是。
-
(2) 为了验证试管②中是否发生复分解反应,小明同学进行了如下探究。
[提出猜想]
猜想1:试管②中没有发生复分解反应,溶液中有MgCl2 , 即Mg2+和Cl﹣同时存在溶液中。
猜想2:试管②中发生了复分解反应,溶液中无MgCl2。
老师提示
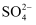 会对Cl﹣的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了如图实验方案。
会对Cl﹣的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了如图实验方案。[设计方案]

沉淀A的化学式是。老师评价该方案时指出:设计思路正确,但试剂选择有误,你认为证明猜想1正确,修改后的实验方案是。(写出操作和现象)
-
(3) [实验反思]小明反思进行步骤Ⅲ时,加NaOH溶液采用了滴加的方式,但没有立即观察到任何现象,你认为其中的原因是。

-
(1) 第一步后,溶液为无色的孔穴有(填孔穴序号)。
-
(2) 第二步后,孔穴1中发生反应的化学方程式为。
-
(3) 第二步后,孔穴2、3的溶液均变成红色,说明Na2CO3溶液显(填“酸”或“碱”)性,此时孔穴2的溶液中含有的溶质是。
- 阅读下列材料 材料1 (各国第一批进入北京的)这些代表们并没有忽视他们的首要责任——要约束中国人适当地履行条约条
- 以下关于蛋白质及其对应功能的描述,正确的是 A.动物激素都是蛋白质,对生命活动具有重要调节作用 B.神
- 六价铬对人体有毒,含铬废水要经过化学处理后才能排放。 工业上为处理含有的酸性废水采用如下方法:在工业废水中加入适量NaC
- 下列物质的化学式书写不正确的是() A.氧化镁 MgO2 B.氧化钠Na2O C.硫酸锌 ZnSO4 D.氢氧化铜Cu
- 1.下列各句中,加点的成语使用恰当的一项是(3分) A. 他获得了参加复赛的资格,但平时不刻苦训练仅依靠现场
- 昆虫学家用人工诱变的方法使昆虫产生基因突变,导致酯酶活性升高,该酶可催化分解有机磷农药。近年来已将控制酯酶合成的基因分离
- 用数字和符号填空 ⑴ 碳酸根离子 ⑵ 四个硫原子 ⑶ 保持水化学性质的最小粒子 ___
- 在苏俄新经济政策的内容中,最能体现多种所有制成分并存的是 A.农业领域 B.工业领域 C.流通领域
- 2013年3月,上海、安徽两地率先发现H7N9型禽流感,某药店以每件50元价格购进800件治疗H7N9的某特效药,第一
- 近年来,随着科技的发展,汽车、手机等商品价格不断下跌,价格大战此起彼伏,企业面临生死考验。 根据以上材料回答问题: (1
- 已知椭圆的离心率为,双曲线的渐近线与椭圆有四个交点,以这四个交点为顶点的四边形的面积为16,则椭圆的方程为( ) A.
- 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。 ⑴ 图中有两处明显的错误是:①
- 过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,
- 如图是书本上演示小蜡块运动规律的装置。在蜡块沿玻璃管(方向)上升的同时,将玻璃管紧贴着黑板沿水平方向(方向)向右运动,得
- I regret ________ up to watch thefootball game last night.I
- 假如某国 M 商品由甲、乙、丙三厂生产,甲厂的个别劳动时间比丙厂长,乙厂的劳动生产率比丙厂高。不考虑其他因素,则下列判断
- 文学常识及名著阅读(6分)(1)“我记得当年玉帝妹子思凡下界,配合杨君,生一男子,曾使斧劈桃山的,是你么?我心要骂你几声
- 点P(8,1)平分双曲线x2-4y2=4的一条弦,则这条弦所在直线方程是 .
- 由氧化铜和氧化铁的混合物a g,加入2 mol·L-1的硫酸溶液50 mL,恰好完全溶解,若将a g的该混合物在过量的C
- 12、依次填入下列各句横线处的成语,最恰当的一组是( )(3分) ①业主希望解除双方的物业管理合同,而面对法



