晶体和结晶的概念与现象 知识点题库
实验操作 | 现象 | 结论 | |
A | 向收集满CO2的软塑料瓶中加入约 | 塑料瓶变瘪 | CO2能与NaCl反应 |
B | 50℃时,将17g KCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时,KCl的溶解度为17g |
C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |

-
(1) 0℃时,A,B,C三种物质溶解度由小到大的顺序是.
-
(2) t1℃时,将40克C物质放入l00克水中,充分搅拌,所得溶液的质量是克.
-
(3) 要使接近饱和的A物质溶液变成饱和溶液,可采取的一种措施是.
-
(4) 将t1℃的A,B,C三种物质的饱和溶液分别升温至t2℃,所得溶液溶质质量分数的大小关系
是.
-
(5) 将t2时A,B,C三种物质饱和溶液降温到t1时,A中(有无晶体),变成t1的不饱和溶液.
-
(1) 水的组成
图1是18世纪化学家卡文迪许做的关于水的组成的实验.写出该反应的化学反应方程式,实验现象是.

该实验证明了水是由(填名称)元素组成的化合物.
全部溶解的方法是.(任写一种)
-
(2) 水的性质
①少量下列物质加入到水中,充分搅拌后,可以得到溶液的是.
A.牛奶 B.蔗糖 C.食盐 D.花生油
②一种抗生素为粉状固体,每瓶含1g.注射时应配成质量分数为20%的溶液,则使用
时每瓶至少需加入蒸馏水 mL.
③甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图2.
Ⅰ.下列说法正确的是.
A.t1℃时,三种物质的溶解度:乙>甲=丙
B.20℃时,将30g甲放入50g水中,充分搅拌,所得溶液的质量是80g
C.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体质量最大
D.分别将t1℃时三种物质饱和溶液升温到t2℃,溶液中溶质的质量分数:乙>甲>丙
Ⅱ.20℃时,将40.0g甲放入100.0g水中,充分搅拌后,发现固体没有全部溶解,请你解释甲固体没有全部溶解的原因可能是.要使该固体全部溶解的方法是(任写一种)

-
(1) t2℃时,A物质的溶解度是g.
-
(2) p点的含义是.
-
(3) 将t2℃A,B的饱和溶液分别降温至t1℃,成为不饱和溶液的是(填A或B).
-
(4) 下列说法正确的是(填序号).
①t2℃时,A,B溶液中的溶质的质量分数A>B;
②t2℃时,用等质量的A,B分别配制成饱和溶液,所得溶液质量A>B;
③通过恒温蒸发溶剂的方法可使A,B的饱和溶液同时析出晶体;
④t2℃时,将150gA的饱和溶液稀释成质量分数为20%的溶液需加水100g.

 ×100%
C . 如果A中含有少量B,可用降温结晶法提纯A
D . 将t2℃时B的饱和溶液降温到t1℃时,溶液变稀了
×100%
C . 如果A中含有少量B,可用降温结晶法提纯A
D . 将t2℃时B的饱和溶液降温到t1℃时,溶液变稀了

 两种物质的溶解度曲线如图所示
两种物质的溶解度曲线如图所示  下列说法正确的是
下列说法正确的是 

|
温度(℃) |
0 |
20 |
40 |
60 |
80 |
100 |
|
|
溶解度(g) |
KNO3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
246 |
|
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
|
-
(1) 20℃时,KNO3和NaCl中的溶解度较大;
-
(2) KNO3和NaCl中,更适合用“冷却热饱和溶液”的方法从溶液中获得较多晶体的是:;
-
(3) 60℃时,饱和KNO3溶液中溶质和溶剂的质量比为。
-
(1) 水与人类的生活密切相关。
①硬水给生活和生产带来许多麻烦,一般可用来区分硬水和软水。
②可利用活性炭吸附水中的异味和色素,活性炭的吸附性属于(填“物理”或“化学”)性质。
-
(2) 下表是KNO3和Ca(OH)2在不同温度时的溶解度。回答有关问题:
温度/℃
10
20
30
40
50
60
溶解度/g
KNO3
20.9
31.6
45.8
63.9
85.5
110.0
Ca(OH)2
0.19
0.17
0.16
0.14
0.13
0.11
①两种物质中,溶解度随温度升高而减小的是。
②60℃时,按图示操作:

A中的溶液是(填“饱和”或“不饱和”)溶液。
C中析出固体的质量是g。
③如图,向烧杯中加入一定量的硝酸铵固体,此时试管中氢氧化钙溶液的溶质质量分数将(填“变大”不变”或“变小”)。


A.  ℃时,65gA的饱和溶液中含有50g溶剂
℃时,65gA的饱和溶液中含有50g溶剂
B.在  ℃,A,B两种物质的溶液溶质质量分数相同
℃,A,B两种物质的溶液溶质质量分数相同
C.将  ℃A,B,C三种物质的饱和溶液升温至
℃A,B,C三种物质的饱和溶液升温至  ℃时,溶液中溶质质量分数由小到大的顺序为C<B=A
℃时,溶液中溶质质量分数由小到大的顺序为C<B=A
D.当A中含有少量B时,提纯A的方法是



-
(1) t3℃时,甲物质的饱和溶液中,溶质、溶剂、溶液的质量之比为。
-
(2) t2℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是(用“甲”、“乙”、“丙”及“>”、“<”或“=”表示)
-
(3) 将t3℃的甲、乙、丙三种物质的饱和溶液各100g,分别降温至t1℃,所得溶液的质量最大是(用“甲”、“乙”、“丙”填空)。
-
(4) 若甲中含有少量乙,可通过法提纯甲。

①t1℃时,A的饱和溶液和C的饱和溶液中溶质的质量相等
②要使C的饱和溶液转化为不饱和溶液,可采用升温的方法
③从含有少量B的A饱和溶液中得到较多的A晶体,通常可采用冷却热饱和溶液的方法
④t2℃时,若从A和B两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是A物质的饱和溶液
⑤将t2℃时,A、B、C的饱和溶液分别降温至t1℃,所得溶液中溶质的质量分数B>A=C
以上说法中正确的数目有( )

-
(1) t℃时硝酸钾和氯化钾的溶解度相等,均为。
-
(2) 60℃时,分别将等质量的KNO3和KCl两种物质的饱和溶液温度降至30℃,析出晶体的质量关系为:KNO3KCl(填写“>”“=”或“<”)。
-
(3) 如图2所示,20℃时,将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是____(填写字母标号)。
①冰块②生石灰固体③硝酸铵固体④干冰⑤浓硫酸⑥氢氧化钠固体
A . ①③④ B . ②⑤⑥ C . ①③⑤ D . ②④⑥
- 如图所示,光滑水平面上停着一辆小车,小车的固定支架左端用不计质量的细线系一个小铁球.开始将小铁球提起到图示位置,然后无初
- 2009年5月25日,朝鲜进行了一次地下核试验,声称是为加强朝鲜的自卫核遏制能力。安理会15个理事国举行紧急磋商后一致认
- ---Canyou show ______________ your photos when you come back
- 已知二次函数y=2x2﹣2(a+b)x+a2+b2,a,b为常数,当y达到最小值时,x的值为() A.a+b B. C
- 诗歌鉴赏(6分)阅读下面这首诗,回答题目晚渡咸阳明·马中锡①野色苍茫接渭川②,白鸥飞尽水连天。僧归红叶林间寺,人唤斜阳渡
- 学习是不断总结的过程,下列小军同学的总结中错误的是 A.水银不是银 B.干冰不是冰 C.纯碱不是碱
- 图7-8是花的结构示意图,请据图回答问题:(1)图中[ ]和[ ]组成了雄蕊,[ ]、[ ]和[
- 下列诗句或谚语可能与化学现象有关,其中说法不正确的是() A.“水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化
- 分子数相同的和之间氧元素质量比是()。 A.1:1 B.2:1 C.1:4 D.1:2
- It’s a fine day. What about to the park? A.go
- 敏而好学, ,是以谓之文也。(《论语·公冶长》)
- 真核细胞某生理过程如图所示,下列叙述错误的是 A.酶1可使磷酸二酯键断裂,酶2可催化磷酸二酯键的形成 B.a链和b链的
- 利用金属晶格(大小约10-10 m)作为障碍物观察电子的衍射图样,方法是让电子通过电场加速,然后让电子束照射到金属晶格上
- 读下面一段话,读完后请运用以子之矛攻子之盾的方法为长工设计一句话来反驳地主。 一天,地主“命令”长工去给他买酒,长工问:
- Bob,you watched the fashion show last night, ________ ?
- 19世纪末,维新变法运动( ) ①是一场救亡图存的爱国运动 ②核心是主张兴民权,实行君主立宪③是民族资产阶
- 下列古代的官职,按分组不同的是 A.、太尉、通判 B.丞相、参知政事 C.御史大夫、刺史
- She spoke very confidently because she wanted to make a grea
- 某班5位同学的身高(单位:米)为:1.5,1.6,1.7,1.6,1.4.这组数据( ) A.中位数是1.7
- 英语是一门重要的工具性学科。有人认为学习英语为了出国;也有人认为学习英语为了升学;还有人认为学习英语为了找到好工作等等。
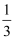 体积的NaCl溶液,旋紧瓶盖,振荡
体积的NaCl溶液,旋紧瓶盖,振荡


