晶体和结晶的概念与现象 知识点题库

-
(1) 50℃时,乙物质的饱和溶液中溶质与溶液的质量比为;
-
(2) 通过加溶质、蒸发溶剂和加热都能将接近饱和的溶液变为饱和溶液的物质是
-
(3) 50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是,所得溶液中溶质质量分数最小的是.
-
(4) 若除去甲中混有的少量乙时,有以下实验步骤:
①常温下溶于水②过滤 ③降温结晶④蒸发浓缩.
合理的先后顺序是.



-
(1) 温度为℃时,A与C物质的溶解度相等.
-
(2) t2℃时,把A,B物质各30g分别加到50g水中,不能形成饱和溶液的是(填字母代号)
-
(3) t2℃时,将等质量A,B,C三种物质的饱和溶液降温至t1℃,所得的三种溶液中,溶剂质量的大小关系是(用字母代号和“>“、”<“或“=”填写)

-
(1) 20℃时,KNO3的溶解度约为g;
-
(2) 要使氯化钠从其饱和溶液中大量结晶析出,最好采用的结晶方法是
-
(3) 将NaCl和KNO3各30g,分别放入10℃100g水中充分溶解,能形成饱和溶液的是;(选填“NaCl”或“KNO3”)
-
(4) 分别将40℃的NaCl饱和溶液与KNO3饱和溶液,同时降温至10℃,下列有关说法中,正确的是 . (填序号)A . 析出晶体的质量一定相等 B . KNO3溶液变成不饱和溶液 C . 两种溶液中溶质质量分数关系:NaCl>KNO3 .


-
(1) P点的含义是
-
(2) t2 ℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗?(填写“能”或“不能”)。
-
(3) t2 ℃时a、b、c三种物质的溶解度按由小到大的顺序排列是(填写物质序号)。
-
(4) 将t1 ℃时a、b、c三种物质饱和溶液的温度升高到t2 ℃时,三种溶液的溶质质量分数大小关系是 (填写选项序号)。A . c>a=b B . a=b>c C . a>b>c D . b>a>c
-
(1) 水(填“属于”或“不属于”)人类所需的六大基本营养素之一。
-
(2) 含有较多可溶性钙、镁化合物的水叫做(填“软水”或“硬水”)。
-
(3) 下列净化水的单一操作中,相对净化程度较高的是 (填字母)。A . 静置沉淀 B . 吸附沉淀 C . 蒸馏
-
(4) 水在通电的条件下可以分解,写出该反应的化学方程式。
-
(5) 甲和乙两种固体物质的溶解度曲线如下图所示,

回答下列问题:
①在℃时,甲和乙两种物质的溶解度相等。
②将t1℃时等质量的甲和乙两种物质的饱和溶液分别降温到0℃,析出固体质量较少的是(填“甲”或“乙”)。
③t2℃时,将60 g甲物质放入100 g水中,充分搅拌,所得溶液的溶质质量分数w(甲)与同温下乙物质的饱和溶液的溶质质量分数w(乙)大小关系为(填字母)。
A.w(甲)<w(乙) B.w(甲)>w(乙) C.w(甲)=w(乙) D.无法确定
-
(1) 净化水常用的方法有沉淀、过滤等,活性炭在净水器中能起到过滤和 的作用。
-
(2) 下列洗涤方法中,利用乳化原理的是__________________。A . 用洗涤精清洗衣服上的油污 B . 用酒精洗去试管中的碘 C . 用汽油清洗油渍
-
(3) 要将一瓶接近饱和石灰水变成饱和溶液,小明选择了如下的方法。其中可行的是(填序号)
①加入 CaO ②加入Ca(OH)2③升高温度 ④降低温度
-
(4) 如下图为甲、乙两种固体物质的溶解度曲线,请 据图回答下列问题

①t2℃时,甲、乙两种物质饱和溶液中的溶质质量分数的大小关系为:甲 乙(填“>”、“<”或“=”)。
②要从乙的饱和溶液中获得较多的晶体,宜采用的结晶方法是 结晶。
③t1℃,取等质量的甲、乙两种固体分别配成饱和溶液,需水质量较多的是(填“甲”或“乙”)。
-
(5) 下图是小明配制 50.0g 质量分数为18%的蔗糖溶液的实验操作示意图:

①配制上述溶液,小明需要称取蔗糖g
②用上图所示的序号表示符合题意配制该溶液的操作顺序为。
A.DECAB
B.ECADB
C.EDABC
③认真观察,改正图中的不符合题意操作。

| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度(g/100g 水) | 32 | 46 | 64 | 85.5 | 110 | 138 | 170 |
甲是 80℃含有 100g 水的 KNO3 溶液,操作过程如图所示。以下分析错误的是( )


 乙
B . 溶剂质量:甲
乙
B . 溶剂质量:甲  乙
C . 溶液质量:甲
乙
C . 溶液质量:甲 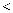 乙
D . 溶质质量
乙
D . 溶质质量

-
(1) 某同学设计的鉴别 NaNO2、NaCl固体的方案如下:
20℃时,取6.0gNaNO2和6.0gNaCl分别放入两只小烧杯中,各加入10mL水(水的密度为 1g/mL)。用玻璃棒充分搅拌后 观察现象。你认为此方案(填“可行”或“不可行”)。
-
(2) 除去 NaNO2固体中混有的少量 NaCl,实验步骤,加 水溶解,蒸发浓缩,,然后过滤、洗涤、干燥。
-
(3) 20℃时,将 182.2gNaNO2饱和溶液蒸发掉50g水,再降温到20℃,可析出晶体的质量为。
-
(4) 根据溶解度曲线,关于 NaNO2和NaCl 下列说法中错误的是______。A . 60℃时,NaNO2溶液的溶质质量分数大于NaCl溶液的溶质质量分数 B . 0℃时,等质量的两种固体加水配成饱和溶液,所得溶液的质量NaNO2溶液大于 NaCl溶液 C . 40℃时,NaNO2的饱和溶液降低温度,溶质质量分数减少 D . 60℃时,两种物质的饱和溶液降温到20℃时,NaNO2析出的晶体较多

A. t2℃三种物质的饱和溶液中,溶质质量最大的是A
B. t1℃的A,B,C三种物质的饱和溶液,分别蒸发等量的水后恢复至t1℃,析出溶质的质量B>A=C
C. 可用降低温度的方法使t2℃时C的不饱和溶液变为饱和溶液
D. 将t2℃时的三种物质的饱和溶液降温至t1℃时,溶质的质量分数由大到小的顺序是: .


|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
|
KNO3 |
13.3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
202 |
245 |
|
NaCl |
35.7 |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
39 |
39.8 |

-
(1) 依据上表数据,绘制KNO3 、NaCl的溶解度曲线,下图1中能表示KNO3溶解度曲线的是。(填“a”或“b”)
-
(2) 下图1中P点的含义是。
-
(3) 要使接近饱和的KNO3溶液,在不增加溶液质量的前提下变成饱和溶液,可以采用 。
-
(4) 30℃时,在两个各盛有100g水的烧杯中,分别加入相同质量的氯化钠和硝酸钾,充分溶解后,其结果如上图2所示,加入的甲物质是。
-
(5) 硝酸钾中含有少量氯化钠时,可通过(填“蒸发结晶”或“降温结晶”)的方法提纯。有下列可供选择的操作步骤:a.结晶 b.降温 c.热水溶解 d.过滤,具体采用的操作步骤依次是 。
-
(6) 20℃时,136g饱和食盐水,蒸发10g水后,再降温到20℃,可析出NaCl晶体的质量为g。
-
(7) 60℃时,将60g硝酸钾放入盛有50g水的烧杯中,充分搅拌,所得溶液的质量为g。
-
(1) 滇池,亦称昆明湖、昆明池、滇南泽、滇海。是云南省最大的淡水湖,有高原明珠之称,滇池不仅是昆明人民的母亲湖,更是一个丰富的生态系统。某学校化学兴趣小组的同学们欲对滇池的水样进行如下研究。
①小张先将水样进行,除去其中的难溶性杂质,再利用活性炭的性除去水中的异味; 再利用蒸馏的方法制取蒸馏水,在蒸馏过程中,水中加入少量碎瓷片的作用是。
②小李取该水样,利用如图装置完成实验。该实验中,负极和正极产生的气体体积比约为。

③为了保护好滇池,下列做法有利于保护水资源的是。
A.禁止在滇池中出现任何水生生物
B.禁止向滇池流域排放污水
C.关停滇池流域范围内的小型工厂
D.治理流域内的所有河流
-
(2) 如图是A、B、C三种不含结晶水的固体物质的溶解度曲线。

①t2℃时,将20gA加入60g水中,所得溶液的质量为g。
②t3℃时,取相同质量的A、B、C配制饱和溶液,所得溶液质量由大到小的关系是。
③将t2℃时A、B、C三种物质的饱和溶液升温至t3℃,所得溶液的溶质质量分数由大到小的关系是。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | KCl | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
- 用化学用语填空: (1)4个氧分子 ; (2)2个氮原子 ; (3)镁
- 如图右所示,将两个铅柱的底面削平、削干净,然后紧紧地压在一起,两铅块就会结合起来,甚至下面吊一个钩码都不能把它们拉开.这
- 国务院把清明、端午、中秋等传统节日列为国家法定假日,对传统节日文化进行了科学、有效的重构与再创造,使之有机“长入”今日的
- 设平面内有n个圆两两相交,且没有三个或三个以上的圆相交于同一点,它们把平面分成的区域数为p(n),如果该平面内再增一个符
- 与我国新疆接界的邻国分别属于A.西亚、中亚地区B.西亚、中亚、东亚、南亚地区C.西亚、东亚、北亚地区D.西亚、中亚、东亚
- 光滑斜面的长度为L,一物体自斜面顶端由静止开始匀加速滑至底端,经历的时间为t,则错误的是:( )A.物体运动全
- 化学是研究物质的结构、性质以及变化规律的科学,研究元素知识是学好化学的基础。下表包含部分元素的相关信息,完成以下填空:(
- 对右表中历史现象起直接推进作用的是A.辛亥革命 B.抗日战争的胜利结束 C.南京解放 D.中华人民共和国成立
- 对亚马孙流域这片全球最大的热带雨林的前景,正确的说法是 A.面对雨林正在遭受毁灭性破坏的严峻形势,应该把保护放在首位
- 下列关于物质的性质和用途说法正错误的是( ) A.石墨有滑腻感,可以做电极 B
- (A)有下列物质:①氧气;②氮气;③五氧化二磷;④二氧化硫;⑤二氧化碳;⑥氖气。请用这些物质的化学式填空: (1)空气中
- 0ne day we willmanage to the world this terrible di
- 如图所示,一轻弹簧与质量为m的物体组成弹簧振子,物体在同一条竖直线上的A、B间做简谐运动,O为平衡位置,C为AO的中点,
- 读“鞍钢和宝钢的区位图”,完成下列问题。 (1)鞍钢的区位优势是_________________。宝钢的区位优势是__
- 根据下列五种微粒的结构示意图,回答下列问题: (1)图中微粒共能表示 种元素。 (2)写出A与B组
- 下列混合溶液中,离子的浓度大小顺序正确的是() A.10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合,c(
- 下列各组词语中,读音完全正确的一项是( ) A.妃嫔pín 媵嫱yìng 颐yú养
- 下列关于产生氧气的方法的叙述中,错误的是 A.工业上用分离液态空气的方法制取氧气是分解反应 B.空气中的氧气主要来自于植
- 中国是一个全新的政党,“新”主要体现在 ①以马克思主义为指导②以武装斗争为主要方式③提出了彻底的反帝反封建纲领④以社会主
- 计算的结果为 ;



